Clear Sky Science · ja
e2MPRAを用いたエピゲノム解析と調節活性の同時測定
細胞の隠れたスイッチを読み解く
体内のほぼすべての細胞は同じDNAを持っているにもかかわらず、脳細胞と肝細胞はまったく異なる振る舞いをします。その違いの要因は、遺伝子の明るさを上げたり下げたり消したりするディマー(調光)スイッチのように働く短いDNA配列にあります。本研究はe2MPRAと呼ばれる強力な新技術を紹介します。これは何千ものこうしたスイッチを同時に検査できるだけでなく、細胞内でDNAがどのように包まれ、どのような目印が付くか—すなわち発生や疾患リスク、なぜ一部の遺伝変異が重要で他はそうでないのかを理解するうえで鍵となるプロセス—を同時に観察できます。
DNAの地図から機能へ
過去10年で、研究者たちはシス調節要素として知られる「候補」スイッチの大規模な地図を作成してきました。これらはDNAがどこで緩く折りたたまれているか(オープンクロマチン)、どのタンパク質が結合しているか、どのヒストン修飾が付いているかを示す手法によって得られます。これらの地図は印象的ですが、主に記述的です:タンパク質が結合していることや修飾が見られることが、その配列が実際に遺伝子活性を制御していることを証明するわけではありません。従来の大規模並列レポーターアッセイ(MPRA)は何千ものDNA断片がレポーター遺伝子を増強または抑制するかを検査できますが、そこにどのタンパク質が結合するかや、その活性に伴ってどのようなエピジェネティック変化が起きるかは示しません。
活性とエピジェネティックマークを同時に測る二刀流アッセイ
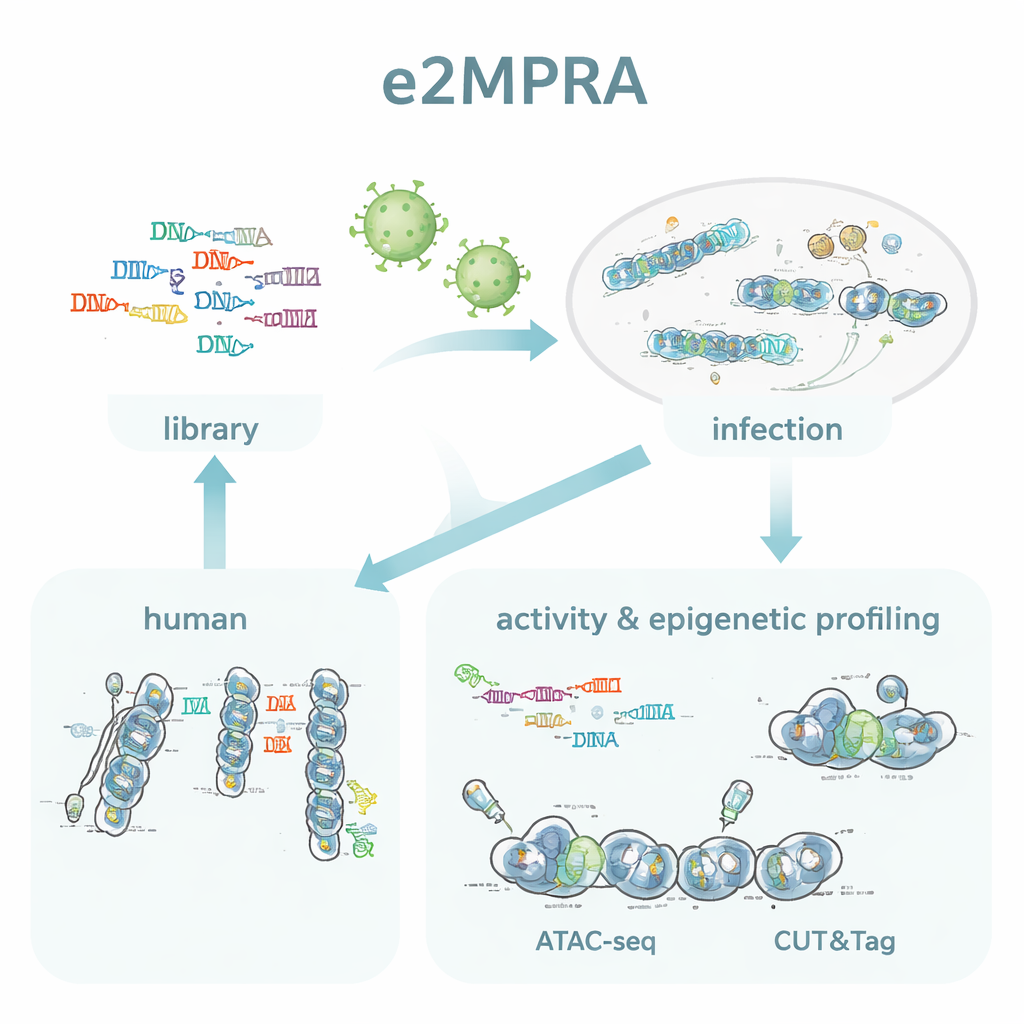
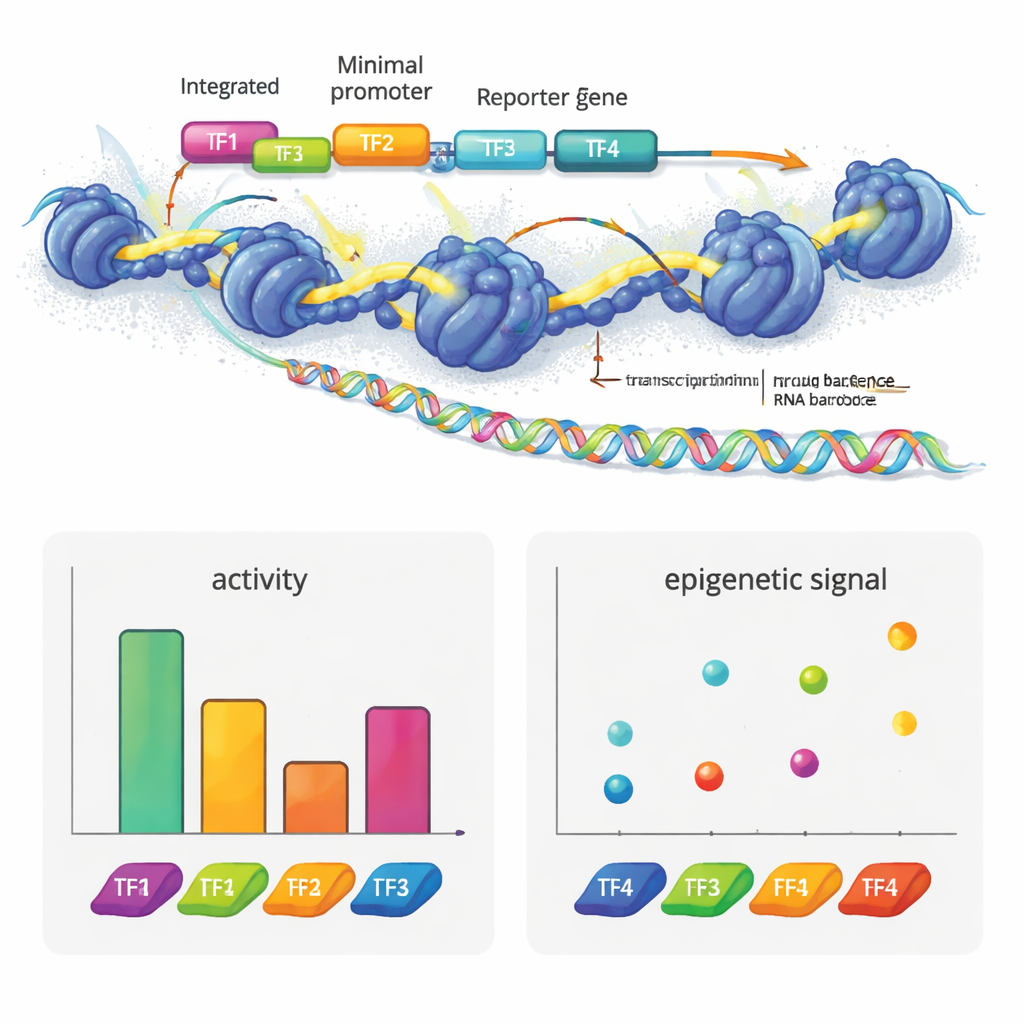
著者らは、レンチウイルスMPRAと二つのエピゲノム技術(ATAC-seqとCUT&Tag)を組み合わせることでe2MPRAを作り出しました。まず、各候補調節配列が短いバーコードに結び付けられ、ミニマルプロモーターとレポーター遺伝子の隣に配置されたDNAライブラリを構築します。このライブラリをレンチウイルスにパッケージし、培養ヒト細胞のゲノムに多数回統合させます。同じ細胞プールからRNA中のバーコードを読み取って調節活性を測定し、ATAC-seqとCUT&Tagを用いて挿入配列特異的にクロマチンの開放性と主要なヒストンマーク(H3K27ac)を測定します。これらの信号を各配列の実際の統合頻度で正規化することで、1回の実験で何千もの要素について「オン/オフの強さ」とエピジェネティック状態を並列に測定できます。
転写因子モチーフの協調作用を解読する
この技術が何を明らかにできるかを示すために、チームは肝細胞で使われる既知の転写因子モチーフから合成エンハンサーを作成しました。これらのモチーフを中性のDNAテンプレート上に異なる数や配列で配置しました。HNF1AやXBP1のような因子は古典的な活性化因子として振る舞い、コピー数が増えるほどレポーター出力が増加しました。一方でHNF1AやONECUT1のような因子は主にクロマチンのアクセス性を高め、「パイオニア」因子として閉じたDNAを開く役割に一致しました。PPARAは異なるパターンを示し、単独では転写を強く変化させないがクロマチンやヒストン修飾を大きく変え、他の因子と協調して遺伝子活性を高めました。既知のリプレッサーであるRESTは活性化因子の隣に置くと活性を抑えました。注目すべきは、四つのモチーフの並べ替えだけでエンハンサー強度が大きく変わることや、活性化因子はプロモーターに近いほど効果的に働く傾向があり、モチーフ配列に一種の文法構造が存在することが示された点です。
多能性エンハンサーの感受性塩基を特定する
研究者らは次に、多能性因子POU5F1(OCT4とも呼ばれる)とSOX2に結合する領域に注目して、幹細胞の同一性に重要なエンハンサーを調べました。100塩基長のエンハンサーの各塩基を体系的に変化させる高密度変異ライブラリや、ランダムに入れ替えた6塩基幅の小窓を作成しました。誘導多能性幹細胞でe2MPRAを用いることで、どの変異がレポーター活性を弱めたり強めたりし、クロマチンの開放性やアセチル化にどのように影響するかを観察できました。POU5F1::SOX2結合モチーフを破壊すると、多くの場合に遺伝子活性とエピジェネティックマークの両方が低下し、その中心的役割が確認されました。POU5F1遺伝子付近のよく研究されたエンハンサーでは、YY1モチーフを変えると転写は増加するがクロマチンの開放は減少することが見つかり、一部の因子は開放状態を促進しつつも発現を抑えるような複雑な働きをする可能性が示唆されました。
遺伝子と疾患への意味合い
e2MPRAはゲノムの自然な3D配線のすべてのニュアンスを完全に再現するわけではありませんが、同一条件下で何千もの調節配列やバリアントを比較する実用的な手段を提供します。機能的出力(DNA断片がどれだけ強く遺伝子を駆動するか)とエピジェネティック出力(そのDNAがどのように包まれ、マークされるか)を結びつけることで、本法はなぜ特定の転写因子モチーフやその組み合わせ、位置が重要なのかを解き明かす助けになります。長期的には、e2MPRAのようなツールは疾患に関連する非コード領域の遺伝的変異の解釈を容易にし、遺伝子治療のための合成エンハンサー設計を支援し、DNA配列と細胞挙動を結ぶより完全な「調節コード」を構築するのに寄与するでしょう。
引用: Zhang, Z., Georgakopoulos-Soares, I., Bourque, G. et al. Simultaneous epigenomic profiling and regulatory activity measurement using e2MPRA. Nat Commun 17, 1724 (2026). https://doi.org/10.1038/s41467-026-68422-3
キーワード: 遺伝子制御, エンハンサー, エピジェネティクス, 転写因子, 機能ゲノミクス