Clear Sky Science · ja
ガーディアンユビキチンE3リガーゼはがん関連のAPOBEC3脱アミノ化酵素を分解の標的としてヒトゲノムの完全性を促進する
味方の誤射からDNAを守る
細胞はウイルスDNAを損傷させる強力な酵素を動員し、感染と戦います。しかし、その同じ酵素のいくつかは制御を失うと自分たちのゲノムに傷をつけ、がんの一因になり得ます。本研究は、ヒト細胞がこうした危険な酵素をどのように監視しているかを解明し、危険な変異体に破壊のためのタグを付ける内在的な「品質管理」システムを明らかにしています。
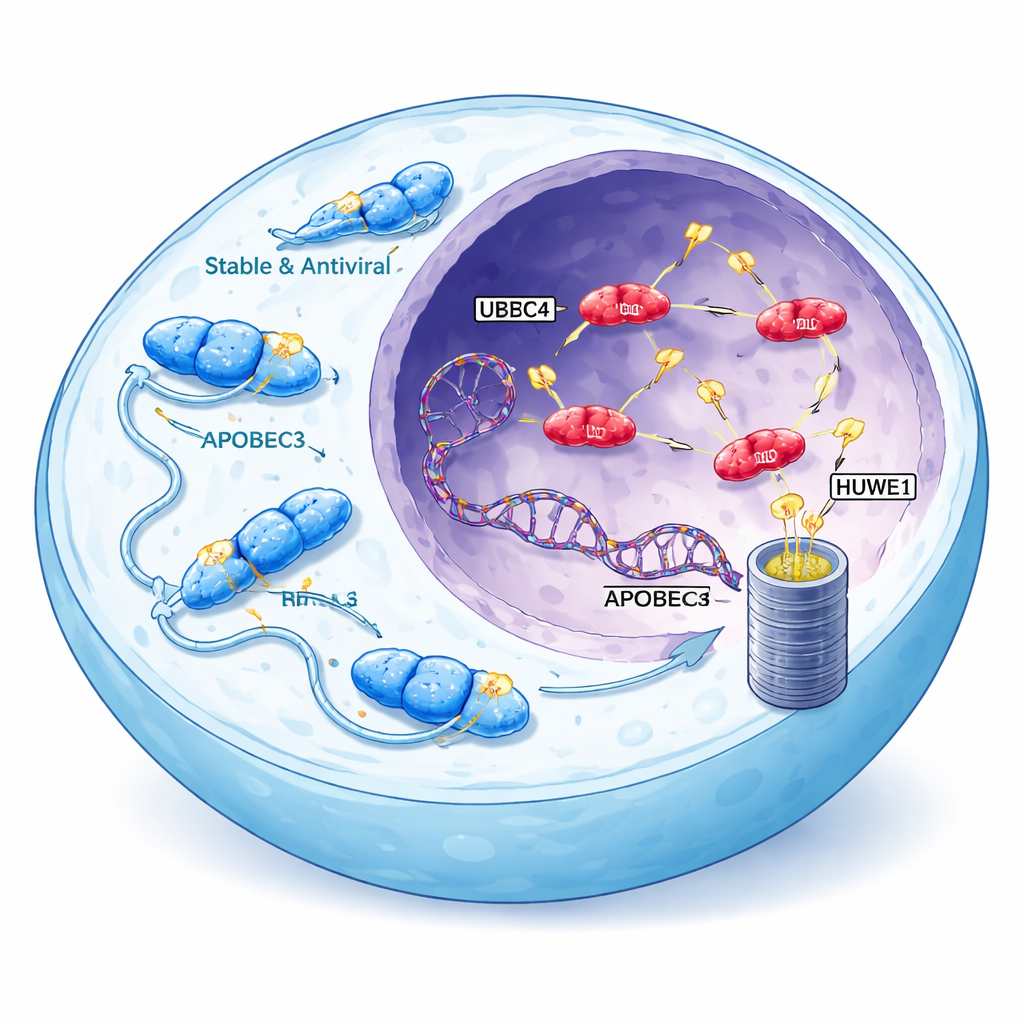
時に反旗を翻すウイルス防御因子
APOBEC3ファミリーの酵素は本来、HIVのようなウイルスに対してウイルスDNAを化学的に改変し致命的なエラーを誘導して防御に寄与します。ヒトは7種類のAPOBEC3変異体を持ち、そのうち3つ—A3A、A3B、そしてA3HのハプロタイプI(A3H-I)—は多くのがんで見られる変異パターンと強く結びついています。これらの酵素は細胞核に移動して染色体に作用し、ゲノムに特徴的な変異クラスターを導入します。APOBECに関連する変異署名は、特に乳がん、肺がん、膀胱がんで多く見られ、腫瘍が適応し治療に抵抗するための遺伝的多様性を拡大します。
危険な形態が奇妙に不安定な理由
興味深いことに、がんと最も強く結びつくAPOBEC3酵素は最も不安定でもあります。細胞質に滞留して高濃度でウイルスを効率的に阻害する仲間とは異なり、A3A、A3B、A3H-Iは速やかに分解され、通常は核内では低濃度で存在します。研究者らはこの不安定性が意図的な制御の産物であると考えました。もし細胞が核内のAPOBEC3タンパク質量を積極的に制限しているなら、その制御が破綻すると突然の変異誘発が起こり得るからです。A3H-Iをモデルとして用いた実験で、がん関連APOBEC3が主にプロテアソーム、すなわち細胞のタンパク質破砕装置によって分解されることが示され、複数のアミノ酸部位に小さな分子「ユビキチン」で標識された後に破壊されることが分かりました。
細胞内のガーディアンを突き止める
A3H-IとA3Bに標識を付ける機構を特定するために、研究チームはCRISPRスクリーニングとタンパク質近接マッピングを組み合わせました。A3H-Iと無害な変異体A3H-IIの安定性に応じて細胞が異なる蛍光を示すように設計し、タンパク質分解に関わる遺伝子を系統的に破壊しました。すると、ユビキチンリガーゼのUBR4、UBR5、およびHUWE1の3つが際立って見つかりました。これらのいずれかをノックアウトすると、不安定で核内にあるA3H-Iの量だけが選択的に増加し、安定で細胞質にいるA3H-IIには影響しませんでした。同じリガーゼ群は大腸や免疫系の細胞株でも内因性A3Bの量を独立に増加させ、3つすべてを同時に削除するとA3B量は累加的に増加しました。生化学的実験では、UBR5とHUWE1がA3BやA3H-Iに物理的に結合して直接ユビキチン鎖を付加する一方、UBR4はこれらの鎖を伸長してタンパク質をより効率的に廃棄可能にする役割を担うように見えることが示されました。
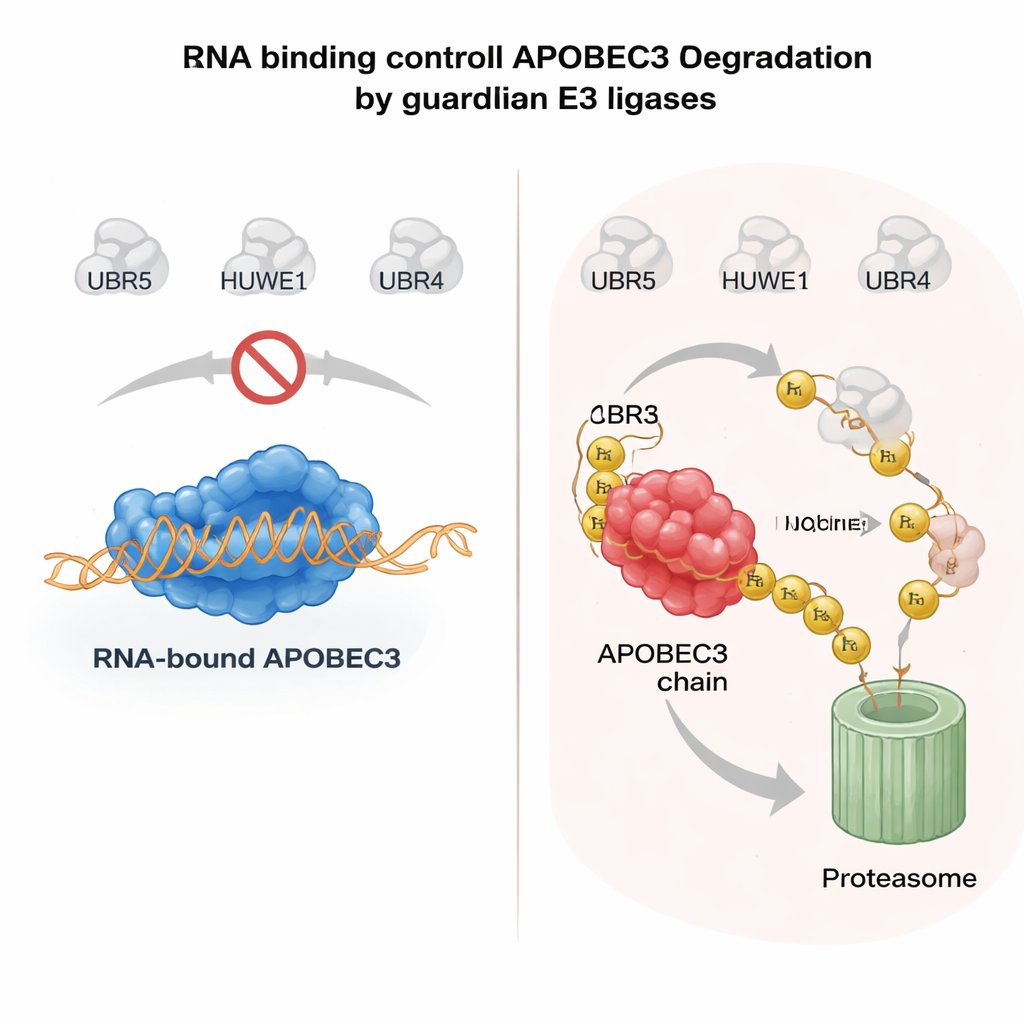
危険な酵素を縛る安全ベルトとしてのRNA
どのAPOBEC3酵素が保護され、どれが分解されるかを決めるものは何でしょうか。重要な手がかりは、APOBEC3タンパク質が細胞質のRNA分子に結合する仕方にありました。A3Hや同ファミリーの別メンバーであるA3GがRNAに結合すると、大きな複合体として細胞質に留まり比較的安定になります。RNA結合を弱める変異はこれらの酵素を核へと漂わせ、保護するパートナーを失わせて非常に不安定にします。著者らは、APOBEC3がRNAに結合していない場合、UBR5とHUWE1が酵素の露出した表面を認識してユビキチンで装飾し、核内での分解へと導くことを示しました。精製系では、RNAを除去するためにRNaseを加えるとこれらのリガーゼがAPOBEC3に結合してユビキチン化する能力が大きく増強され、RNA結合が分子レベルの盾として働くことが確認されました。この仕組みにより、細胞は細胞質での抗ウイルスAPOBEC3を活性のまま保ちつつ、核内でRNAに結合していないゲノムを脅かすプールを迅速に除去できます。
ガーディアンが失敗したとき:がん変異との関連
もしUBR4、UBR5、HUWE1がガーディアンとして働くなら、これらが失われると変異レベルが上がるはずです。研究者らはこれを検証するために各リガーゼを大腸がん細胞で無効化し、時間経過でのDNA変化を感度の高い配列解析法で追跡しました。特にA3H-Iを発現する細胞では、これらのリガーゼを除去するとAPOBEC特異的な変異パターンが増幅され—まさにヒト腫瘍で見られる種類の変化が生じました。患者データに拡張して解析すると、UBR5やHUWE1に変異を持つ腫瘍は、リガーゼが正常な腫瘍に比べてAPOBECに関連する変異署名の割合が有意に高いことが数千のがんゲノム解析で示されました(全体の変異負荷を考慮しても)。これは、患者におけるガーディアンリガーゼの欠損ががん関連APOBEC3酵素の暴走を許し、腫瘍ゲノムを再構築している可能性を示唆します。
将来のがん医療にとっての意義
専門外の人への要点は、細胞が抗ウイルス酵素が誤って自分のDNAを損なわないようにする洗練された監視システムを持っているということです。UBR4、UBR5、HUWE1はAPOBEC3酵素がもはやRNAに安全に結合していないことを感知し、特に核内でそれらを細胞の破砕装置へ送ります。この制御系がリガーゼの変異やタンパク質分解を阻害する薬剤によって弱まると、APOBEC3活性が遺伝的混乱を助長し、がんの進化や治療抵抗性を促進し得ます。このガーディアンネットワークを理解することは、リガーゼ変異やAPOBECタンパク質量といった新しい診断マーカーへの道を開き、将来的には抗ウイルス防御を損なわずに腫瘍内の有害な突然変異の発生を抑えるためにこの経路を慎重に調節する可能性を示唆します。
引用: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
キーワード: APOBEC3, ゲノム安定性, ユビキチンリガーゼ, がん変異原性, タンパク質分解