Clear Sky Science · ja
深層学習とナノポア直接RNAシーケンシングによるRNA修飾の動態と相互作用の包括的マッピング
RNAの隠れた句読点
細胞内のRNA分子は単なるA、C、G、Uの並びではありません。そこには多くの小さな化学的マークが飾られており、句読点のように働いて、どの遺伝子がオンになるか、タンパク質がどのように作られるか、細胞がストレスや疾患にどう応答するかを制御します。しかしこれまで、科学者は主にこれらのマークを一度に一種類ずつしか調べられず、ゲノム全体でそれらがどのように連携しているかを把握するのは難しかった。本論文はORCAという、ネイティブなRNA分子を直接読み取り、これらの化学的マークとその相互作用のグローバルで多層的な地図を構築する深層学習システムを紹介します。
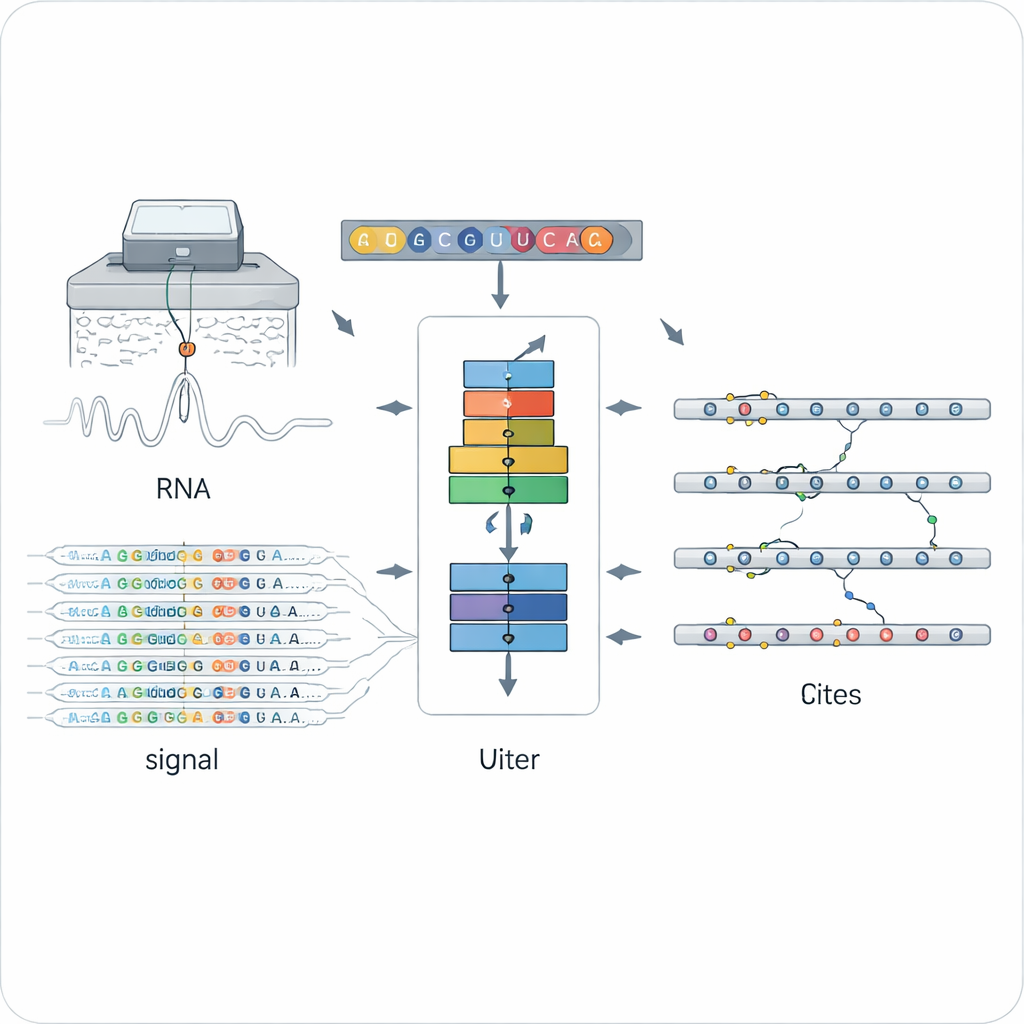
RNA上の化学マークを読む新しい方法
従来のRNA修飾検出法は、一般に特定のタイプのマーク(例えば広く用いられるN6‑メチルアデノシン(m6A))に対応した抗体や化学処理に依存してきました。これにより感度は高いものの対象は狭く、各手法は一種類のマークしか検出できないか、特定の実験条件に限られます。ナノポア直接RNAシーケンシングは別の道を開き、個々のRNA分子を微小な孔に通して、各塩基の正確な化学構造に応じて変化する電流を測定します。修飾された塩基と非修飾塩基は信号やベースコールを微妙に歪めますが、このノイズの多い高次元データを多様な修飾タイプにわたって解釈することは大きな課題でした。
あらゆるマークを見つけるようにニューラルネットワークを教える
ORCA(Omni‑RNA modification Characterization and Annotation)はこの課題に二段階で取り組みます。まず各位置の周辺に小さなウィンドウを設定し、多数のリードにわたる生の電気信号とシーケンシング誤りのパターンを集約します。特定の修飾を持つRNAコピーは一部に過ぎないため、真に修飾された部位は信号分布の偏りやその位置でのベースコール誤りの頻度が高くなります。ORCAは“敵対的”な戦略で訓練された深い再帰型ニューラルネットワークを用い、既知の単一化学型に固着することなく修飾と非修飾を区別する一般的なパターンを学習します。これにより各部位に対して修飾スコアと修飾を持つ分子の推定割合を割り当てることが可能になります。
各マークの正体を学ぶ
第二段階では、ORCAはどの種類の化学マークが存在するかをラベル付けすることを学びます。著者らは、従来の実験で既にm6A、5‑メチルシトシン(m5C)、Ψ(プソイドウリジン)、イノシン、2′‑O‑メチル化、そしていくつかの稀な修飾が同定されている公開データベースの高信頼部位をモデルに供給します。ORCAは信号パターン、配列文脈、各部位周辺の短い配列“モチーフ”を低次元のマップに圧縮し、修飾タイプとその塩基を予測するよう微調整します。重要な点は、ラベルのない部位も“背景”例として使われ、未知のマークを誤ったカテゴリに無理に押し込まないようにすることです。訓練が完了すると、ORCAは学習したラベルをトランスクリプトーム全体の何万もの未注釈部位に転移できます。
同時に多くの修飾を可視化する
ヒトおよびマウス細胞にORCAを適用したところ、著者らはそれがm6A、m5C、Ψなど特定のマークに対する先行ツールの精度に匹敵またはそれを上回るだけでなく、明示的に訓練されていなかったマークも検出できることを示しました。例えば、訓練時にm6Aデータを除外しても、ORCAは独立に測定された多くのm6A部位を回復し、修飾されていない類似配列モチーフと正しく区別しました。同様に2′‑O‑メチル基、イノシン編集部位、リボソームRNA上の多様な化学変化(質量分析で測定された多くの稀な修飾を含む)についても同様の検出が行われました。総じてORCAは既存データベースと比べてm5C、Ψ、m7Gおよびその他の低存在量修飾の注釈数を何倍にも拡大し、既知のRNA修飾サイトのカタログを大幅に増強します。
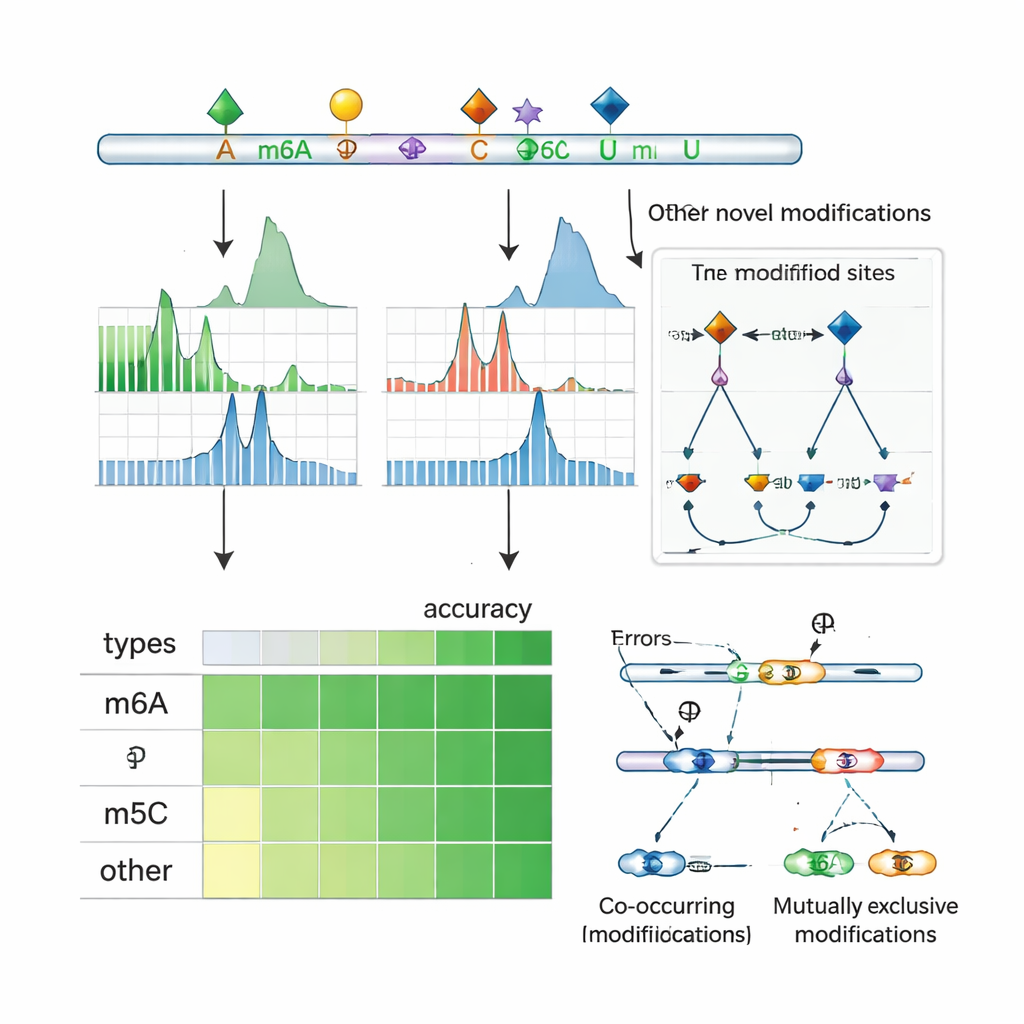
相互作用とスプライシング制御の解明
ナノポアシーケンシングはRNA分子全体を読み取るため、ORCAは同一トランスクリプト上でどのマークが同時に現れるか、あるいは互いに排他的かを調べることができます。著者らはRNA上の近接するマークをクラスタリングし、確率モデルを用いて二つの部位が単一分子上で共修飾されることが多いのか、相互排他なのかを推定します。彼らはm6Aとm5Cや他の修飾の共起が頻繁に見られること、また隣接する部位の一方が修飾されるのは隣の部位がされていない場合に限られる領域が多数存在することを明らかにしました。ヒトの細胞株では、これらのパターンは選択的に含まれるかスキップされるエクソンの近傍にしばしば位置し、スプライシング調節因子や修飾RNAを認識する“リーダー”タンパク質の結合部位と重なります。個々の遺伝子では、ORCAは特定のスプライスバリアントがある修飾パターンを多く含む一方で、別のバリアントは異なるパターンを持つことを示し、RNAの局所的な化学的装飾がメッセージの切接合にどう結びつくかを明らかにします。
生物学と医学にとっての意義
直接RNAシーケンシングと柔軟な深層学習を組み合わせることで、ORCAは複雑な電気信号をトランスクリプトーム全体にわたる化学マークの豊かで多層的な地図に変換します。非専門家にとっての主要な成果は、科学者が個々のRNA修飾がどこに生じるかだけでなく、どれだけ多様なマークが同一分子を飾るか、それらの組み合わせが遺伝子制御、特にRNAスプライシングとどう関連するかを見られるようになったことです。この枠組みにより、多くの細胞種や条件で各修飾のために新たな実験を設計することなくRNAの“エピジェネティクス”を研究できるようになり、発生、脳機能、がんや神経疾患などの病態にこれらの小さな化学的修飾がどのように寄与するかについての発見への道を開きます。
引用: Dong, H., Gao, Y., Cai, Z. et al. Comprehensive mapping of RNA modification dynamics and crosstalk via deep learning and nanopore direct RNA-sequencing. Nat Commun 17, 1722 (2026). https://doi.org/10.1038/s41467-026-68419-y
キーワード: RNA修飾, ナノポアシーケンシング, 深層学習, エピトランスクリプトーム, 選択的スプライシング