Clear Sky Science · ja
自己組織化した機械物質活性勾配による収縮性の空間配列がショウジョウバエの原腸形成の基本となる
組織はどうやって自ら形づくられるか
初期胚は、単純な細胞のシートを複雑な三次元形態に変えていきます。本研究はその仕掛けにある基本的な疑問を問います:組織が正しい位置と向きで折れ曲がるように、細胞はいつどこを収縮・曲げるかをどう協調して決めるのか?高解像度でショウジョウバエ胚を観察することで、著者らは「機械的モルフォゲン」のように振る舞い、細胞が自らを引き締める場所を直接配列して発生上の重要な折り畳みを駆動する化学シグナルを明らかにしました。
胚を折りたたむ波
ショウジョウバエ(Drosophila)では、初期発生の重要な段階が原腸形成で、平らな細胞層が内側に隆起して消化管の形成を始めます。胚の後方では、後端内胚葉原基と呼ばれる細胞群が頂端側(アピカル面)を収縮させることでこの過程を開始します。この初期の曲がりが、隣接する細胞群へと伝播する組織の陥入の波を引き起こします。著者らは、この波がFogと呼ばれる分泌分子に依存しており、FogはGPCRとして知られる受容体群を活性化し、さらにモータータンパク質Myosin-IIから成る細胞の収縮機構をオンにすることを示しています。
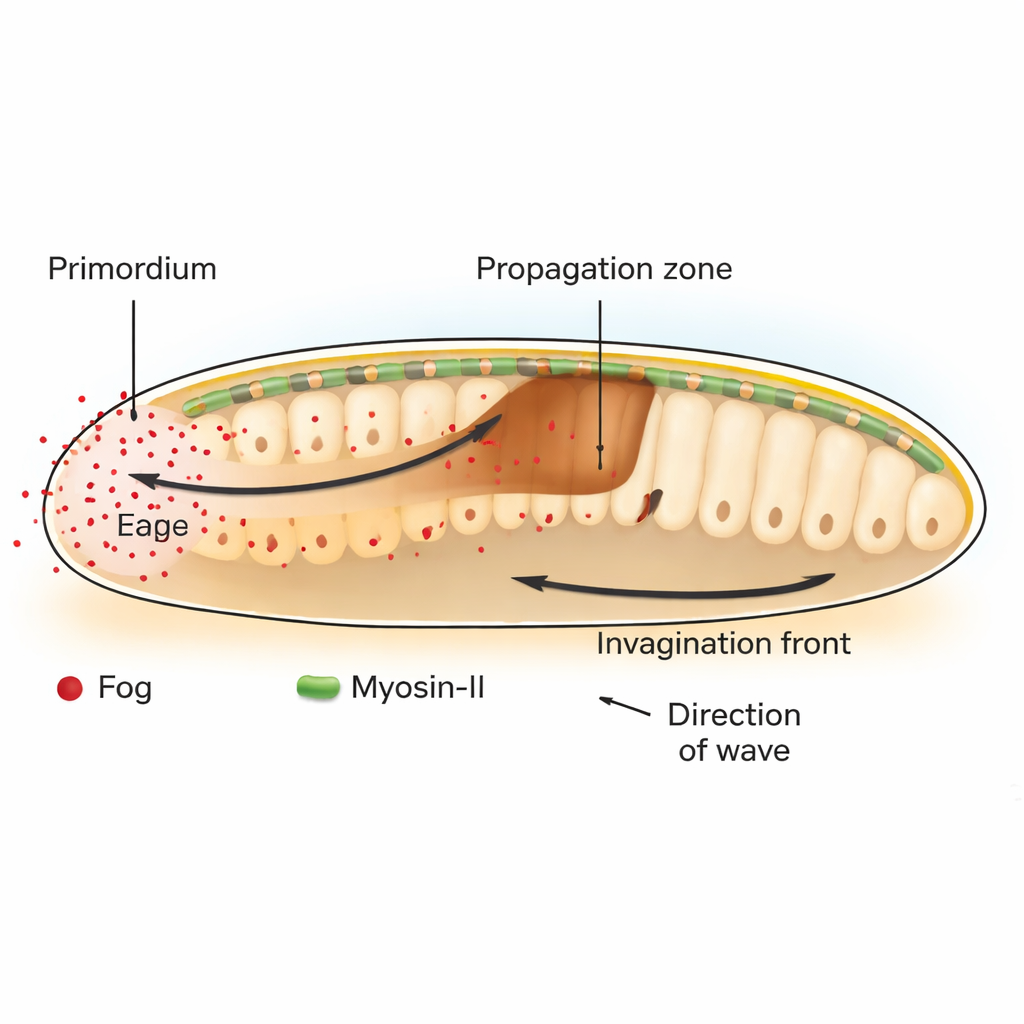
運命ではなく力を配列する化学物質
古典的に発生生物学は、濃度勾配によって細胞の運命(どの種類の細胞になるか)を指示する「モルフォゲン」に注目してきました。しかしここでのFogは異なる振る舞いをします。領域の細胞が何になるかを変えるのではなく、Fogは細胞の収縮の強さを直接調節します。原基内でのFogの産生を選択的に回復または遮断し、その下流の伝達因子Gαを特定領域で操作することで、研究者たちは原基で生じるFogが隣接する伝播領域におけるMyosin-IIの活性化と組織の折り畳みを遠隔で誘導するために必要かつ十分であることを実証しました。Fogが広がれないように固定されると、収縮するのは分泌細胞だけで、陥入の波はわずか一〜二列の細胞で停滞します。
細胞表面に隠れた勾配
自然な考え方として、Fogは細胞外に古典的な濃度勾配を作るかもしれないと想定されます。蛍光タグ付きFogと高感度蛍光測定を用いると、チームは逆の結果を得ました:組織と包む殻(卵黄膜)との間の薄い液層では、Fogは驚くほど均一に分布していました。しかしMyosin-IIの活性は、前進する折り目の直前で最も強く、数個分の細胞径で急速に減衰する鋭い、伝播する勾配を明確に作っていました。欠けていたピースは、Fogが単純なバルク濃度の手がかりとして働くのではなく、ごく一部のFogが細胞表面に一時的に捕捉されてGPCR受容体に結合し、自由なFog分子は流体中で均一でも表面に結びついた活性の勾配を作る、という点です。
受容体、エンドサイトーシス、接着が波を形作る
著者らは、この表面結合したFogが受容体とともに自己組織化してパターンを生むことを示します。Fogが受容体に繰り返し出会う場所では、受容体のクラスタリングと活性化が促され、これがさらに多くのMyosin-IIを呼び込みます。細胞の「片付け」機構であるGPCRのエンドサイトーシスは、活性複合体を除去して暴走的な活性化を防ぎ、信号の広がりを調節します。このエンドサイトーシスが遺伝学的に遅くなると、Myosin-IIの勾配は高さと幅の両方で増します。もう一つの重要な要素はインテグリンと呼ばれる接着分子群です。組織が曲がると折り目の前の細胞は卵黄膜に押し当てられ、この接触が局所的にインテグリンを活性化し、それがFog–GPCRシグナルの有効性を高めます。強いインテグリン関与の領域はMyosin-II勾配の範囲と一致し、インテグリンがないとFogシグナルが強化されても波は弱く短距離にとどまります。
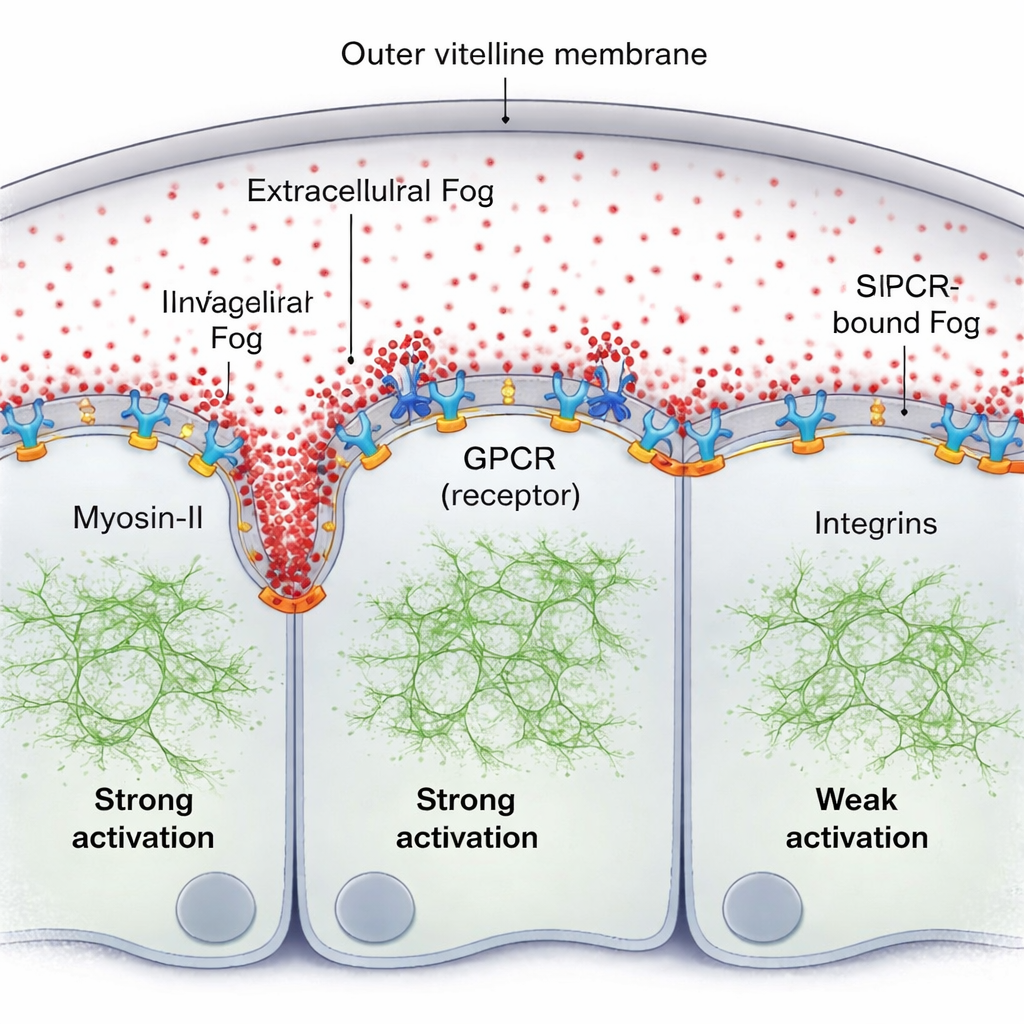
自己更新する機械的パターン
非専門家にとっての主なメッセージは、胚はどこを折り畳むかを決めるために事前に描かれた化学地図だけに頼っているわけではないということです。代わりに、胚は走行中に機械的活性の移動するパターンを構築します。Fogは均一に広がりますが、その実効的な作用は受容体のクラスタリング、受容体の除去、細胞が周囲に押し当てられることで変化する組織の幾何学によって細胞表面で造形されます。これにより、組織を内側に引き込む協調的な波を引き起こす自己組織化した走行性の収縮力勾配が生まれます。本研究は、拡散する分子が組織内の物理的力を直接配列するという長年理論化されてきた「メカノジェン」の具体例を提示し、生きた形が発生の過程でどのように常に整然と形づくられるかを説明する助けとなります。
引用: Mundhe, G., Dunsing-Eichenauer, V., Philippe, JM. et al. Spatial patterning of contractility by a self-organized mechanogen activity gradient underlies Drosophila gastrulation. Nat Commun 17, 1721 (2026). https://doi.org/10.1038/s41467-026-68418-z
キーワード: 原腸形成, メカノジェン, ショウジョウバエ胚, 組織力学, Fogシグナル伝達