Clear Sky Science · ja
DNA末端の構成がNHEJによる末端架橋時のシナプシス複合体形成を決定する
DNAが切れると、細胞は素早く判断しなければならない
私たちの細胞内のDNAは、日々の代謝や環境ストレスによって傷つき、切断され、損なわれます。最も危険な損傷の一つが二本鎖切断で、DNAらせんの両鎖が断たれる現象です。こうした切断が迅速かつ正確に修復されないと、細胞死を招くか、あるいはがんへと向かうリスクが高まります。本研究は、切れたDNA末端の正確な形状や化学的性質が、非相同末端結合(NHEJ)と呼ばれる主要な修復経路がどのように末端を効率的かつ誤りを最小にして引き合わせるかを決める仕組みを探ります。
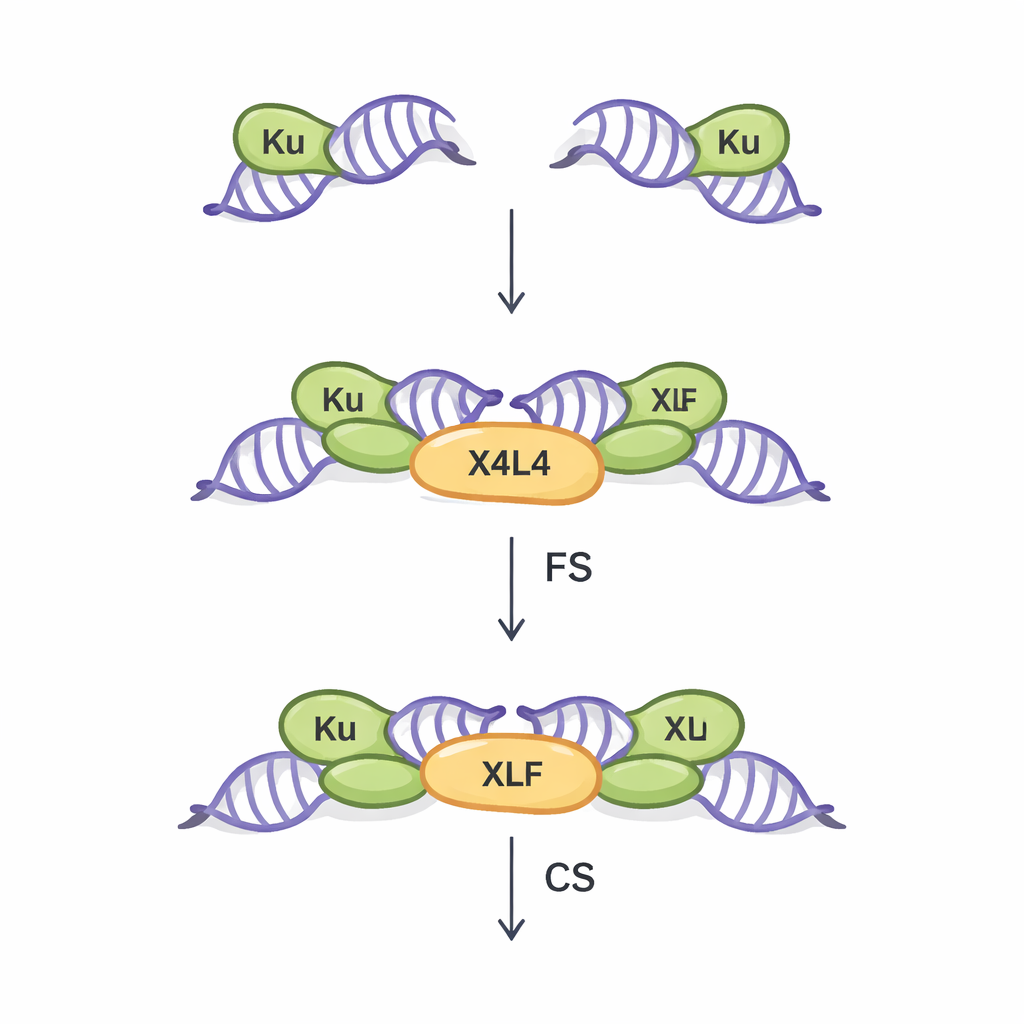
切断されたDNAをつなぐ二つの方法
NHEJは多くの体細胞における二本鎖切断の主要な修復ルートです。相同な鋳型を必要とせずに働くため、迅速ですがやや誤りが入りやすい特徴があります。この経路の最初の重要な段階はシナプシスと呼ばれ、物理的に二つの切断末端を架橋して後に接合できるようにすることです。これまでの研究(主に理想化されたブランク末端を用いたもの)は、二種類のシナプス状態を明らかにしました。『可動性シナプス(flexible synaptic、FS)』状態では末端が互いに近い位置に保持され、接合の手がかりを探りながら動くことができます。一方『密接シナプス(close synaptic、CS)』状態では末端が端対端に整列し、リガーゼによる封鎖の準備が整っています。Ku、XRCC4–Ligase IV(合わせてX4L4と表記)、およびXLFの三つの主要タンパク質がこの過程を協調することは知られていましたが、実際の不均一な末端がどのようにしてどのシナプス状態を選ばせるかは十分に理解されていませんでした。
末端の形状と短い相同性が修復経路を導く
研究者たちは単一分子FRETという、ナノメートルスケールの距離を追跡する蛍光ベースの手法を用いて、NHEJタンパク質によって個々のDNA分子がどのように引き寄せられるかを観察しました。彼らは単純なブランク末端と、短いオーバーハング—相互に相補的に対合し得る一塩基鎖の尾部—を持つより現実的な末端とを比較しました。オーバーハングが相補的であれば、わずか数塩基でも密接シナプス複合体が形成される確率が劇的に高まることがわかりました。実際、切断部での3塩基の“マイクロホモロジー”があれば、XLFを必要とせずともKuとX4L4だけで安定したCS複合体を作り出せました。これはDNA自体が補助タンパク質が通常与える一部のエネルギーや指針を供給できることを示しています。
小さなDNAフラップが橋を安定化する仕組み
異なるFRETシグネチャーを解析することで、オーバーハング末端に対する密接シナプス状態には少なくとも二つの構造的バリエーションがあることが明らかになりました。一つはオーバーハングの最先端が互いに対合してニックやギャップのある接合を作る形です。もう一つは、二本鎖DNAと一本鎖オーバーハングの接合部が一直線に押し付けられ、オーバーハングが小さなフラップのように外側に反転する形です。これらのフラップは依然として塩基対を作ることを可能にし、末端を非常に近接させたままにするため複合体を安定化し、最終的な封鎖前に酵素が切り詰めたり伸長したりする余地を与えます。興味深いことに、オーバーハングに生じる一般的な酸化損傷(例えば8-オキソグアニン)はこの過程に与える影響が控えめであり、NHEJが特定の損傷形態に対して堅牢であることを浮き彫りにします。
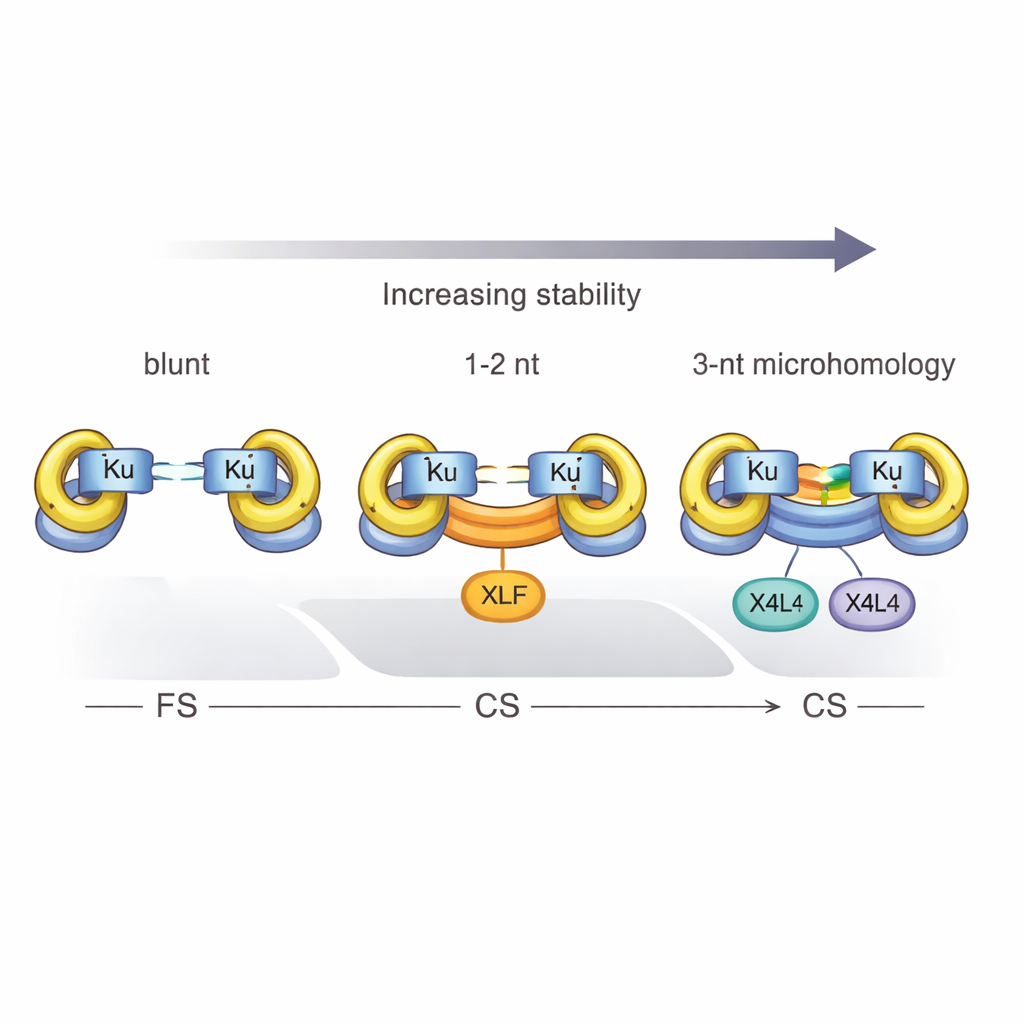
タンパク質、リン酸、そして“3”の力
本研究はまた明確な閾値を定義しました:KuとX4L4が可動性のある複合体を確実に密接なものへと変換するには、少なくとも3つの相補的塩基対が必要です。1つあるいは2つだけの一致では、XLFが参加して末端をクランプする手助けをしない限り、系は主に可動性状態で停滞します。化学的な詳細も重要です。切断されたDNAが5′リン酸基を持つ(多くの生理的切断で見られる普通の特徴)場合、シナプシスはより効率的になり、密接複合体が真にリガーションされる可能性が高くなり、一時的な架橋が恒久的な修復に変わりやすくなります。しかし、このリン酸による促進効果は、切断部での塩基対による安定化効果を完全に代替することはできません。
これが健康とゲノム編集に意味すること
平易に言えば、本研究は切断されたDNA末端が修復を待つ受動的な存在ではないことを示しています。その正確な形状、わずかな一致配列、化学的タグが、修復タンパク質がどのように末端を掴み、整列させ、再接続するかを能動的に導きます。3塩基以上の一致がある場合、DNA末端自体が損傷を修復準備完了の構成に固定する手助けをし、時には特定の補助タンパク質を不要にします。一方でこうした一致が乏しい場合は、追加のタンパク質因子が不可欠になります。これらの知見は、なぜある切断がきれいに修復され、他は小さな変異や再配列を引き起こすのかを説明する助けとなります。また、CRISPRのように意図的に作られた切断が同じNHEJ機構で修復されるゲノム編集ツールの改善にも示唆を与えます。切断末端を調整することで、科学者たちはゲノムがどのように書き換えられるかをよりよく制御できる可能性があります。
引用: Zhang, C., Jin, W., Jiang, Y. et al. DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging. Nat Commun 17, 1720 (2026). https://doi.org/10.1038/s41467-026-68417-0
キーワード: 二本鎖DNA切断修復, 非相同末端結合(NHEJ), DNAシナプシス, マイクロホモロジー, ゲノム安定性