Clear Sky Science · ja
バリンからロイシンへの単一スイッチがPlasmodium falciparum AP2-GのDNA結合を破壊し、ap2-g活性化におけるGDV1の役割を明らかにする
マラリア寄生虫が直面する生死を左右する重要な選択
血中に生息するマラリア寄生虫は常に重大な選択を迫られています:一人の宿主内で増殖を続けるか、または蚊刺しによって次の宿主へ移ることのできる形態へ切り替わるか。本研究は、寄生虫のあるタンパク質におけるごく小さな変化が、その感染性で蚊に伝播可能な段階を完全に遮断しうることを明らかにし、マラリア伝播を阻止するための新しい手掛かりを示します。
寄生虫の分かれ道
血流中では、Plasmodium falciparumは主に急速な増殖に注力し、それが病気の原因になります。しかしごく一部は配偶子体と呼ばれる性的形態に変換し、これが蚊によって取り込まれ次の宿主へ伝播され得る唯一の段階です。なぜ群れの中でごく一部だけがこの切り替えを行うのかは長年の謎でした。以前の研究で、GDV1とAP2-Gと呼ばれるDNA結合タンパク質の二つがこの決定の中心にいることが示されました。GDV1は通常サイレントなap2-g遺伝子の活性化を助け、AP2-Gは次に性的発達を駆動する一連の遺伝子をオンにします。本研究は別のキナーゼであるSTK2を調べることを目的としていましたが、代わりにAP2-G自身に関するはるかに劇的な発見に行き当たりました。
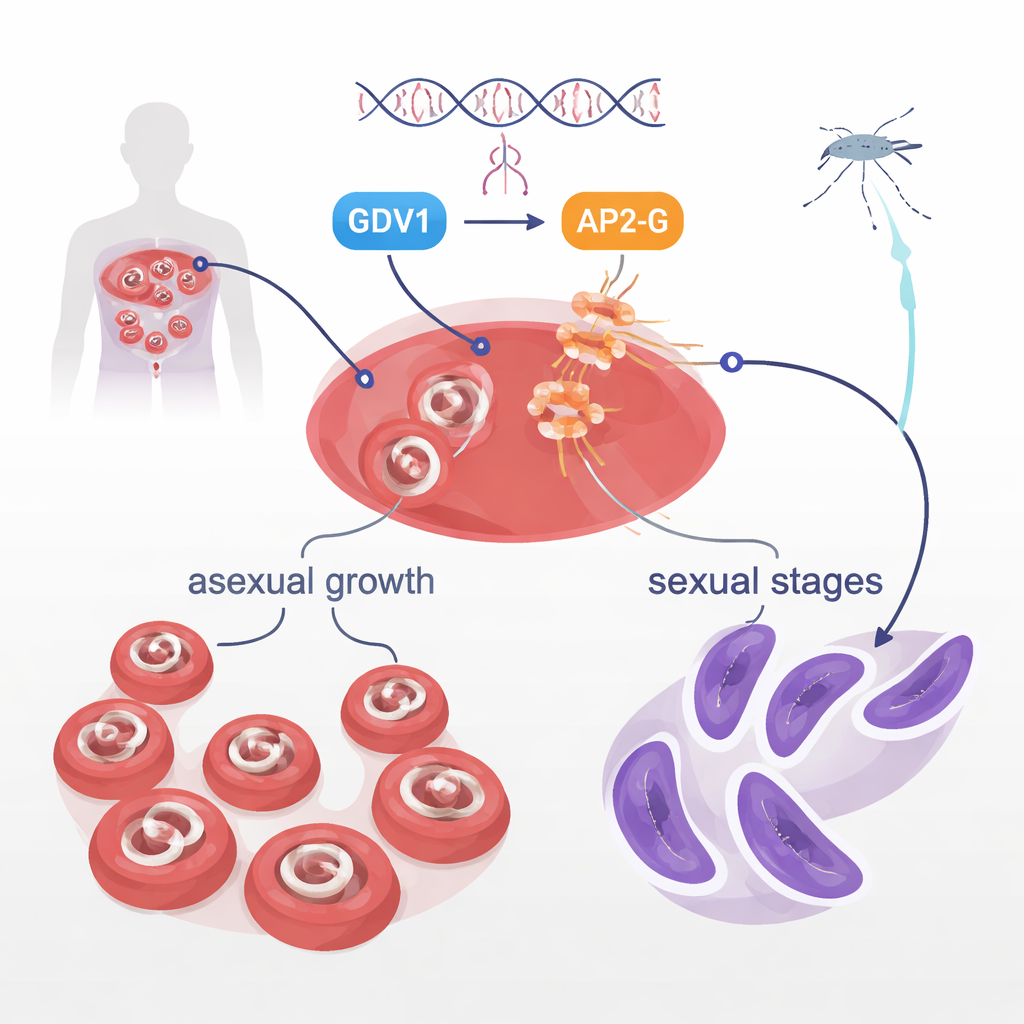
伝播を止める単一のアミノ酸
研究者たちはある実験室株でstk2遺伝子を欠損させたとき、これらの寄生虫が配偶子体をまったく作れなくなったことに気付きましたが、無性増殖は問題なく続きました。驚いたことに、別の株で同様の操作を行うと配偶子体は正常に形成されました。全ゲノム配列解析により隠れた原因が明らかになりました:ap2-g遺伝子の一塩基の変化で、2163番目の位置のアミノ酸がバリンから非常に類似したロイシンへ置換されていたのです。この位置はAP2-GのDNA結合領域のちょうど先頭にあり、特定のDNAモチーフを物理的に掴んで遺伝子をオンにする部分に当たります。このごく小さなバリン→ロイシンの切り替えだけで配偶子体形成が消失しました。研究者が正常な寄生虫にこの変異を導入すると配偶子体は消え、逆にバリンに戻すと性的発達は完全に回復しました。
スイッチが分子の鍵を壊す仕組み
この微妙な変化がなぜこれほど致命的なのかを理解するために、チームはコンピュータモデルと実験を組み合わせました。構造予測は、バリンをロイシンに置き換えることでAP2のDNA結合ドメインの精密な形状がずれ、不安定になることを示唆しました。精製タンパク質を用いた試験管内アッセイでは、正常なAP2-Gは「GnGTAC」を含む好ましいDNA配列に強く結合しましたが、2163位にロイシンを持つ変異型AP2-Gはこの配列にまったく結合できませんでした。安定したDNA結合が失われると、AP2-Gは自身の遺伝子をオンにする(自己増幅ループとして知られる自己制御)ことも、寄生虫を性的経路へ押し進めるために必要な数十の下流遺伝子を活性化することもできませんでした。機能的には、変異体寄生虫は「不妊」になり、赤血球中では繁栄するものの蚊に感染させる形態を作ることができなくなりました。
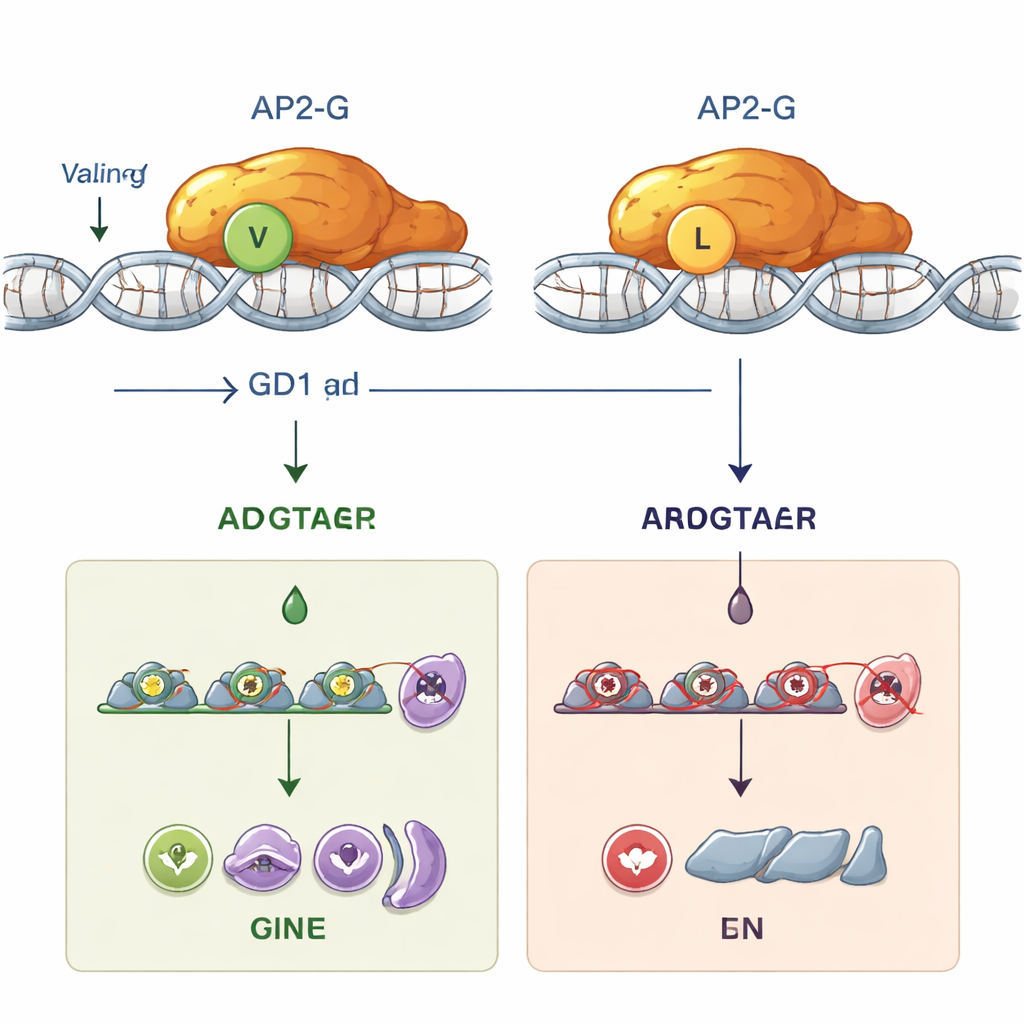
AP2-Gが主導する前のGDV1の隠れた役割
この変異は研究者にとって独自のツールも提供しました:ap2-g遺伝子はオンにできるがAP2-GはDNAに結合できない寄生虫です。蛍光や発光リポーターを用いて、赤血球内での寄生虫の48時間のサイクル中にそれぞれの因子がいつ働くかを追跡しました。GDV1タンパク質はまず schizogony(分裂増殖期)と呼ばれる初期段階で現れ、サイレント状態にあるap2-gの発現を立ち上げるために不可欠であることが分かりました。この初期活性化は、ap2-gが正常なAP2-Gをコードしているか変異型であるかにかかわらず起きました。のみならず、十分な量の正常なAP2-Gが蓄積して初めて強い自己増幅ループと他の「性的」遺伝子の活性化が起こりました。MSRP1という重要なマーカータンパク質は機能的なAP2-Gを持つ寄生虫でのみ発現し、早期と後期の性的決定寄生虫を区別する便利な指標となりました。ロイシンへの切り替えを持つ変異株では、GDV1はap2-gを目覚めさせることができたものの、壊れたAP2-Gはその後のプロセスを進められず、性的発達は停滞しました。
マラリア拡散を食い止めるための示唆
一般読者への結論は単純です:マラリア寄生虫は伝播可能かどうかを決める極めて敏感な分子の鍵に依存している。本研究は、その鍵の「歯」を一つ変えるだけ――AP2-GのDNAを掴む領域にある単一のバリン――で寄生虫が蚊に感染させる段階を作れなくなることを示しました。同時に、別のタンパク質GDV1が最初にサイレントなap2-gを解錠する鍵として働き、AP2-Gが自らの産生を強化してより広い性的プログラムを起動する以前に作用することを明確にしました。これらの一連のイベントをマッピングし、各段階で光るリポーター株を作成することで、性的コミットメントを妨げる薬剤やヒト由来の因子をスクリーニングする強力なツールが提供されます。長期的には、AP2-GのDNA結合領域やGDV1駆動の活性化ステップを標的にすることが、単一の患者のマラリアを治療するだけでなく、伝播の連鎖を断つ新たな戦略の基礎となり得ます。
引用: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
キーワード: マラリア伝播, Plasmodium falciparum, 配偶子体発生, AP2-G, GDV1