Clear Sky Science · ja
TMEM110はTRPML1の立体構造を制御してエンドリソソームの恒常性を維持し、ミトコンドリアDNAの漏出と病的な自己DNA処理を防ぐ
外傷後に流出するDNAが問題となる理由
頭部への強い打撃など重度の外傷を受けると、損傷は局所にとどまりません。多くの患者は肺、肝臓、腎臓などの臓器機能が失われる危険な全身反応を発症します。本研究は、細胞内の小さな構造体—リソソーム、ミトコンドリア、免疫センサー—が互いに情報をやりとりして、身体が静かに破片を片付けるか、自己に向かう免疫攻撃へと暴走するかを決めている仕組みを明らかにします。この見えない清掃システムの理解は、外傷後の臓器不全を防ぐ新しい方法や自己免疫・炎症性疾患の治療法につながる可能性があります。
頭部外傷から全身危機へ
外傷性脳損傷(TBI)は多臓器不全症候群(MODS)と呼ばれる強力な炎症嵐を引き起こすことがありますが、脳の損傷がどのように遠隔臓器へ波及するかは不明な点が多いです。著者らは血液や組織を巡回し、プロの清掃係として働く単球およびマクロファージに注目しました。TBI後には細胞が制御不能に死滅し、自己のDNAを持つ独立した小さな発電所であるミトコンドリアが丸ごと循環に放出されます。このミトコンドリアDNA(mtDNA)は免疫系にとって細菌DNAに似ており、迅速に除去されないと強い抗ウイルス様防御を誘導します。通常、細胞はこれらの余剰ミトコンドリアをリソソームと呼ばれる酸性コンパートメントへ取り込み、酵素がDNAを分解して細胞質へ漏れるのを防ぎます。 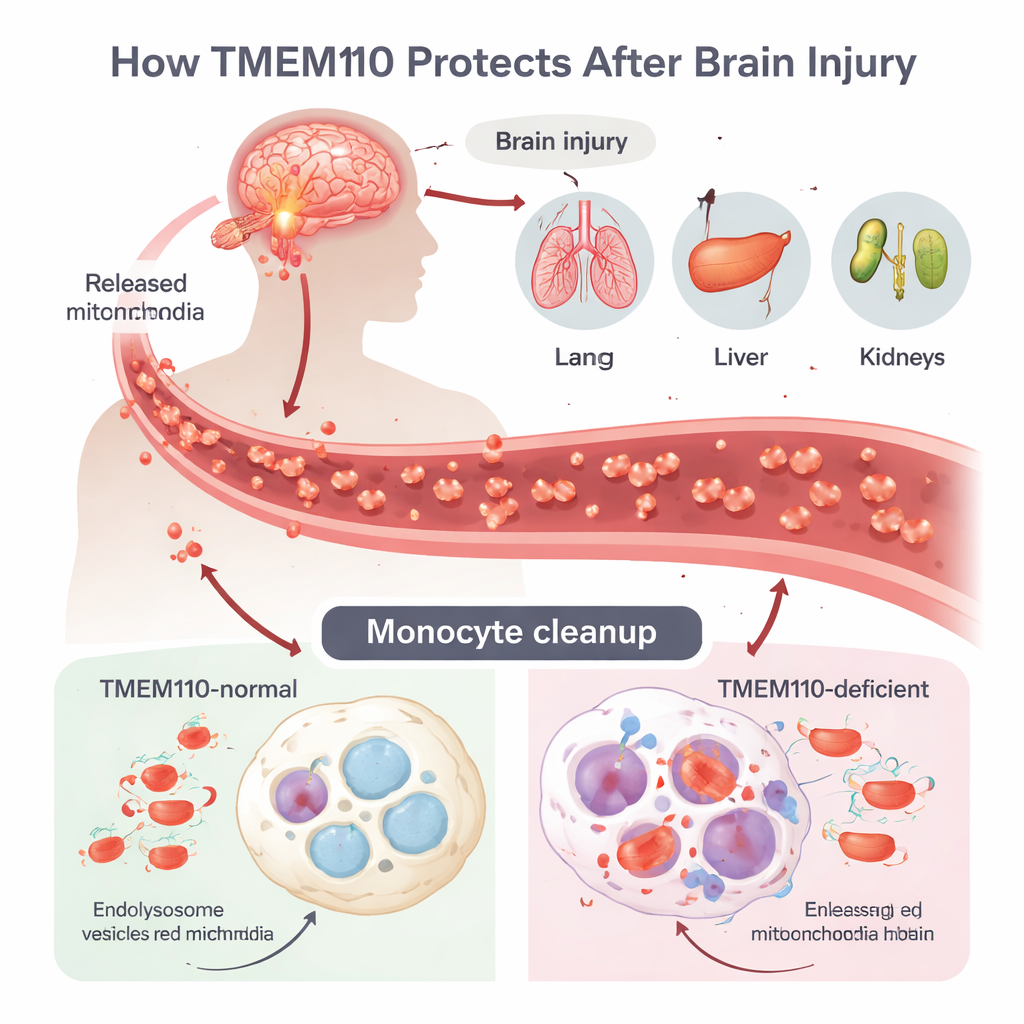
リソソームを安定化する門番タンパク質
研究チームは内在性膜ネットワークである小胞体の膜を貫通するタンパク質TMEM110を、この過程の重要な門番として同定しました。単球・マクロファージでのみTMEM110を欠損させた遺伝子改変マウスを用いて制御された脳損傷モデルを作成したところ、正常マウスと比べTMEM110欠損マウスは血液および脳脊髄液中のタイプIインターフェロン(強力な抗ウイルスシグナル分子)レベルが著しく高くなりました。これらのマウスでは肺、肝臓、腎臓、リンパ節の損傷がより重度で、TBI後の長期生存率も大幅に低下しました。研究者らがタイプIインターフェロンの受容体を阻害するか、変異骨髄を正常な細胞で置換すると、臓器損傷と死亡率が低下し、末梢単球からの過剰なインターフェロンシグナルがこの状況でMODSを駆動する主要因であることが示されました。
イオン制御の破綻がDNA漏出を招くしくみ
これらの免疫細胞の内部を詳しく調べると、TMEM110欠損のリソソームは化学的に不均衡で、酸性度が低下しカルシウムが過剰に蓄積していました。この状態では通常リソソーム内でDNAを分解する酵素DNase IIの活性が失われ、リソソーム膜が脆弱になり、mtDNAが細胞質へ漏出しました。標識した供与ミトコンドリアを取り込むヒト単球の実験でも、TMEM110がないとより多くのmtDNAが細胞質に漏れ出し、インターフェロン刺激遺伝子が急増することが確認されました。本研究はTMEM110がリソソームのイオンチャネルTRPML1を制御することで働くことを示しています。TMEM110が存在するとTRPML1に物理的に接触して“開いた”立体構造へと移行させ、リソソーム表面に小さなカルシウム放出ホットスポットを作ります。これらの制御されたカルシウム流出は適切な酸性度の維持、膜修復の支援、そしてmtDNAを内部に留めて分解することを助けます。 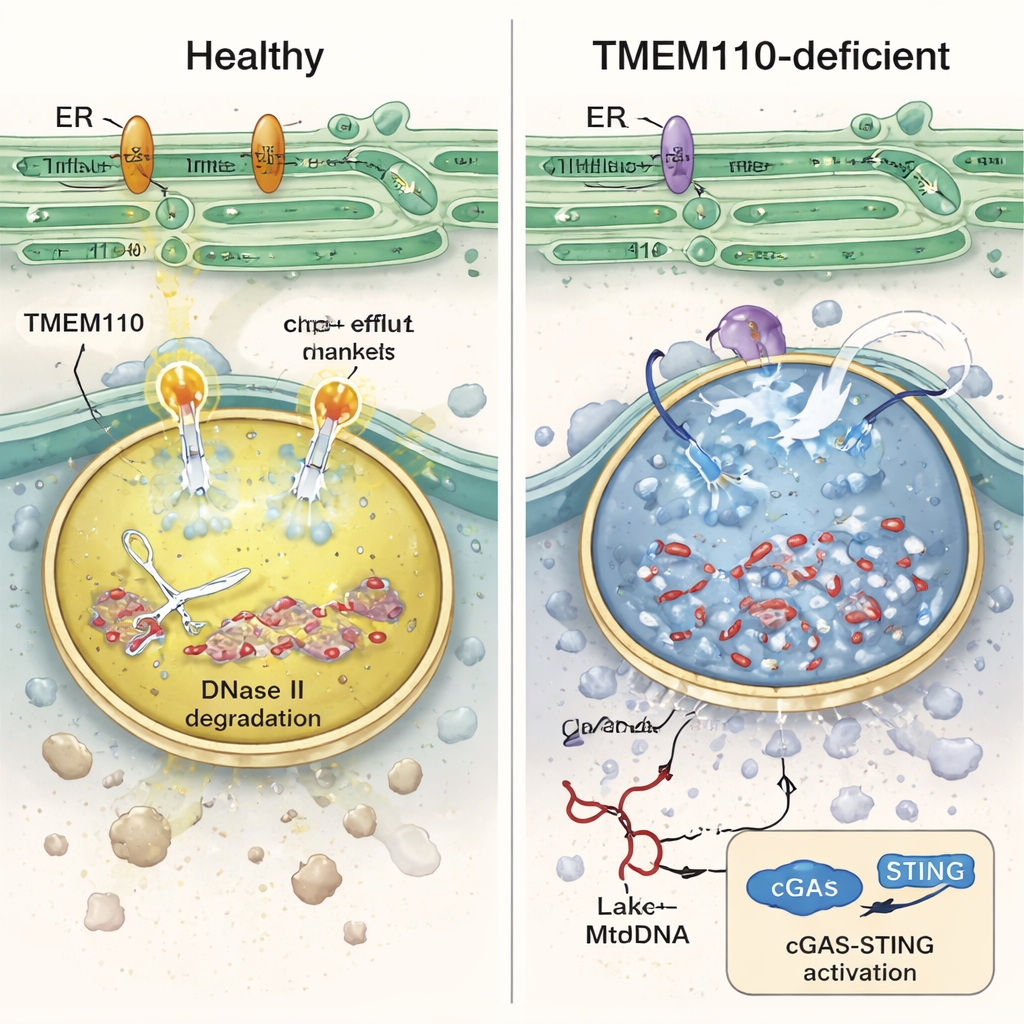
細胞のDNA警報システムとのフィードバックループ
一旦mtDNAが細胞質に漏れると、それは異所性DNAに対する主要な警報システムであるcGAS–STING経路によって認識されます。興味深いことに、TMEM110は安静時にSTINGにも結合して小胞体に隔離し、不必要な警報の発動を防いでいます。細胞質DNAが蓄積するとSTINGが活性化しTMEM110への結びつきを緩めます。これによりTMEM110の別の領域が露出してTRPML1と結びつき、リソソームからのカルシウム流出を増強してフィードバックループを形成します:自己DNAを感知するとDNA除去を強化する機構が活性化されるのです。ヒトの自己炎症症候群で見つかるSTINGの疾患関連変異はこの引き継ぎを阻害し、TMEM110を抑制状態に閉じ込めて慢性的なインターフェロン活性化に寄与します。こうしたSTING変異を持つマウスではTBI後に臓器損傷と死亡率が悪化しましたが、mRNA‑リポイドナノ粒子療法を用いてTMEM110の小片をリソソームへ届けるとmtDNAの制御が部分的に回復し生存率が改善しました。
患者からの手がかりと新治療への道筋
著者らは次に、外傷性脳損傷とMODSを有する143人の臨床コホートを調査しました。受傷後早期に単球のTMEM110レベルが高い患者は臓器機能の回復と生存がより高率でした。TMEM110が低い患者は循環性のmtDNAや細胞を失ったミトコンドリアが多く、インターフェロン応答が強く、臓器不全スコアが高く、DNAや核タンパク質に対する抗体を含むより広範な自己抗体プロファイルを示しました。これらのパターンはマウスでの所見とよく一致しており、TMEM110によるリソソーム安定性とmtDNA処理の制御がヒト疾患に共通するメカニズムであることを支持します。
重篤な外傷患者にとっての意味
平易に言えば、この研究は重大な外傷後に私たちの免疫系が繊細な選択を迫られることを示唆します:死にゆく細胞から放出された自己DNAの洪水を静かに消化するか、それをウイルス侵入とみなして自己臓器を損なう全面的な攻撃を開始するか。TMEM110はリソソームのイオンチャネルを調整しDNAセンサーSTINGと協調することで、細胞がより安全な道を選ぶのを助けます。このシステムが崩れると—TMEM110が欠如する、STINGが変異する、またはリソソームが圧倒されると—mtDNAが漏出して警報が鳴り続け、多臓器障害につながります。リソソーム指向のmRNA療法などでTMEM110–TRPML1–STING軸を標的にすることは、重度外傷後の臓器不全や自己免疫様合併症を予防・治療する新たな手段を提供する可能性があります。
引用: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
キーワード: 外傷性脳損傷, ミトコンドリアDNA, リソソーム, タイプIインターフェロン, cGAS‑STING経路