Clear Sky Science · ja
ヒトCOP1–DET1ユビキチンリガーゼ複合体のクライオ電子顕微鏡構造
細胞がどのタンパク質を破棄するかを決める仕組み
すべての細胞内では、何千ものタンパク質が適切なタイミングで常に合成、改変、あるいは分解され続けています。本論文は、がんや発生に関わる強力な遺伝子調節因子の除去を決める「品質管理」機構の一つ、分子シュレッダーともいえる装置を扱います。著者らはその三次元構造をほぼ原子レベルで明らかにし、この装置が不活性な積層状態と基質を処理する能動的な形態の間でどのように切り替わるかを示しています。この知見は将来的に、装置の活性を高めたり抑えたりする薬剤設計に役立つ可能性があります。
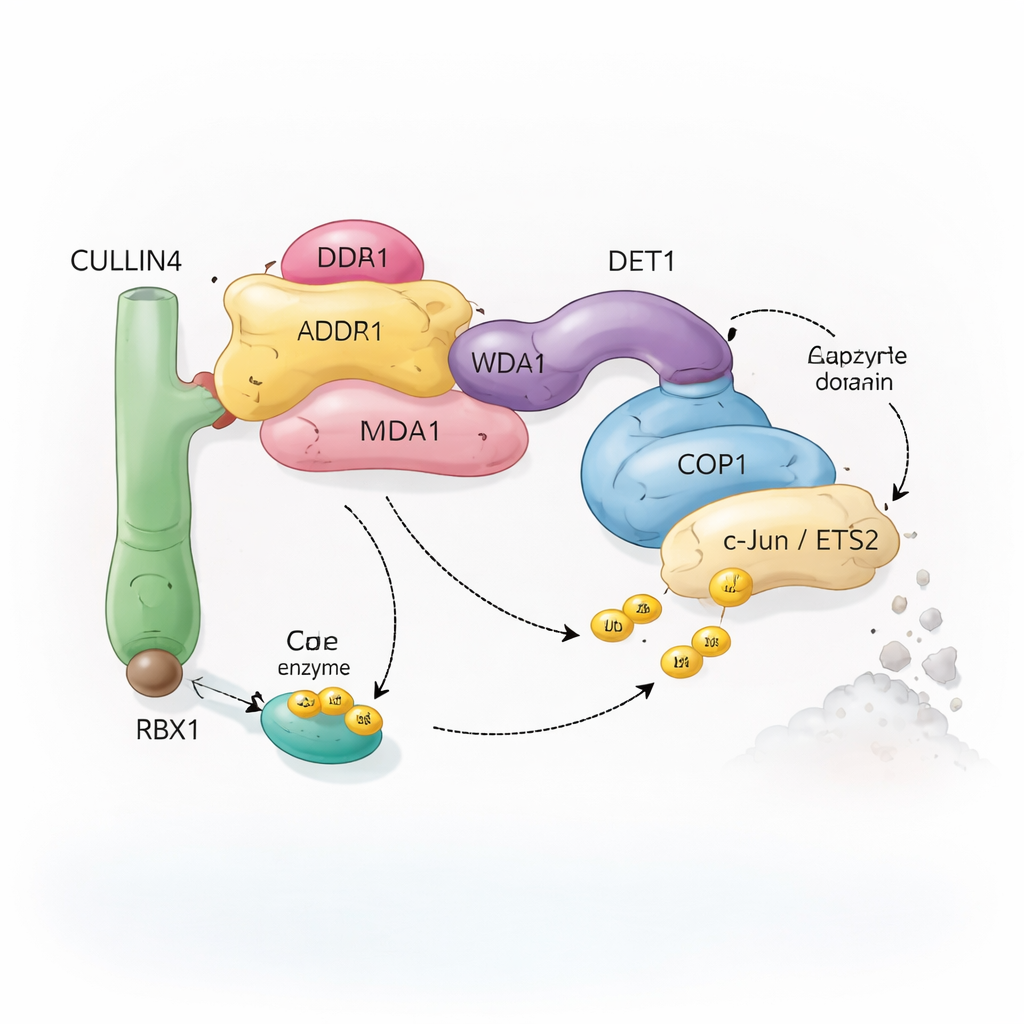
多くの部品からなる分子リサイクル班
細胞はユビキチン化と呼ばれる仕組みに依存してタンパク質をリサイクルの標的にします。小さなユビキチン分子は着脱可能な旗のように働き、タンパク質が改変されるべきか、移動されるべきか、あるいは破壊されるべきかを示します。これらの旗を特定標的に付加するのがユビキチンリガーゼと呼ばれる特別な酵素複合体です。本研究で中心となる複合体はCOP1を核とし、植物からヒトまで見られるタンパク質で、遺伝子のオン/オフを制御する転写因子を標的づけるのに関与します。COP1は単独では働かず、CULLIN4という足場タンパク質を中心にDDB1、DDA1、DET1といったアダプターが組み合わさってより大きなアセンブリを形成します。これらは協働して柔軟な「リサイクル班」を作り上げ、c‑JunやETS2など、細胞増殖やがんに関与する特定の転写因子を認識します。
複合体を3Dでとらえる
この班がどのように機能するかを理解するため、研究者らは単粒子クライオ電子顕微鏡という手法を用い、急速凍結したタンパク質を撮像して高解像度で形状を再構築しました。ヒトCOP1–DET1系を培養細胞で再構築し、複合体を精製していくつかの異なる構造状態を可視化しました。まず中心ハブとして機能するDDB1–DDA1–DET1モジュールの構造を解明しました。DET1は剛直な円盤状ではなく、部分的に柔軟な異常な形をとり、突出した“クロー”がパートナー酵素をつかむことができます。次にCOP1とE2として知られる補助酵素群を加えることで、すべての要素がどのように組み合わさるかを示すより大きなアセンブリをとらえ、緻密な積層構造とより開いた二量体(COP1が2つ並ぶ)配置の両方を明らかにしました。
不活性な積層と能動的な二量体
もっとも注目すべき発見の一つは、複合体が繰り返し層をなす積み重なったフィラメント状構造を形成することです。各層では、8つのCOP1分子がコイルドコイル領域を介して絡み合い、菱形のリングを作ります。基質認識領域であるWD40ドメインはすべて同一方向を向き、隣接する層によって部分的に遮蔽されています。この密な詰まりは標的タンパク質のアクセスが制限される「オフ」状態を表している可能性が高いです。一方、研究チームがc‑JunやETS2といったCOP1基質と共発現させた複合体を観察すると、異なる二量体形態が見られました:2つのCOP1分子が並び、WD40ドメインが外向きに配され、多くの転写因子に見られる短い“VP”モチーフを結合できる状態です。生化学的検証により、長いユビキチン鎖をc‑Junに効率よく構築できるのはこの二量体状態のみであることが確認されました。
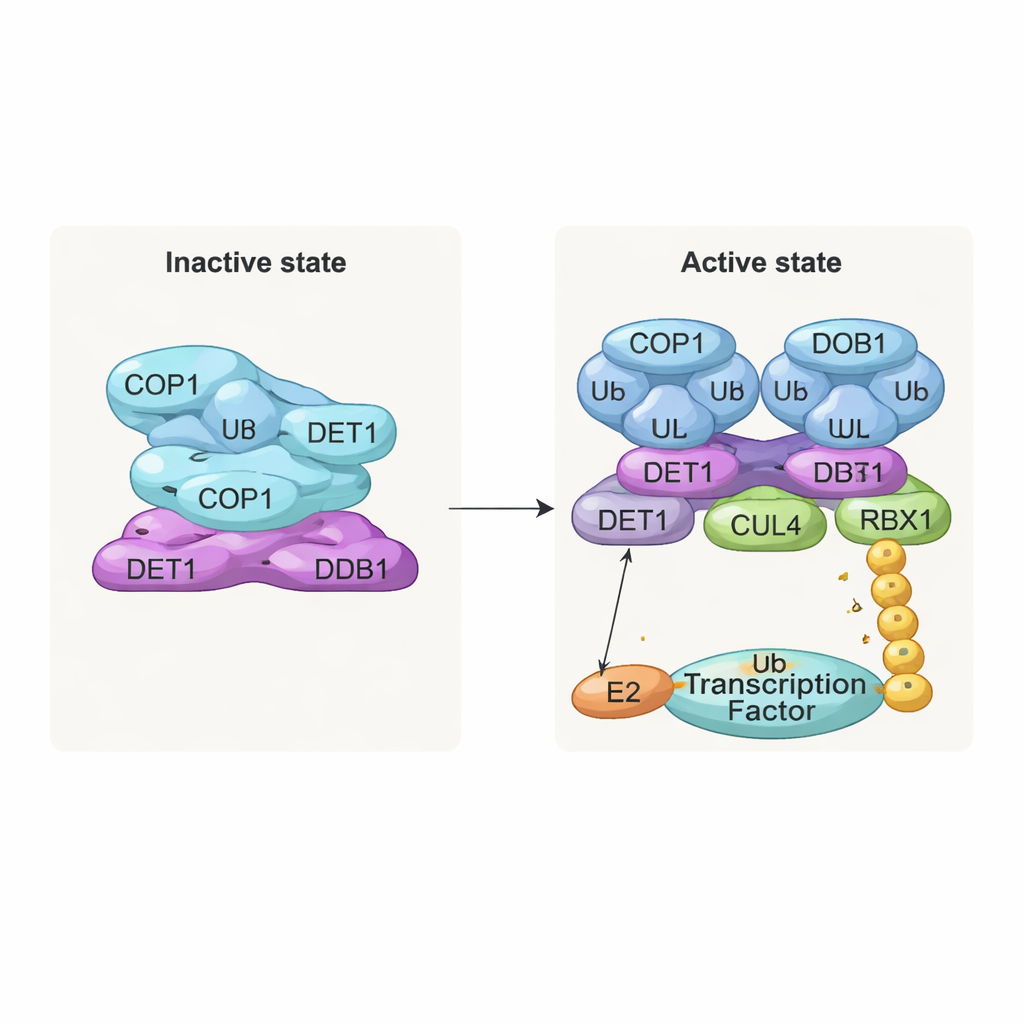
柔軟な橋渡し役であり交通整理役としてのDET1
DET1は装置のすべての部品をつなぐ主要なオーガナイザーとして浮かび上がります。そのN末端領域はDDB1に入り込み、複合体をCULLIN4の足場に固定します。一方、クロー領域はUbe2eと呼ばれるE2酵素ファミリーを取り巻きます。詳細な変異解析により、DET1がE2を直接把握しているのはCOP1ではなくDET1であること、そしてそれがCOP1の触媒領域であるRING近傍にE2を配置していることが示されました。この配置では、Ube2eが基質に最初のユビキチンタグを付ける手助けを行っているように見えます。続いて二つ目のE2酵素であるUbe2d3がCULLIN4–RBX1アームを介して動員され、これらのタグをより長い鎖へと伸長し、完全な分解のシグナルを形成します。言い換えれば、DET1は柔軟な橋として一つのE2をCOP1に提示し、より大きな足場が二つ目のE2を呼び込んで仕事を終わらせる役割を担います。
この研究が健康と疾患にとって重要な理由
これらの構造状態とその活性を写し出すことで、同じタンパク質群がアイドル状態の積層形態と転写因子を標的とする能動的二量体とをどのように切り替えるかが説明されます。このスイッチは、細胞分裂を駆動し、制御を失うとがんと強く結びつく因子であるc‑Junのような因子にとって特に重要です。DET1のクローがどのように特定のE2を選ぶか、COP1のWD40表面がVP含有基質をどのように認識するか、能動的な二量体がどのように形成されるかを理解することは、今後の研究のための設計図を提供します。長期的には、不活性な積層を安定化させる薬や能動的二量体を優先する薬は、がんやタンパク質分解が乱れるその他の疾患において遺伝子制御経路を調整する新たな手段を研究者に提供する可能性があります。
引用: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
キーワード: ユビキチンリガーゼ, COP1, タンパク質分解, クライオ電子顕微鏡構造, c‑Jun