Clear Sky Science · ja
エンジニアリングされたVPg saRNAは、生体内でキャップ非依存かつ低免疫原性で治療タンパク質を正確にコードする
RNA医薬のルールを書き換える
メッセンジャーRNA(mRNA)を基盤とするワクチンはCOVID-19との闘いの流れを変えましたが、同様の分子を慢性疾患で欠損したタンパク質の置換や補充に用いるのははるかに難しいです。体は異物のRNAを速やかに分解し強い免疫反応を起こす傾向があり、既存の多くの自己増幅型RNA設計は複製時にエラーを生じます。本研究は、人ノロウイルスの要素をもとに設計された新しいタイプの自己増幅型RNAを記述します。これは長持ちしやすく、炎症誘発性が低く、特に高い正確性を備えており、より精密で持続的なRNA医薬の可能性を開きます。
より賢い自己複製RNA
従来のmRNA医薬はタンパク質の1つの「レシピ」を運び、細胞に一度読み取られた後に分解されます。自己増幅型RNA(saRNA)は、細胞内で自身を複製する余分なウイルス由来の装置を含み、少量の投与から大幅な産生増加を可能にします。最も研究の進んだsaRNAシステムはアルファウイルス由来ですが、これらは大きく抗ウイルス防御を強く誘導し、配列を比較的低精度で複製します。著者らは代わりに、胃腸炎の一般的原因である人ノロウイルスに目を向けました。彼らはノロウイルスのコンパクトな遺伝領域を単離し、それを治療遺伝子の運搬体として再構築しました。その中心にはVPgという小さなウイルスタンパク質があり、RNAの先端に化学的に結合しています。VPgはヒトmRNAに通常ある「キャップ」構造に代わるもので、特定のストレス信号に対してより鈍感な別の翻訳因子群を使ってRNAが翻訳されることを可能にします。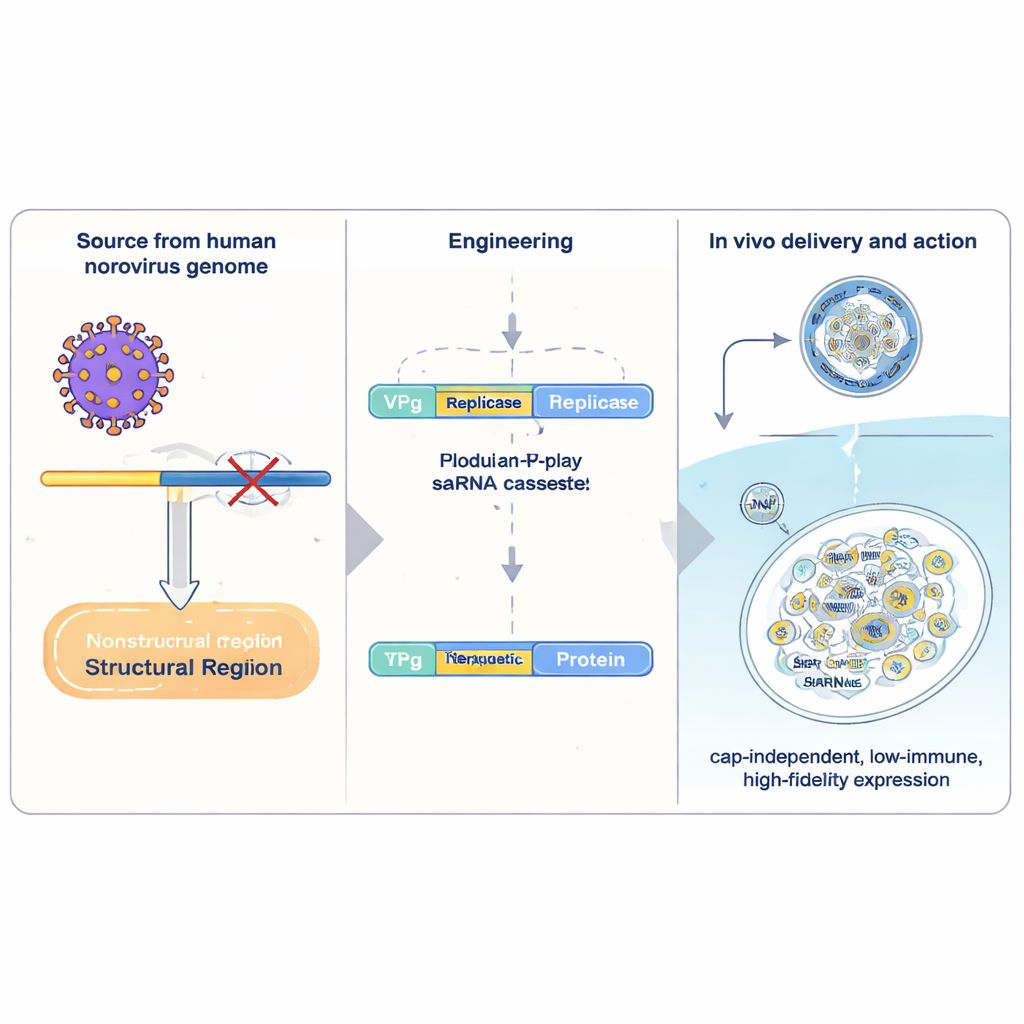
免疫を刺激せずに高い正確性を実現
タンパク質治療では正確性が重要です。わずかなコピーの誤りでも薬の挙動を変えたり、有毒な副産物を生じたりします。チームは、ノロウイルスのVPgがウイルスのRNA複製酵素(ポリメラーゼ)に結合すると、誤ったヌクレオチドが組み込まれる速度が遅くなり、エラー率が大幅に低下することを示しました。彼らはVPgの特定のアミノ酸がポリメラーゼの重要な制御領域に接触していることを特定し、この界面を乱すと複製の正確性が落ちることを実証しました。一方で、従来のsaRNA設計は二本鎖RNAを大量に生み出し、これは分子レベルの警報として抗ウイルス防御を活性化しタンパク質生産を停止させます。著者らはポリメラーゼを特定のVPg結合開始形に有利に働くよう再設計し、ゲノム配列を並べ替えて治療鎖のみが効率的に産生されるようにすることで、二本鎖RNAの形成を大幅に減らしました。さらに、RNAの末端領域を調整してVPgが正しい部位に付くようにし、意図しない短い断片が余計なペプチドに翻訳されるのを防ぎました。
標準的mRNAが失敗する場所で働く
新しいVPgベースのsaRNAは、通常のキャップ付きmRNAが効果を発揮しにくい厳しい病態で試験されました。がんに伴う悪液質—筋肉や脂肪が失われる消耗症—では、標準mRNAのキャップを認識する主要な翻訳因子がオフになっており、キャップ依存的なmRNAは非効率になります。VPgは翻訳機構への代替の入り口を使うため、膵臓がんのマウスモデルにおいて食欲や代謝を司るホルモン、グレリンの産生を持続的に促しました。月1回の低用量注射は筋肉や脂肪の保持、摂食と代謝の改善、そして明らかな毒性や慢性的な免疫活性化の徴候なく生存時間のわずかな延長をもたらしました。
精密ながん攻撃と抑制された自己免疫
高精度な複製が本当に重要かを検証するため、研究者らはVPgベクターにGSDMDENGという複雑なオンコリティック構成体を搭載しました。これはがん細胞のミトコンドリアに穴を空け腫瘍特異的な免疫反応を刺激するよう設計されています。同じ構成体を従来のアルファウイルスsaRNAに載せると、複製を重ねるごとに変異が蓄積して選択的ながん細胞殺傷および免疫誘導機能が弱まってしまいました。対照的にVPgシステムは意図した配列を保持し、強力ながん細胞殺傷を生み出し、持続的なT細胞応答を誘導して膵臓がんモデルの進行を遅らせあるいは防ぎました。最後に、著者らは別の課題、骨髄移植後に免疫細胞が肺を攻撃する慢性移植片対宿主病にVPg saRNAを適用しました。活性化プロテインCをコードするVPg saRNAは有害な抗体形成を減らし、肺の線維化を防ぎ、マウスの呼吸機能を改善しましたが、同等のアルファウイルス由来構成体はより強い自然免疫を誘発し転帰を悪化させました。
将来のRNA薬にとっての意義
まとめると、本研究はコンパクトで「差し替え可能」なRNAプラットフォームを示しており、三つの望ましい特性を兼ね備えます:高い複製精度、免疫アラームを抑える設計、そして標準的なmRNA翻訳を制限するいくつかのボトルネックを回避すること。治療遺伝子は固定されたノロウイルス由来のバックボーンに単純に差し替えられるため、ホルモンから凝固調節因子、オンコリティック剤に至るまで多くの異なるタンパク質が同じシャーシ上で検証可能です。ヒトでの使用にはまだ多くの作業が残りますが、このVPg saRNAアプローチは、低用量で長持ちし、病変組織でも通常のmRNAメッセージが確実に読み取れないような環境下でも機能する、より安定したタンパク質補充に似たRNA医薬への道を示唆します。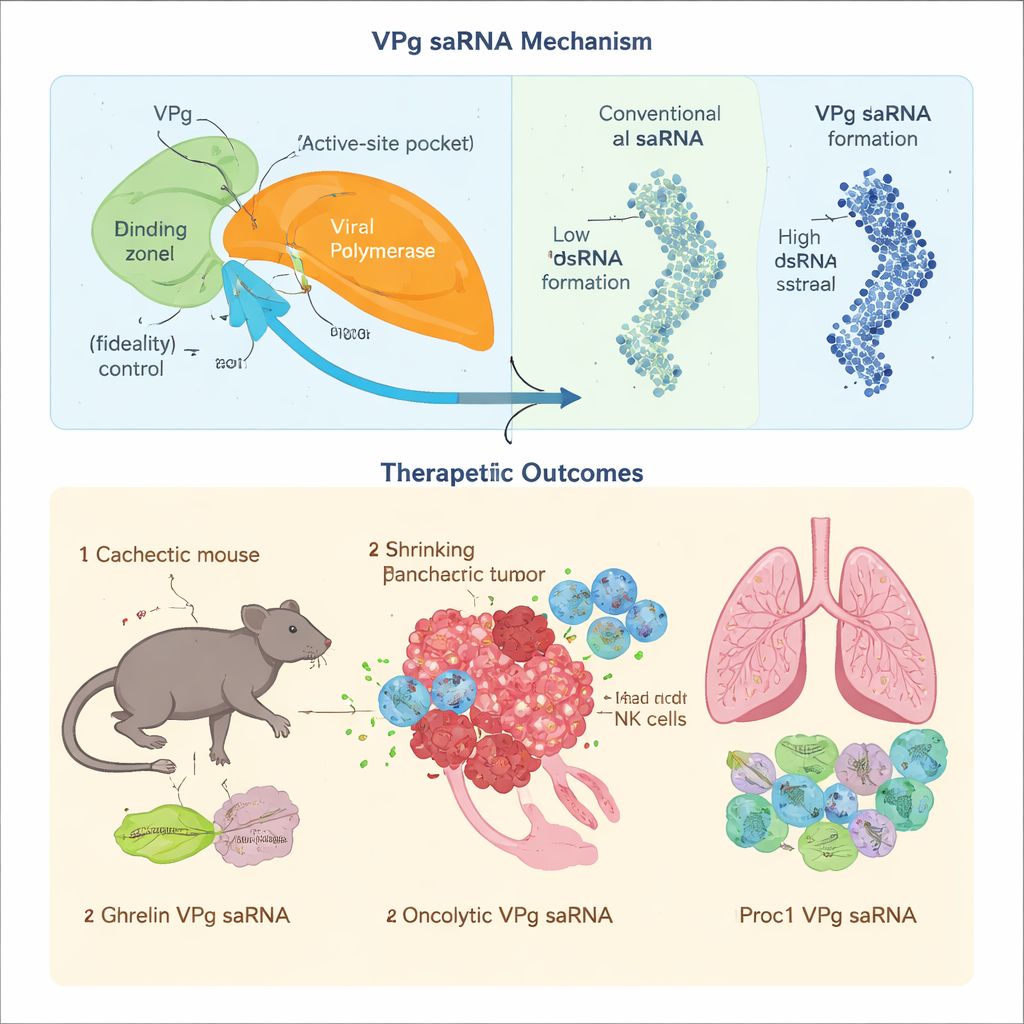
引用: Feng, Z., Chu, L., Li, Q. et al. Engineered VPg saRNA achieves cap-independent, low-immunogenic and precise encoding of therapeutic proteins in vivo. Nat Commun 17, 1666 (2026). https://doi.org/10.1038/s41467-026-68364-w
キーワード: 自己増幅型RNA, mRNA治療薬, ノロウイルスVPg, がん悪液質, 移植片対宿主病