Clear Sky Science · ja
RNA–RNA相互作用における低複雑性リピートの役割と二本鎖予測のためのディープラーニング枠組み
細胞の振る舞いを形作る「粘着性」のRNA配列
細胞内ではRNA分子が絶えず互いに衝突し、一時的な結合を作ってどの遺伝子がオンになるか、どのようにタンパク質が合成されるか、細胞がどう分化するかといった過程を制御しています。本研究は、多くのRNA–RNAの出会いが偶然ではなく、分子用のベルクロのように機能する短く単純で高頻度に繰り返される配列によって導かれていることを示します。研究者たちはさらに、こうしたRNA対が形成されやすい箇所を見分ける人工知能ツールを構築し、健康や疾患における細胞の仕組みを探る新たな道を開いています。
強力な影響を持つ単純なリピート
しばしばRNAはDNAからタンパク質へ情報を運ぶメッセンジャーとして語られますが、足場、制御因子、ガイドとしての役割も果たします。多くの活動は二本のRNA鎖の結合に依存しています。ヒトとマウス細胞の大規模な実験データを組み合わせることで、著者らは実際に結合に関与する領域が「低複雑性リピート」と呼ばれる配列に強く富んでいることを示します。これらは短いモチーフ(たとえばGやCの連続など)を何度も繰り返した配列です。ゲノムの“ジャンク”ではなく、これらの反復配列は多くのRNAが結びつく主要なドッキングサイトであり、トランスクリプトーム全体で密な相互作用ハブを形成します。
発生と制御のためのRNAハブ
研究チームがこれらのリピートに富む接触部位を持つ遺伝子を調べると、顕著なパターンが浮かび上がりました。それらの多くは転写因子のような発生や細胞アイデンティティを制御するタンパク質をコードしています。積極的に分化していないがん細胞株においても、発生プログラムに関連するRNAはリピートに基づく接触に深く関与していました。著者らはまた、タンパク質をコードしないがしばしば調節を担う長鎖非翻訳RNA(lncRNA)に着目しました。たとえばlncRNA TINCRや運動ニューロン形成に重要な別のlncRNA Lhx1osのターゲットは、ともに相補的リピートが過剰に存在していました。これらの場合、lncRNA上の単純なリピートが相手RNAの相補的リピートと一致し、安定した結合を可能にして重要な発生遺伝子の量や翻訳を調整する助けになります。
タンパク質や編集酵素の関与
こうしたリピート主導のRNA接触は単独で働くことはほとんどありません。著者らがタンパク質結合マップを相互作用データに重ねると、多くのリピートを含む接触部位が翻訳制御、RNA分解、Pボディやストレス顆粒などの細胞質顆粒の形成に関わるRNA結合タンパク質によっても認識されていることが分かりました。特にSTAU1というタンパク質はそのRNA標的の破壊を誘導し得るもので、低複雑性リピートを介して形成された二本鎖によく結合します。STAU1をノックダウンすると、特にリピートを含む二本鎖に関与するRNAのレベルが上昇し、リピート媒介のRNA対合が転写体を制御された分解の標的にできることが示唆されます。同じリピートに富む領域はADAR1のようなRNA編集酵素も引き寄せ、二本鎖RNA内の特定塩基を化学的に修飾することで、低複雑性リピートが編集サイトを配置してRNAのふるまいを微調整する手助けをしていることを示しています。
ニューラルネットワークにRNA接触を学ばせる
標準的なコンピュータプログラムは主に熱力学的安定性、すなわち二本鎖を形成または解くのに必要なエネルギーに基づいてRNA–RNA結合を予測します。便利ではありますが、これらのモデルは特に長いRNA間の細胞内で観察される実際の相互作用を見逃すことが多いです。単純なエネルギー規則を超えるために、著者らはRIMEと呼ばれるディープラーニングモデルを訓練しました。これは「言語モデル」型の埋め込みを使用し、塩基配列からパターンを学習した数値表現を用います。RIMEはRNA断片のペアを提示され、それらが相互作用するかどうかを分類することを学びます。陽性例にはpsoralenベースの架橋実験から得られた多数の実際の対を用い、陰性例には慎重に構築した非相互作用ペアを用いました。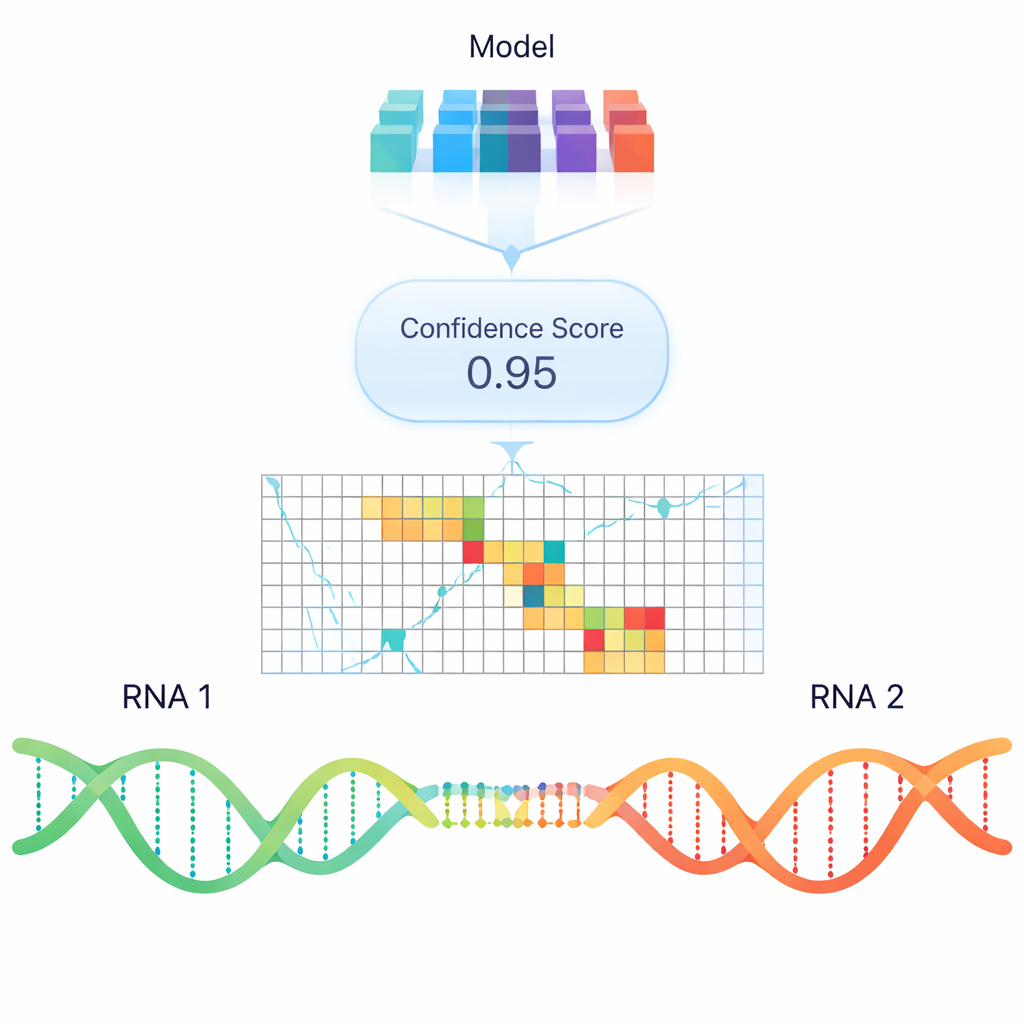
より賢い予測と新たな生物学的手がかり
主要な熱力学ベースのツールや別のニューラルネットワーク法と比較したベンチマークで、RIMEは真のRNA–RNA接触を偽のものから区別する点で一貫して優れており、特に高信頼度の実験的相互作用で性能が良好でした。RIMEは単に二つのRNAが対合するかどうかを予測するだけでなく、関与する正確な領域を特定する傾向があり、低複雑性リピートが接触の強力な予測因子であることを自然に学習します。驚くべきことに、異なるRNA間の相互作用だけで訓練された同じモデルは、単一のRNA分子内の内部塩基対形成の予測にも良く適用でき、構造実験や古典的な折りたたみアルゴリズムと整合します。TINCR、NORAD、SMaRTのような非コード性調節因子に対しては、RIMEは既知の機能的相互作用部位を再発見し、追加の候補領域も示唆します。
なぜこれが重要か
一般読者向けに要点を述べると、かつて無視されがちだった短く繰り返すRNA配列は、細胞のRNA配線図における中央の接続点として機能しているということです。これらはRNAを引き寄せ、調節タンパク質や編集酵素を招き、細胞の発生やストレス応答を制御する経路で多用されています。新しいRIMEモデルは、ゲノムを走査してこれらのRNA–RNAパートナーシップを見つけ出す強力な手段を研究者に提供し、リピート拡大に関連する神経疾患などで誤動作する可能性のある結合も対象にできます。本質的に、この研究は単純なRNAリピートがどのように結合するかを理解・予測することで、遺伝子制御の隠れた層を明らかにできることを示しています。
引用: Setti, A., Bini, G., Pellegrini, F. et al. The role of low-complexity repeats in RNA–RNA interactions and a deep learning framework for duplex prediction. Nat Commun 17, 1637 (2026). https://doi.org/10.1038/s41467-026-68356-w
キーワード: RNA–RNA相互作用, 低複雑性リピート, 長鎖非翻訳RNA, ディープラーニング, 遺伝子制御