Clear Sky Science · ja
中心扁桃体の単一核アトラスがヒトのアルコール使用障害におけるクロマチンと遺伝子転写の動態を明らかにする
この研究が日常生活にとって重要な理由
アルコール使用障害(AUD)は何百万もの人々とその家族に影響を及ぼしますが、長期にわたる過度の飲酒が個々の細胞レベルで人間の脳に具体的にどのような影響を与えるかについては、驚くほど不明な点が残っています。本研究は、恐怖やストレス、動機づけのハブである小さく重要な領域—中心扁桃体—に焦点を絞り、アルコールが脳細胞とそれらの遺伝子制御システムをどのように再編するかをマッピングします。最先端の「単一細胞」シーケンシングを依存症リスクの遺伝学的研究と組み合わせることで、なぜ一部の人がAUDに対してより脆弱なのか、そしてアルコールが脳に長期的な分子レベルの痕跡を残す仕組みの説明を始めます。
小さな脳の中枢を詳しく見る
中心扁桃体は感情やストレスのネットワークにおける主要な出力ステーションであり、不安軽減、渇望、強迫的な飲酒と強く結びついています。本研究では、50人の中心扁桃体から死後に採取した約17万5千の個々の細胞核を解析しました—うち22人はアルコール使用障害の既往があり、28人はAUDなしです。単一細胞で遺伝子活動(RNA)とクロマチンの可及性(DNAがどれだけ「開いている」か)を同時に読み取る技術を用い、この領域に存在する主要な脳細胞型の詳細なアトラスを構築しました。そこには複数の種類のニューロンや、アストロサイトやミクログリアといった支持細胞が含まれます。抑制性ニューロン(脳活動を抑えたり形作ったりする細胞)が中心扁桃体に特に豊富で、AUDのある人々で特に影響を受けているように見えることがわかりました。 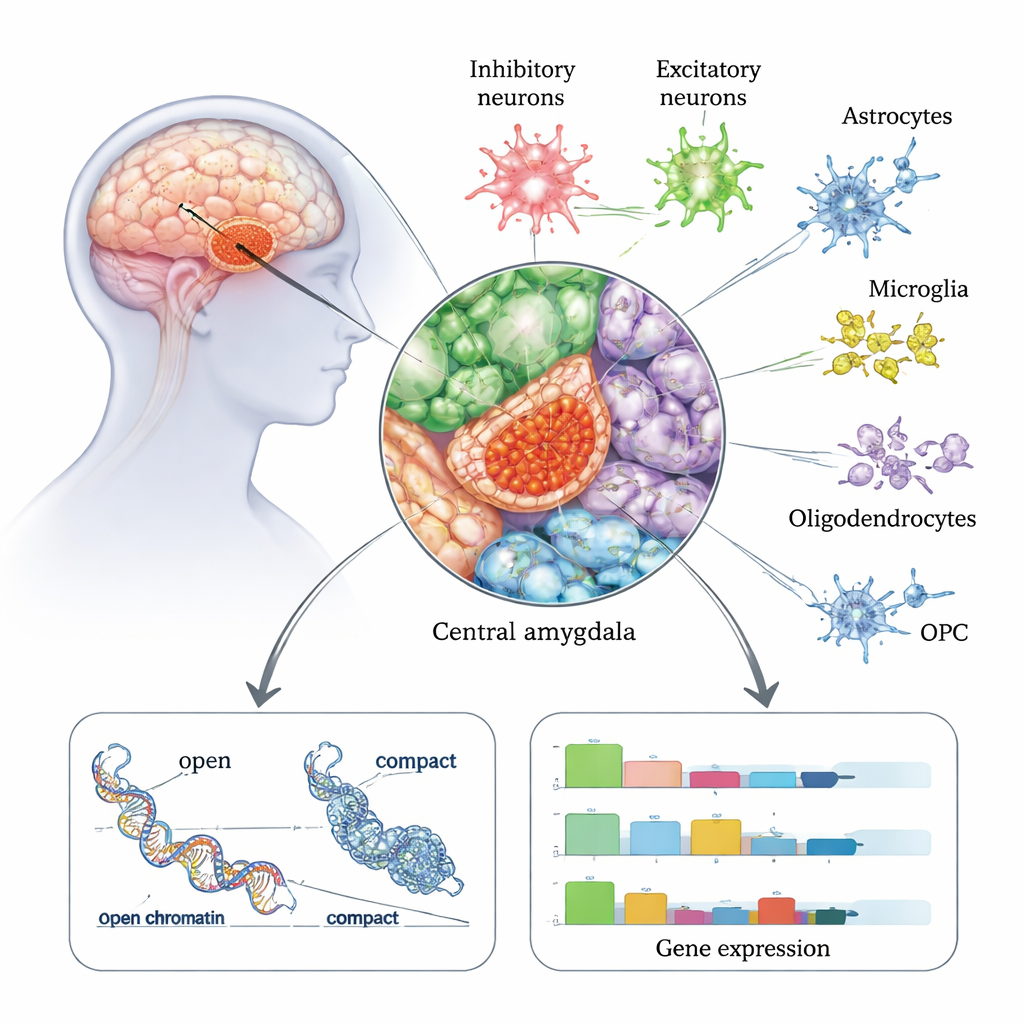
アルコール使用障害でどの細胞や遺伝子が変化するか?
研究チームは、細胞型ごとにAUDのある人とない人の遺伝子活動を系統的に比較しました。その結果、特定の細胞集団で活動が変化した遺伝子が1,800を超えることが判明し、最も大きな変化は抑制性ニューロン、次いで興奮性ニューロンやアストロサイトに見られました。ペプチド前駆体プロエンケファリン(PENK)でマークされる抑制性ニューロンの一亜型は特に顕著な変化を示しました。影響を受けた多くの遺伝子は脳細胞間の情報伝達、特に興奮性シグナルであるグルタミン酸と抑制性シグナルであるGABAのバランスに関わっています。例えば、主要なGABA受容体の構成に関わるGABRA2は特定の抑制性ニューロンで増加しており、一方でグルタミン酸受容体のGRM8やシナプスに重要な細胞接着分子であるNCAM1はニューロンの亜型間で逆方向に変化しました。これらのパターンは、中心扁桃体における興奮と抑制の微妙な調整がAUDで乱れていることを示唆します。
脳の制御スイッチ:クロマチンと調節エレメント
遺伝子は単独で働くわけではなく、スイッチや調光器のように機能するDNAの領域によって制御されています。クロマチン(DNAがどのように包装されているか)を調べることで、研究者らは50万を超える候補調節エレメントを同定し、細胞型特異的に近傍の遺伝子に結び付けました。これらのエレメントのほぼ半数は単一の細胞型に特有であり、異なる脳細胞がいかに特化しているかを浮き彫りにします。AUDで変化した多くの調節エレメントは、カルシウム処理やグルタミン酸シグナルに関わる遺伝子、例えばニューロンで強く活性なカルシウム結合遺伝子CALN1に結び付いていました。抑制性ニューロンでは、CALN1は発現の増加と緻密な調節ループの集積の両方を示し、アルコール暴露がこの遺伝子を制御する局所的なDNA構造を再形成していることを示唆します。 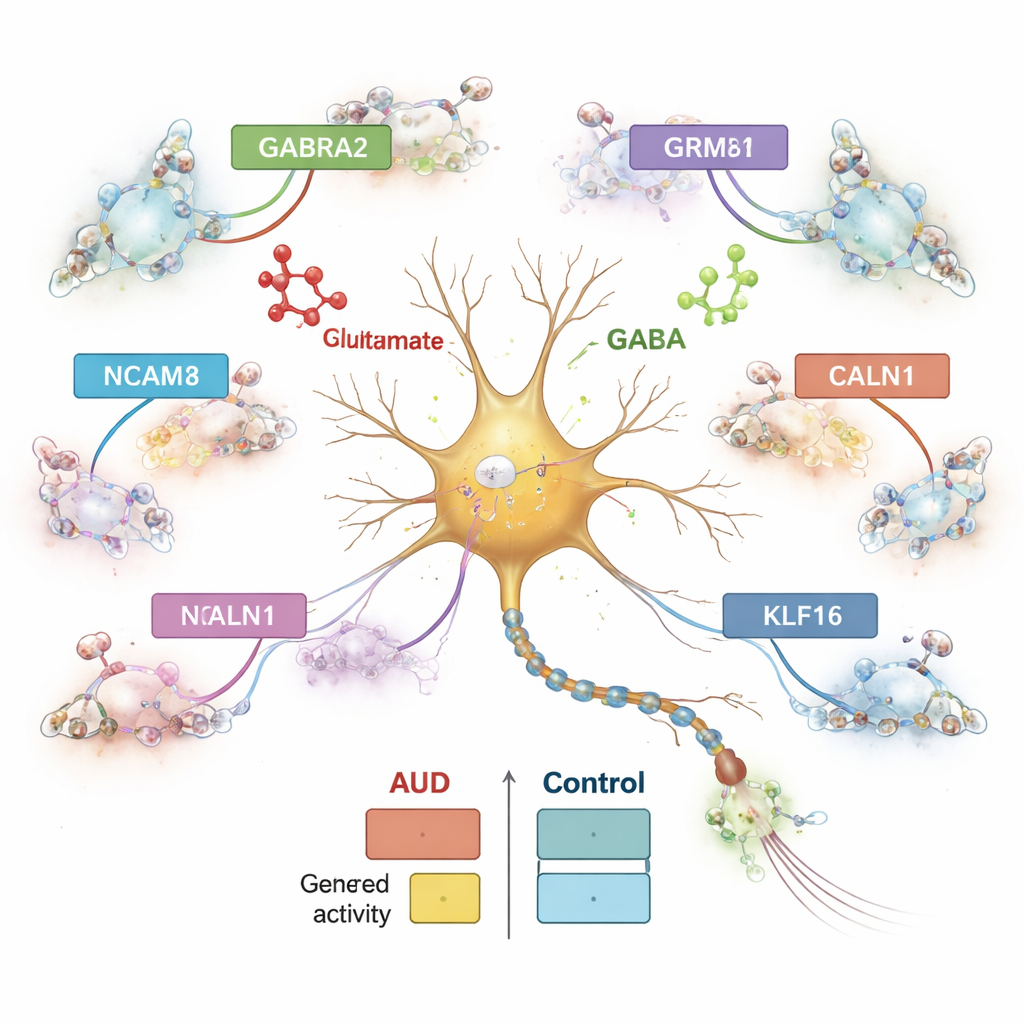
リスク遺伝子から実際の脳の変化へ
遺伝学的研究は、アルコール関連問題のリスクを高める多くのDNA変異を同定してきましたが、それらが脳のどこでどのように働くかは不明でした。彼らの単一細胞マップを大規模なゲノムワイド関連解析(GWAS)による問題的飲酒のデータと重ね合わせることで、リスク遺伝子が中心扁桃体のニューロン、特に抑制性ニューロンで不均衡に活性化・異常化していることが明らかになりました。細胞型で開いている調節エレメントの内部に位置する200以上の候補因果的リスクバリアントを特定しました。その中には、ニューロンの興奮性やドーパミンシグナルを制御するCACNA1CやDRD2のように依存症と既に結び付けられている遺伝子近傍のものもありました。また、SEMA6DやNF1といった新たな候補も浮上しました。研究チームはさらに、カルシウムやグルタミン酸関連遺伝子の広範な変化を調整しているとみられるKruppel様因子(特にKLF16)という転写因子群を同定し、この制御ネットワークの一部を急性アルコール暴露のマウスモデルで確認しました。
AUDの理解と治療にとっての意義
平たく言えば、本研究はアルコール使用障害が単なる拡散的な脳の問題ではなく、重要な情動ハブ内の特定の細胞型と分子経路に集中した高度に組織化された乱れであることを示しています。中心扁桃体の抑制性ニューロンやアストロサイトなどの支持細胞は、遺伝子活動とそれらの遺伝子を制御するDNAスイッチの協調的変化を示しており、とくにグルタミン酸、GABA、カルシウム信号を管理するシステムに影響が集中しています。これらの細胞変化を遺伝的リスクバリアントと結び付けることで、本研究は遺伝的脆弱性を脳内での具体的な分子事象に結びつけるロードマップを提供します。将来的には、このような細胞特異的アトラスが、脳全体に広く作用する治療ではなく、興奮と抑制のバランスを回復するより精密な治療法の開発を導く可能性があります。
引用: Lee, C.Y., Hwang, A., McRiley, D. et al. Central amygdala single-nucleus atlas reveals chromatin and gene transcription dynamics in human alcohol use disorder. Nat Commun 17, 1634 (2026). https://doi.org/10.1038/s41467-026-68351-1
キーワード: アルコール使用障害, 中心扁桃体, 単一細胞ゲノミクス, 抑制性ニューロン, 遺伝子制御