Clear Sky Science · ja
構造的・細胞的アプローチから見たTDP-43/RNA複合体の形成と疾患関連TDP-43凝集への移行
なぜこの脳タンパク質が重要なのか
筋萎縮性側索硬化症(ALS)や前頭側頭型認知症のような神経変性疾患では、神経細胞内に誤って折りたたまれたタンパク質の塊が見られることが多いです。最もよく関与する因子の一つがTDP-43というタンパク質で、通常は遺伝子の作業用コピーであるRNAの処理を助けます。本研究は重要な問いを投げかけます:健康な細胞でTDP-43は何をしており、どのような変化で有用なRNA補助因子が有害な凝集体形成タンパク質に変わるのか?
健康な神経細胞におけるTDP-43の働き
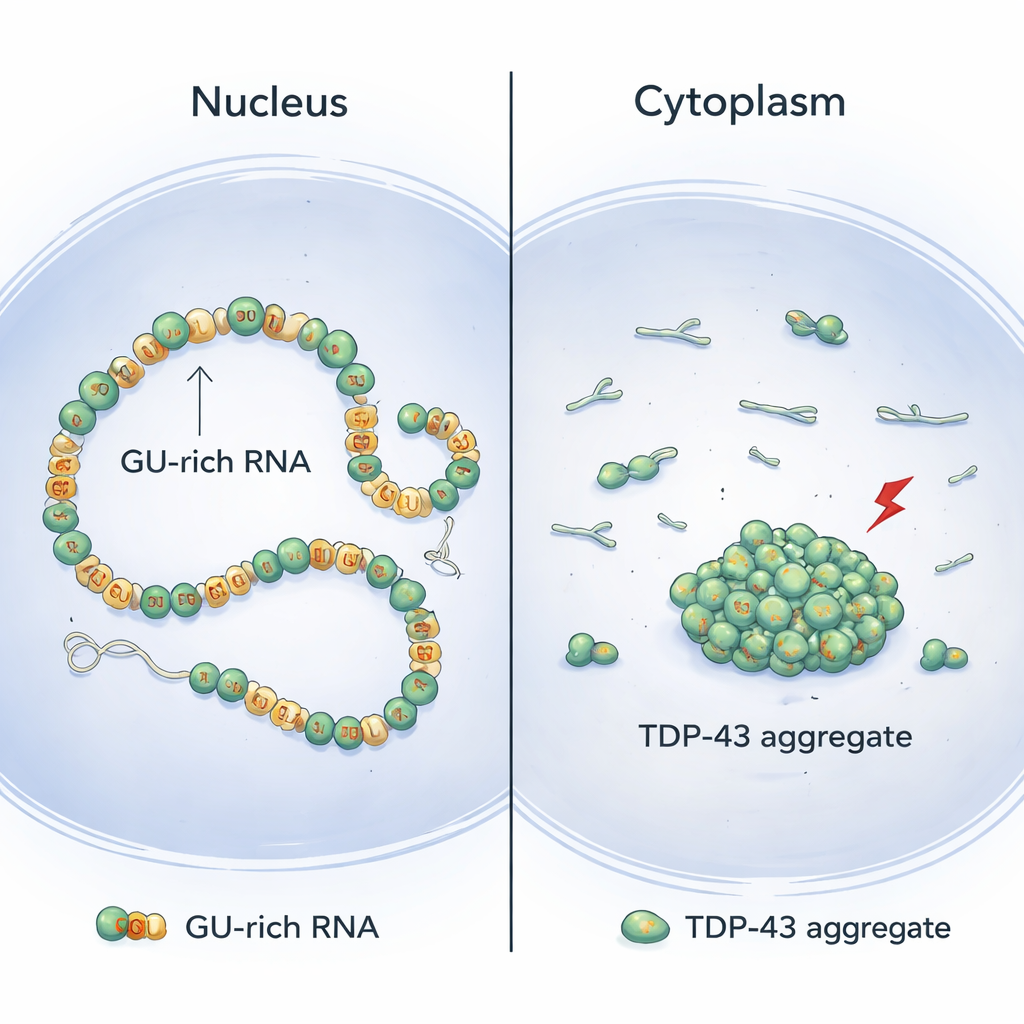
TDP-43は通常細胞核に局在し、繰り返し現れる「GU」配列に富む長いRNA伸長領域に結合します。構造生物学と細胞実験を組み合わせた解析により、著者らはTDP-43分子がこれらのGUリッチ領域に沿って協調的に並び、RNA上に滑らかで連続した鎖を形成することを示しました。このように配列されると、タンパク質の前部にあるN末端ドメインは隣接する分子間で物理的に隔てられます。その結果、これらのN末端断片は同じRNAの遠く離れたGUリッチ領域に手を伸ばして結びつけ、長いイントロン(遺伝子内の非コード領域)をやさしくループ化・コンパクト化する一方で凝集は起こりにくくなります。
タンパク質内部に組み込まれた綱引き
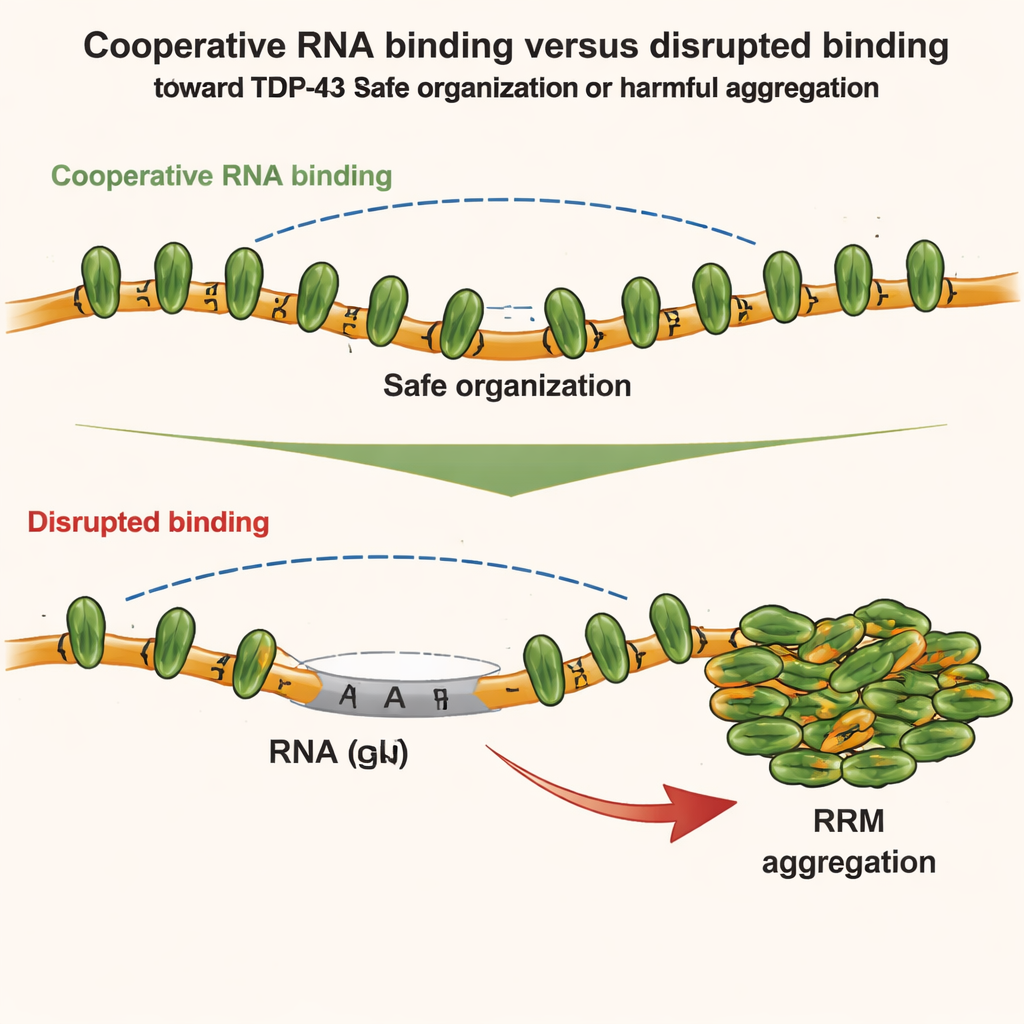
次にチームはTDP-43の異なる部分がどのように競合または協調するかを調べました。注目したのは二つの領域です:互いに付着し得るN末端ドメインと、GUリッチRNAに沿った協調的結合を促す中心部のRNA結合モジュール。NMR分光、示差熱量測定、小角X線散乱などの高感度手法を用いると、TDP-43が協調的にRNAに結合すると鎖の幾何学が隣接分子間の直接的なN末端–N末端接触をむしろ弱めることがわかりました。言い換えれば、強い協調的RNA結合は局所的なN末端相互作用を抑制します。しかし、この協調性が壊れると—たとえばRNAに非GU配列を挿入するかTDP-43を変異させると—近接するタンパク質のN末端領域は互いに接近し、結合し得る状態になります。
有益なコンパクト化から有害な凝集へ
これらの構造学的知見は生細胞で検証されました。著者らは設計された細胞系を用いて、異なるTDP-43変異体が人工的なRNAリッチコンパートメント内でどのように混ざり合うか、あるいは分離するかを追跡しました。協調的なRNA結合とN末端相互作用はともにTDP-43を高次集合体へと組織するのに寄与しますが、その働き方は異なります。協調的結合はGUリッチRNAに沿ってタンパク質を連結し、N末端接触は遠く離れたクラスター同士をつなぎます。しかし軽度の酸化ストレス下では状況が変わります。ヒ素化合物のような化学的ストレッサーは中心部のRNA結合モチーフに特定の化学修飾—アセチル化—を引き起こし、それらを互いに粘着しやすい状態にします。協調的なRNA結合が保たれていればTDP-43は主に可溶性のままですが、協調性が弱まると近接するTDP-43分子間のN末端結合が骨組みのようにアセチル化されたコアを引き寄せ、不可逆的な凝集を促進します。
なぜTDP-43は細胞質でより多く凝集するのか
本研究から導かれるモデルは、なぜ疾患におけるTDP-43凝集が核ではなく細胞質でよく見られるのかを説明する助けになります。核内では多くのGUリピートを含む長いイントロンが一般的で、連続的で協調的な結合が起こりやすく、近隣間のリスキーなN末端接触が低く抑えられ、安全な長距離ループ形成が促されます。一方で細胞質では成熟RNAはGUリッチ領域がはるかに少なく、TDP-43の結合はむらがちで協調性が低くなり、隣接するN末端ドメイン同士が相互作用する可能性が高まります。そこにストレス誘導性の化学変化が加わると凝集の舞台が整います。支持する証拠として、核内に余分なGUリッチイントロンを人工的に供給するとストレス下でのTDP-43凝集が減少しました。
今後の治療への意味
要するに、この研究はTDP-43を有益なRNA組織化と有害な凝集との間でバランスを取るタンパク質として描いており、GUリッチRNAへの協調的結合が安全装置として機能していることを示しています。その安全網が—RNA配列の変化、タンパク質変異、または細胞ストレスによって—損なわれると、通常は長いRNA断片をコンパクトにするドメインが毒性をもつ凝集体の形成を促すようになります。専門外の方への主要な示唆は、TDP-43とRNAの間の適切な相互作用を維持することが、ALSや関連する脳疾患で見られるタンパク質凝集を防ぐか遅らせる有望な戦略になり得る、という点です。
引用: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
キーワード: TDP-43凝集, RNA結合タンパク質, ALS, タンパク質–RNA相互作用, 神経変性