Clear Sky Science · ja
グリセロール3-リン酸アシルトランスフェラーゼは脂質過酸化を増加させることでα-シヌクレイン誘発毒性を悪化させる
なぜ脳の脂質がパーキンソン病で重要なのか
パーキンソン病は通常、α-シヌクレインというタンパク質が凝集して運動を制御する脳細胞を損なう問題として説明されます。本研究は、脳の脂質—特にその合成と損傷のされ方—がα-シヌクレインの毒性をどれほど強めるかに驚くほど大きな役割を果たすことを示しています。神経細胞の損傷を悪化させる脂質合成酵素を明らかにすることで、パーキンソン病の根本に対処する既存の取り組みを補完し得る、薬剤で狙える新たな経路を示しています。
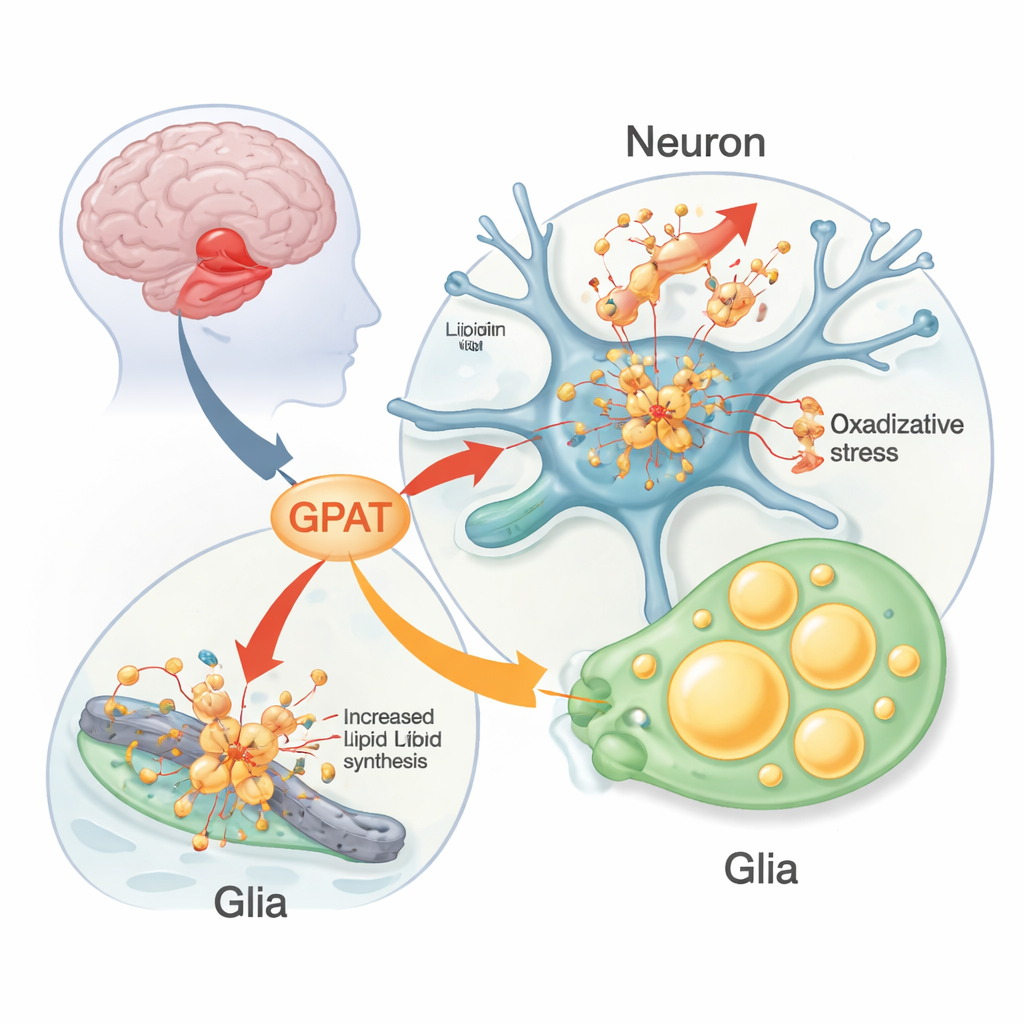
パーキンソン病で不正に振る舞うタンパク質
パーキンソン病の患者は、運動を調整する深部脳領域のドーパミンを産生する神経細胞を徐々に失います。これらの死にゆく細胞の内部では、研究者はしばしばルイ体と呼ばれる密な沈着物を見つけ、それはα-シヌクレインを多く含んでいます。まれな家族例では、α-シヌクレイン遺伝子の変異やコピー数増加が直接パーキンソン病を引き起こしますが、一般的な遺伝的変異はリスクをわずかに高めるにすぎません。これは、他の遺伝子や経路がα-シヌクレインの有害性を修飾していることを示唆します。増えつつある証拠は、細胞膜やエネルギー貯蔵を形成する脂質—脂肪や脂肪様分子—が、α-シヌクレインの凝集と神経細胞死の双方で重要な共犯者であることを指し示しています。
ショウジョウバエモデルで見つかった強力な脂質酵素
研究者らは、神経系でヒトのα-シヌクレインを発現するよう改変したショウジョウバエを生きた試験系として用いました。これらのハエはパーキンソン様の問題を呈します:ドーパミン産生ニューロンの喪失、登攀運動の困難、日内活動リズムの乱れなどです。チームは、α-シヌクレインの影響を変えるハエのヒトのパーキンソン病リスク遺伝子相同を系統的に変化させました。その中で際立っていたのがminoという遺伝子で、ミトコンドリアに局在するグリセロール3-リン酸アシルトランスフェラーゼ(GPAT)の形態を作ります。GPATはホスホ脂質やトリグリセリドの合成の入り口に位置し、膜や脂肪滴を形成する脂質の供給を担います。神経でのmino活性を低下させると、α-シヌクレイン発現ハエはより多くのドーパミンニューロンを保ち、運動能力が長く維持されました。一方、minoの増強は逆に有害な効果をもたらしました。
損傷した脂質、ストレスを受けたミトコンドリア、グリアの脂肪滴
さらに踏み込むと、GPATは脳脂質に蓄積する酸化的損傷の程度に影響を与えることが分かりました。病態を悪化させる高温で飼育したα-シヌクレインハエでは、脳膜での脂質過酸化、つまり脂質の化学的“さび”が増加しました。minoを下げるとこの損傷は減り、過剰発現すると増加しました;α-シヌクレインがない場合は、minoの変化はほとんど影響を与えませんでした。視覚中枢領域での細胞死マーカーも同様のパターンを示しました。研究チームはまた、脂肪滴—微小な脂質貯蔵球—がニューロン自体ではなく隣接するグリア細胞に著しく蓄積しているのを観察しました。これらの脂肪滴はα-シヌクレインハエで年齢とともに拡大し、トリグリセリドを合成または分解する酵素によって変動し、ストレス下におけるニューロンとグリア間の活発な代謝的協調を浮き彫りにしました。
代謝の再配線とα-シヌクレインの凝集
ハエ脳の代謝物測定では、α-シヌクレイン発現が細胞のエネルギー生産サイクルにおけるボトルネックと結びついていることが示されました:クエン酸およびイソクエン酸というTCA(クエン酸回路)中間体が強く蓄積し、下流の段階はより控えめに変化していました。乳酸レベルも上昇しており、解糖系の亢進と一致します。同時に詳細な脂質プロファイリングは、膜ホスホ脂質のバランスや脂肪酸組成の変化を示し、酸化損傷を受けやすい種が優勢になっていました。ミトコンドリアにあるminoや小胞体上の関連GPAT酵素をいくつか低下させると、α-シヌクレインは蓄積し続けましたが、高次オリゴマー(多タンパク束)を形成する傾向は低下し、ミトコンドリアの活性酸素ストレスや“老化”の兆候も少なくなりました。
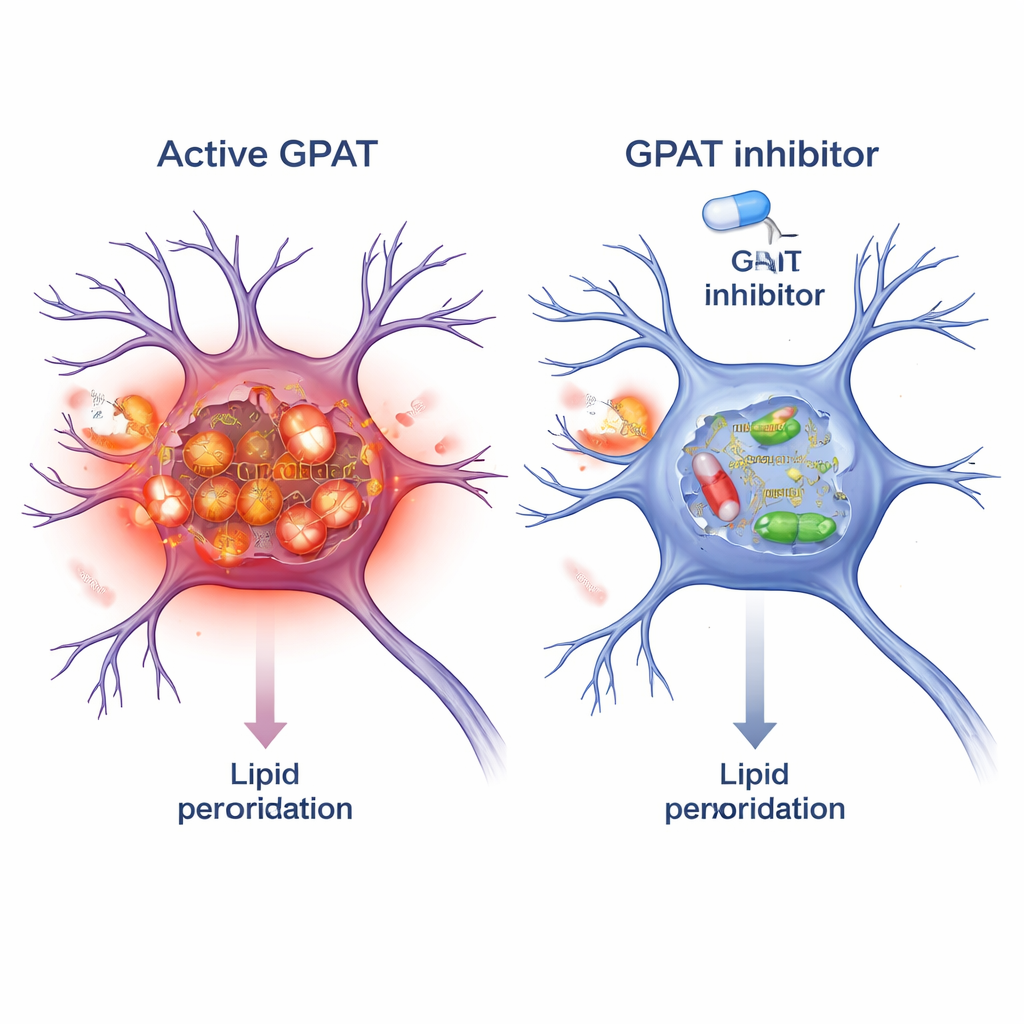
GPATを阻害することの保護的戦略としての可能性
GPATは酵素であるため、小分子薬で標的にしやすいという利点があります。研究者らは肥満や糖尿病向けに開発されたいくつかの既存GPAT阻害剤のうち、FSG67を試しました。α-シヌクレインハエにFSG67を餌に混ぜると、遺伝学的なGPATノックダウンの利点が再現されました:運動能の改善、ドーパミンニューロンの生存率向上、害のあるα-シヌクレインオリゴマーの減少、ミトコンドリア酸化ストレスの低下です。この概念が哺乳類にも当てはまるかを検証するために、彼らは培養したマウス脳ニューロンに事前形成したα-シヌクレイン線維(毒性凝集を種々誘導する)を処理しました。FSG67との同時処理は、リン酸化α-シヌクレインの蓄積を減らし、これらのニューロン内での複数の独立した脂質過酸化マーカーを低下させました。
これはパーキンソン病の患者にとって何を意味するか
平たく言えば、本研究は脳が脂質をどう扱うかがα-シヌクレインの毒性を上げたり下げたりできることを示しています。GPATが高活性のとき、より酸化されやすい脂質が膜や貯蔵滴に組み込まれ、それらは酸化されやすくなります;この損傷した脂質環境は有害な形態のα-シヌクレインを促進し、細胞の発電所であるミトコンドリアに負担をかけるように見えます。GPATを遺伝的に、または薬剤で下げることは、脂質の“さび”を減らし、有毒なタンパク質集合体を減少させ、ニューロンの健康を改善する方向へバランスを変えます。これらの発見はまだ初期段階であり、ハエや培養マウス細胞に基づくものですが、脂質代謝、特にGPATを注目すべき新たな治療角度として浮かび上がらせ、α-シヌクレインを直接標的にする戦略を補完し得る可能性を示しています。
引用: Ren, M., Lim, G.G.Y., Tang, W. et al. Glycerol 3-phosphate acyltransferase exacerbates α-synuclein-induced toxicity by increasing lipid peroxidation. Nat Commun 17, 1618 (2026). https://doi.org/10.1038/s41467-026-68325-3
キーワード: パーキンソン病, α-シヌクレイン, 脂質過酸化, GPAT阻害剤, 神経変性