Clear Sky Science · ja
SHOC2-KRAS-PP1C複合体の構造が明かすRASアイソフォーム特異的決定因子とRAS阻害剤による複合体形成阻害の示唆
細胞が増殖するかどうかを決める仕組み
細胞は増殖するか分裂するか、あるいは静止するかを決めるために細胞内の配線のような仕組みに依存しています。その中心にあるのがRASタンパク質で、微小な分子スイッチとして働き、がんではしばしば異常をきたします。本研究は、SHOC2、RAS、PP1Cという特定のタンパク質群がどのように結合して重要な成長スイッチを切り替えるか、そして現在のがん薬がその過程をどのように阻害できるかを詳しく調べ、治療に対する腫瘍の回避を防ぐ方法について洞察を与えます。
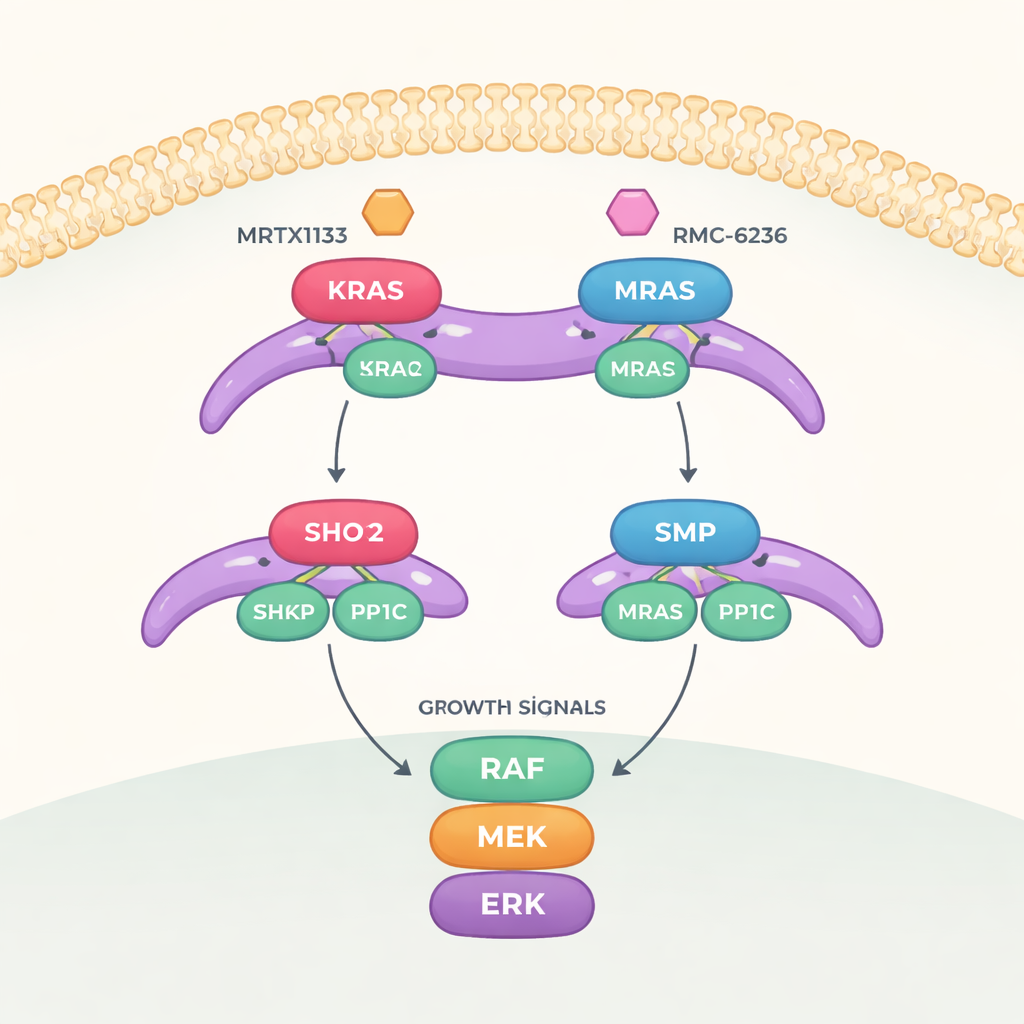
3つの重要な要素からなる成長スイッチ
本研究は、細胞表面から核へ成長のメッセージを伝えるMAPK経路に着目しています。この経路を完全にオンにするには、別のタンパク質であるRAFを“オフ”から“オン”に切り替える必要があります。そのスイッチは、SHOC2(足場として複合体を保持する)、PP1C(リン酸基を除去する酵素)、および活性化されたRASタンパク質からなる三者複合体によって制御されます。この三者が結合すると、RAFから特定のリン酸修飾が除去され、下流の成長カスケードが活性化されます。
低親和性の仲間ががんで重要である理由
RASにはいくつかの種類があります。MRASはSHOC2およびPP1Cと非常に強固な複合体を形成する一方で、より知られているがんドライバーであるKRAS、HRAS、NRASは同様の複合体をより弱く形成します。驚くべきことに、変異KRAS、HRAS、NRASによって駆動されるがん細胞は、複合体が不安定であってもSHOC2に強く依存することが示されました。大規模な遺伝学的スクリーニングのデータは、特にQ61やG13のような重要な位置に影響する特定のRAS変異を持つ多くの腫瘍がSHOC2の喪失に非常に感受性を示すことを示しており、この複合体が生存に不可欠であることを示しています。
KRAS複合体の形を明らかにする
これまで、研究者は高親和性のMRASベースの複合体の高解像度構造しか得られていませんでした。KRAS版はあまりに脆弱で撮像が困難でした。本研究では、病気に関連する変異を利用して構成要素間の接触をわずかに強め、SHOC2–KRAS–PP1C複合体をクライオ電子顕微鏡で観察できるほど安定化しました。その結果、全体的な構造はMRAS複合体とよく一致するものの、KRASはMRASがSHOC2やPP1Cをより確実に保持するために用いるいくつかの小さな構造的特徴を欠いていることが分かりました。そのためKRAS複合体は接触面積が小さく、結合も少なく、結果として本来不安定である理由が説明されます。とはいえ、KRASが過活動な腫瘍では依然として重要な役割を果たします。
RAS阻害剤はどのように複合体形成を妨げるか
研究チームは次に、RASを標的とする2つの薬剤クラスがこの三者複合体にどのように影響するかを調べました。KRASの柔軟な領域であるスイッチII近傍のポケットに結合するよう設計されたMRTX1133は、この領域をSHOC2の面と衝突する形にロックします。これにより新しいSHOC2–KRAS–PP1C複合体の形成が強く阻害されますが、既に存在する複合体を解体する効果はやや限定的です。第二の薬剤であるRMC-6236は、シクロフィリンAという補助タンパク質と協同して作用し、SHOC2結合に必要な同じKRAS表面を遮断します。しかし、どちらの薬剤も自然にはMRASに結合しないため、高親和性のMRAS複合体はそのまま残り、KRASが阻害されたときに成長経路を再活性化する手助けをする可能性があります。
耐性を防ぐための二重標的化に向けて
二重標的化が可能かを検証するため、研究者らはMRASのスイッチIIポケットを改変し、MRTX1133が結合できるようにした変異体を作製しました。この変異体は依然としてSHOC2およびPP1Cと強い複合体を形成しましたが、薬剤はその形成を阻害し、試験管内アッセイでRAFをオンにする能力を低下させました。SHOC2結合化合物に関するデータと合わせると、KRASベースとMRASベースの両方の複合体を遮断する薬を設計することは現実的であることが示されます。一般向けに言えば、がん細胞は一つのスイッチが薬で抑えられても成長シグナルを維持するために複数の密接に関連したバックアップスイッチを使います。これらタンパク質複合体の正確な形や接触部位を理解することで、研究者は両方のバックアップ経路を同時に狙う治療法を設計でき、RAS駆動がんが適応して耐性を獲得するのを難しくできます。
引用: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
キーワード: RASシグナル伝達, KRAS阻害剤, MAPK経路, タンパク質複合体, 薬剤耐性