Clear Sky Science · ja
ヌクレオチド類似体ベースの抗ウイルス薬に対するSARS-CoV-2の耐性の仕組み
ウイルスが主要な抗ウイルス薬を出し抜く方法
COVID-19ウイルスは、自己の遺伝情報を校正できるというまれなRNAウイルス群に属しており、そのため一部の有力な抗ウイルス薬に対して特に耐性を示しやすい。この研究は、SARS-CoV-2がヌクレオチド類似体と呼ばれる広く使われている薬剤群をどのように検出し除去するかを原子レベルで解き明かし、他のウイルスには有効な薬がコロナウイルス感染ではしばしば効果を発揮しにくい理由を説明する。
ウイルスRNAをめぐる綱引き
SARS-CoV-2は約3万塩基のRNAゲノムを、複製転写複合体と呼ばれる大きな分子機械で複製する。その中心には新しいRNA鎖を合成するRNA依存性RNAポリメラーゼ(RdRp)があり、別のユニットとして誤りを校正し切断するエキソヌクレアーゼ(ExoN)が存在する。肝心の多くの抗ウイルス薬は、元のRNA構成要素に非常に似せて作られ、RdRpによって取り込まれると鎖延長を止めたりエラーを導入したりする。しかし残念ながらコロナウイルスはExoNを持ち、挿入されたこれらの“偽物”を認識してRNA鎖から切り取ることができ、ウイルスの複製を救ってしまう。
薬がRNAの相棒を切り替えてしまうとき
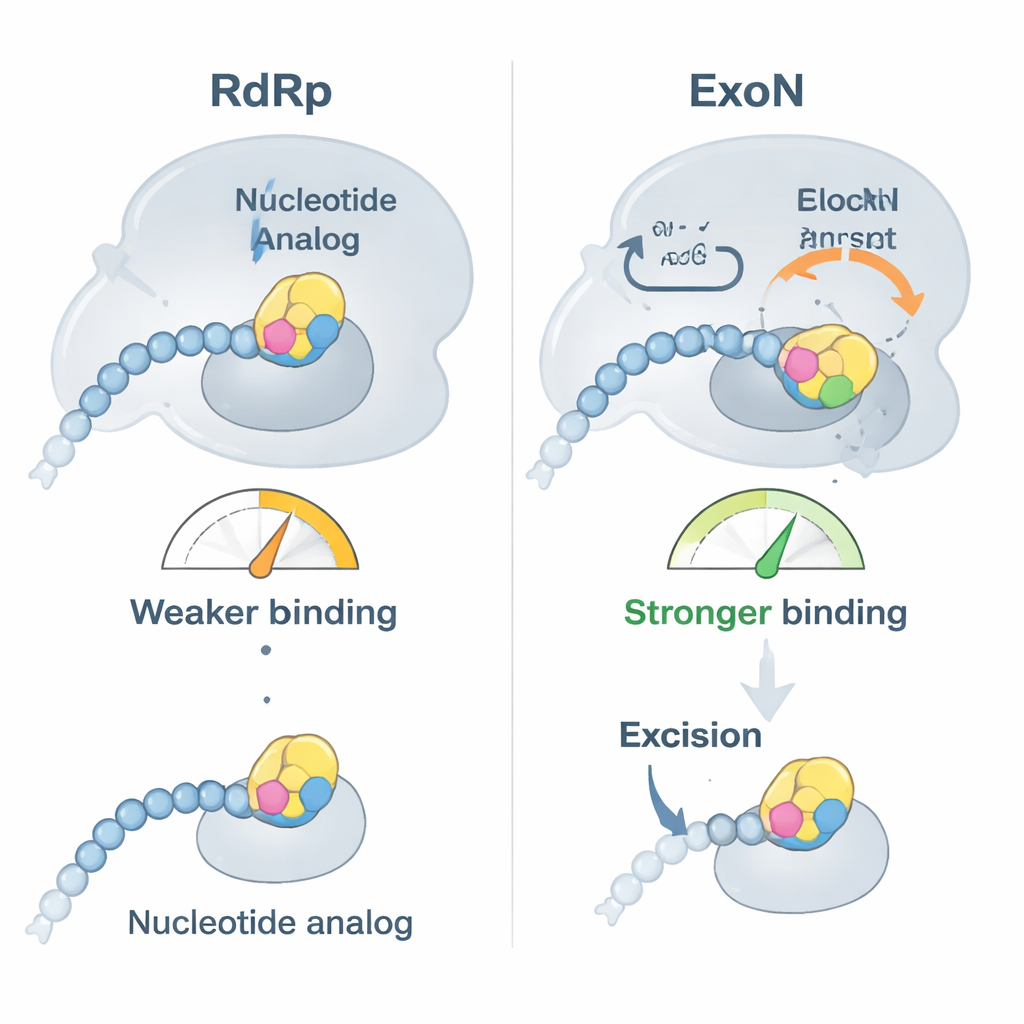
研究者たちは、欠陥のあるRNA構成要素として設計された臨床上重要な2つの抗ウイルス薬、ベムニフォスブビルとソホスブビルに着目した。まず、SARS-CoV-2のポリメラーゼがこれらの類似体をRNA鎖の末端に容易に挿入し、その後ほぼ鎖の伸長を止めることを示した。ところが結合試験ではひとつのひねりが明らかになった。類似体がRNAの先端に位置すると、RNAはもはやポリメラーゼに強く結合せず、代わりにExoNにより強く結合するようになるのだ。実質的に、薬剤で修飾されたRNAは複製機から押し出され校正装置に手渡され、そこで問題のヌクレオチドが切り取られて複製が再開される機会が与えられる。
遅くなるが止められない校正
生化学的な時間経過実験により、ExoNはベムニフォスブビルやソホスブビルをRNAから除去するが、通常のヌクレオチドを除去するよりも遅いことが示された。細胞フリーの反応系では、両類似体はそれ自体でRNA合成を強く阻害した―にもかかわらず活性化したExoNを加えると、停止したRNA鎖の相当部分が救われて伸長された。働かないExoN変異体ではこの効果が見られず、校正活性が薬の効果を相当程度取り消していることが確認された。さらに、ポリメラーゼがExoNと共存すると類似体の除去が速まることから、これら二つのウイルス酵素が障害を取り除き複製を維持するため協調して働いていることが示唆される。
原子分解能で校正装置を観察する
ExoNがこれらの薬剤をどのように認識し反応するかを理解するため、研究チームは高分解能クライオ電子顕微鏡を用い、ベムニフォスブビルまたはソホスブビルで終端したRNA鎖に結合したExoN複合体の構造を解いた。個々の化学基が識別できるほど鮮明なこれらの構造は、各薬剤の修飾糖環がExoNタンパク質の短いループで形成される疎水性ポケットにはまり込んでいることを明らかにした。この追加の密着が薬を含むRNAのExoNへの強い結合を説明する。しかし同時に意外な副作用もあった。そのループを引っ張ることで、近傍の触媒ループの精密な配置が乱れ、重要なヒスチジン残基の位置がずれてしまうのだ。このヒスチジンが切断部位から外れると、ExoNの活性中心は部分的に非活性化され、類似体の切除が遅くなるが完全には阻止されない。
ウイルス校正を調節する組み込みのスイッチ
この敏感なループ内の個々のアミノ酸を変異させると、その重要性が確かめられた。保存された4つの残基を変えると、ExoNが標準的なRNA末端や薬で終端した末端の両方を切る能力が大幅に低下し、さらにExoNがどの末端塩基を好んで除去するかも変わった。これはそのループがアロステリックな調節因子、つまりRNA先端の塩基の種類を感知して酵素活性を調整する内蔵の機械的スイッチであることを示す。構造はまた、ExoNが可変的な水素結合を通じて異なる塩基(A、U、C、G)を認識する一方で、グアニン様塩基の収容が最も困難であることを示しており、ベムニフォスブビルがグアノシンを模倣する点はここで関連する。
今後のCOVID-19治療薬に与える意味
専門外の読者にとっての要点は、SARS-CoV-2が高度な「つづりチェッカー」を備えており、複製を一時停止させる目的でゲノムに挿入された特定の薬剤を後で引き抜けるということだ。ベムニフォスブビルとソホスブビルはウイルスの複製装置を弱めるが、同時にRNAを校正装置へと誘導し、その効果を部分的に取り消される道を作ってしまう。本研究が明らかにしたのは、ウイルスの校正装置がこれらの薬剤をどのように保持するか、そして小さな調節ループが酵素を活性状態と低活性状態の間でどう切り替えるかという正確な仕組みである。これらの知見は、ExoNに結合しにくい、あるいはExoNを不活性なコンフォメーションに固定する、またはグアニン様構造を扱う際の困難を逆手に取るような新たな抗ウイルス性ヌクレオチドを設計するためのロードマップを提供する。次世代のこうした分子はウイルスに“消されにくく”なり、COVID-19や将来のコロナウイルス流行に対する治療効果を高める可能性がある。
引用: Liu, C., Li, Y., Cao, X. et al. Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals. Nat Commun 17, 1601 (2026). https://doi.org/10.1038/s41467-026-68304-8
キーワード: SARS-CoV-2, 抗ウイルス薬耐性, ヌクレオチド類似体, RNA校正機構, コロナウイルス複製