Clear Sky Science · ja
試料消費に特に焦点を当てたタンパク質X線結晶構造解析の試料供給法のサンプル
分子の活動を観る
X線結晶学は、生命を駆動する小さな機械であるタンパク質の原子配列を科学者に見せてくれます。シリアル結晶学と呼ばれる新しい手法はさらに一歩進み、酵素が薬物を処理する様子や光合成タンパク質が水を分解する様子など、タンパク質の「分子ムービー」を捉えることができます。しかし問題があります。多くの重要なタンパク質は生成や結晶化が難しく、現在の実験ではミリグラムからグラム単位の貴重な試料が消費されてしまうことが少なくありません。本総説は一見単純な問いを投げかけます:強力なX線ビームに結晶を供給しつつ、いかにして試料の無駄を最小限にできるか?
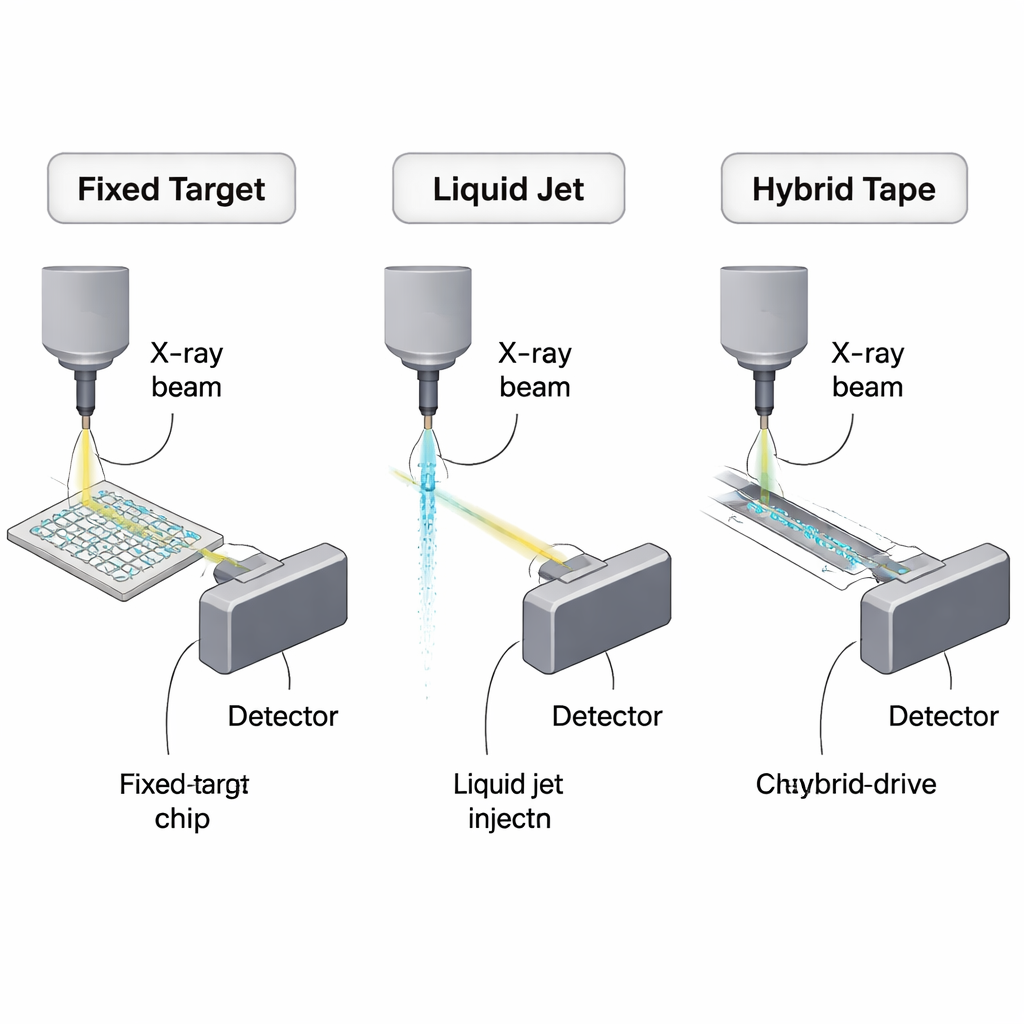
なぜシリアル結晶学で供給法の改善が必要か
従来の結晶学は大きな単結晶をX線ビームの中で回転させる方法に依存していました。シリアル結晶学はこれを覆し、一つの大きな結晶の代わりに、各々が一度だけ使われる何千ものマイクロ結晶をシンクロトロンやX線自由電子レーザー(XFEL)からの超高輝度パルスに向けて走査または噴射します。これにより室温でのデータ収集や化学反応の高速「スナップショット」が可能になりますが、同時にパルス列のレートに合わせて結晶を継続的に補充する必要があり、パルス列は秒間百万に達することもあります。実際には多くの結晶懸濁液がビームに触れることなく廃棄されるため、試料消費の低減はこの分野の重要な技術的かつ経済的課題となっています。
固定ターゲット:一滴も無駄にしない小さなチップ
一つの主要戦略は、固定ターゲットと呼ばれる小さな固体支持体上にマイクロ結晶を固定することです。結晶をビームのそばで噴霧する代わりに、研究者はシリコンやポリマーのチップ上に結晶を配列させ、チップを移動して各結晶を一度だけX線焦点に入れます。理論上の最良ケースでは、モデルタンパク質の約1万個のマイクロ結晶で、概ね450ナノグラムのタンパク質だけで完全なデータセットが得られる可能性があります。実際の装置はまだそこまで節約的ではありませんが、すでに必要量を数十マイクログラムから数百マイクログラム程度にまで削減しており、初期のシリアル実験に比べて桁違いの改善を示しています。総説はシリコンメッシュ、超薄ポリマーフィルム、多層プラスチックチップを比較し、利点(低バックグラウンド散乱、チップ上での結晶成長、室温実験との相性)を、脱水、チップ材料からの散乱、手作業でのピペッティングによる余分な“デッドボリューム”といった実際的な問題と秤にかけて論じています。
液体ジェットと高粘度ストリーム:速いが試料を喰う
別の方法群は結晶を液体中に浮遊させたまま連続的にビームの下へ供給します。ガス動力学的仮想ノズル(GDVN)は髪の毛のように細いジェットを作り、速いXFELパルス列に追従できるため、時間分解研究や混合直後に反応を誘起するミックス&インジェクト実験で広く用いられています。しかしジェットは連続的に流れるため、ストリームの大部分はX線パルスに当たらずに流れて行きます。入念な最適化をしても実験で消費されるタンパク質は理論的最小値よりはるかに多く、典型的には濃縮された結晶スラリーで数十〜数百マイクロリットルに達します。損失を和らげるために、犠牲的な液体で結晶流を覆うダブルフローノズル、低流量で動作する電気紡糸“MESH”インジェクタ、ゲルや脂質二次元相に埋めた結晶を毎分マイクロリットル以下で押し出す高粘度エクストルーダーなど、より効率的な設計が開発されてきました。これらの粘性流動法は壊れやすい膜タンパク質やシンクロトロンでの室温実験に特に有用ですが、流路が太いため背景散乱が増え、最も高速のX線源には不向きな場合があります。
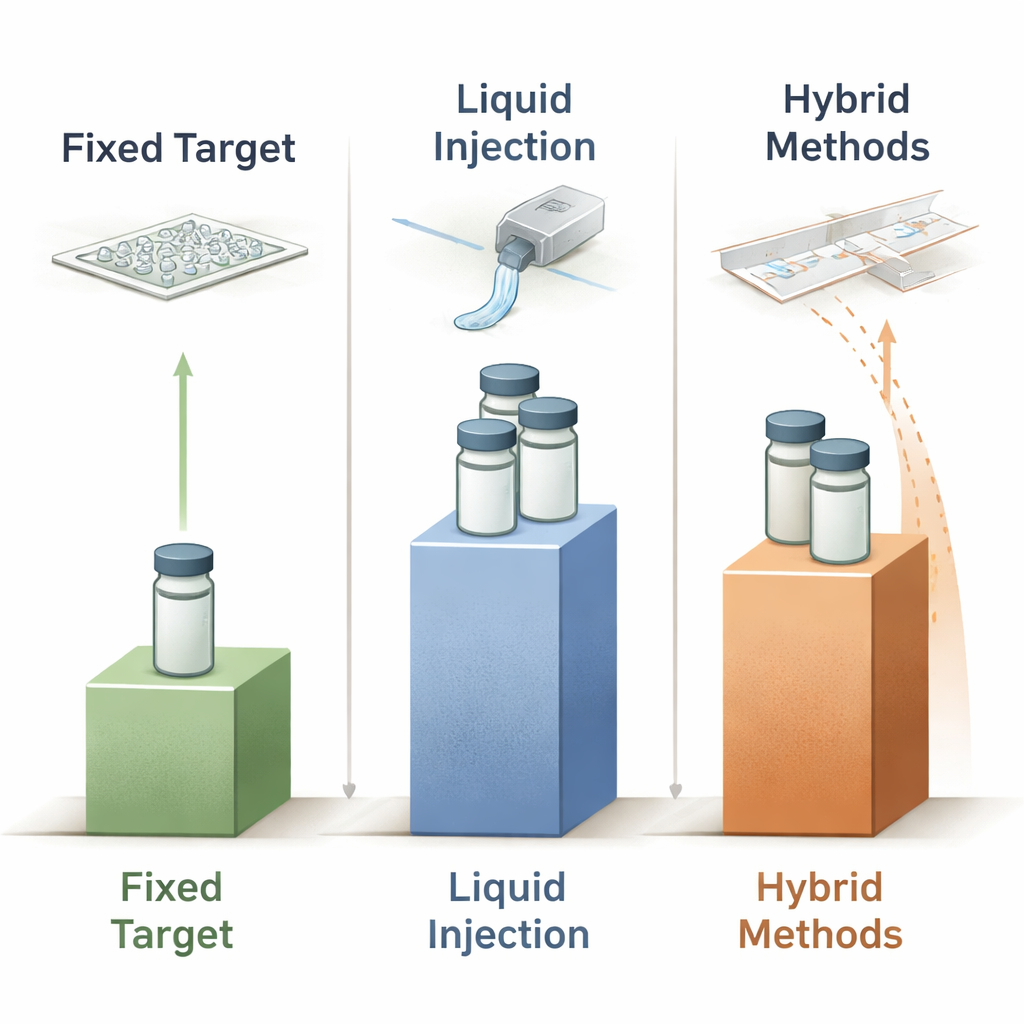
ドロップ、テープ、ハイブリッド:パルスに一つずつ合わせる
第三の、ますます創造的になっているクラスは、固体支持体と制御された液体またはドロップレット供給を組み合わせた“ハイブリッド”アプローチです。テープドライブシステムは例えば、移動するポリマーフィルム上にドロップレットや薄い液体ストライプを堆積し、そのフィルムをビームに通す方式で、移動のタイミングを制御することで反応ステップやガス暴露を定められた遅延で調べることができます。ドロップオンデマンド方式はさらに進み、音響や圧電デバイスを用いてX線パルスが来ると予想されるときにのみナノリットルあるいはピコリットルのドロップレットを噴出し、廃棄を劇的に減らします。中には、テープ上の既置の結晶含有ドロップレットにリガンドドロップレットを到達直前に混合する設計もあり、慎重に配分した試薬で時間分解酵素学を可能にします。LAMAオンチップ法のように、固定ターゲットチップ上に事前に配置した結晶に微量の基質ドロップを直接加えるハイブリッドもあります。これらの設計全体で報告されるタンパク質使用量は幅広く、フルの時間分解シリーズでミリグラム近くから数ミリグラムに達するものまであり、ドロップレット、結晶、X線パルスの同期化に関する約束と現在の工学的課題の両方を示しています。
理論的最小値にどれだけ近づいているか?
固定ターゲット、液体インジェクタ、ハイブリッドシステムにまたがる数十の公開実験を比較すると、著者らは既存のどの方法も理想的な450ナノグラムのベンチマークには近づいておらず、最良の装置でも概ね二桁程度の過剰消費が残っていることを示しています。しかし明確な傾向も見えます。固定ターゲットは通常最も少ないタンパク質で済み、時間分解混合が不可欠でない場合やチップ上で工夫できる場合に魅力的です。液体ジェットは依然として最も厳しい時間分解XFEL研究を支配していますが、特に多くの時間点が必要な場合は試料集約的です。ドロップ&テープ系のハイブリッドは、特にドロップのタイミングがX線源と厳密に同期される場合に相対的な節約効果が大きく出ます。今後の進展は、より良いマイクロ流体制御、無駄な取り扱いを排する自動化、コンパクトなX線源の活用、そしてデータ駆動型の最適化による実験と供給システムの協調設計からもたらされ、タンパク質消費を理論上の限界にますます近づけるだろうと論じられています。
引用: Manna, A., Doppler, D., Sripati, M.P. et al. Sample delivery methods for protein X-ray crystallography with a special focus on sample consumption. Nat Commun 16, 9856 (2025). https://doi.org/10.1038/s41467-025-65173-5
キーワード: シリアル結晶学, タンパク質X線結晶構造解析, 試料供給, X線自由電子レーザー, マイクロ流体