Clear Sky Science · ja
臓器工学の神経中枢
臓器に配線を引くことが重要な理由
研究者たちは、心臓や肝臓、腎臓などドナー臓器の深刻な不足に対処するため、代替臓器を試験管内で作る技術に近づいています。しかし、多くの人工臓器は血管系に注目する一方で、もう一つの重要な要素、すなわち神経を無視しています。本総説は、体の電気的配線が臓器の成長、日常機能、治癒に不可欠である理由と、研究者がどのようにして試験管内で作られた臓器に神経ネットワークを織り込もうとしているかを説明します。
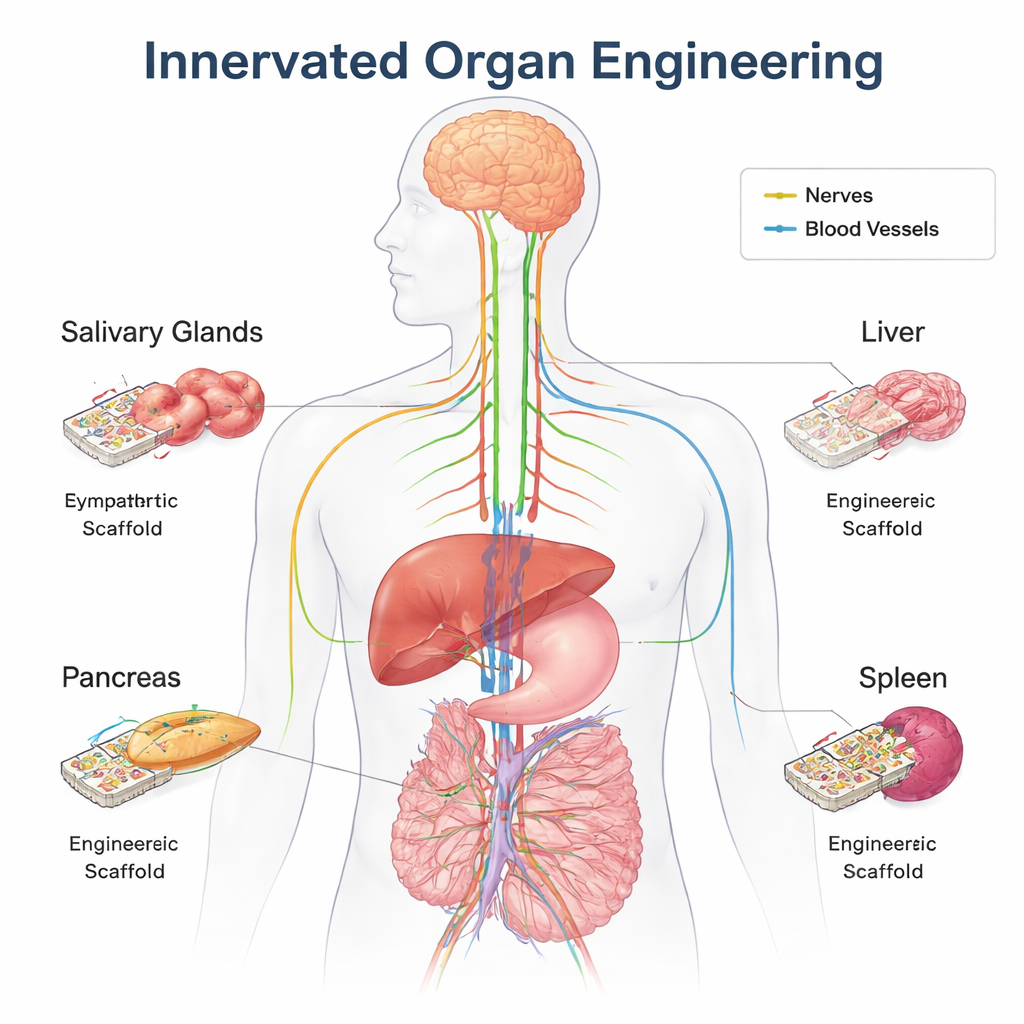
体の隠れた制御ネットワーク
主要な臓器はすべて、脳や脊髄と絶えず情報をやり取りする神経線維で張り巡らされています。自律神経系――“闘争か逃走か”と“休息と消化”の枝――を介して、これらの神経は血糖、消化、免疫応答、血流などを静かに調節します。アセチルコリンやノルエピネフリンといった化学的メッセージを送るだけでなく、伸展、温度、栄養レベルなどの変化を感知します。日常の制御に加えて、神経は胎生期の臓器形成を形づくり、創傷治癒を導き、組織を修復する幹細胞を支えます。多くの場所で、神経は血管と並んで成長し、類似した誘導シグナルを利用するため、配線(神経)と配管(血管)はともに発達します。
なぜ移植臓器は神経なしでも耐え得るのに、人工臓器はそうではないのか
従来の臓器移植では、元の神経をそのまま維持せずに移植されることが一般的です。移植された肝臓や腎臓は血流を通じてホルモンやその他のシグナルを受け取れるため機能し続け、時間とともに受容者側から新たな神経線維が成長してきます。その「猶予期間」は、ゼロから組み立てられた工学的臓器には存在しません。こうした構築物は通常、自然な臓器に見られる成熟した多様な細胞型や複雑な支持マトリックスの完全な組み合わせを欠いています。精密な神経接続は、膵臓、肝臓、唾液腺、脾臓のような多様な専門細胞を内包する臓器の協調に特に重要です。著者らは、ボトムアップの臓器工学――小さな構成要素から臓器を組み立てる手法――においては、事前に計画された神経支配をオプションではなく設計要件として扱うべきだと主張しています。
神経が形作る四つの主要臓器
総説は、神経がどのように四つの代表的臓器に影響を与えるかを詳述します。膵臓では交感神経と副交感神経の線維が発生過程でインスリン産生細胞群(ランゲルハンス島)の構造を形成し、成体では血糖の変動に応じてインスリンとグルカゴンの分泌を微調整します。唾液腺では、発生早期の副交感神経入力が上皮幹細胞の生存を維持し、最終的に唾液を分泌する分枝状導管の形成を導きます;これらの神経を誤った時期に切断すると正常な腺形成が阻害されます。肝臓の神経は血中の塩分、水分、糖、脂質濃度を感知し、代謝、血圧、損傷後の再生を調節します。脾臓では交感神経線維が免疫細胞と直接対話し、炎症を抑制または増強して感染やストレスへの応答を助けます。これらの臓器全体にわたり、神経の喪失や配線の誤りは糖尿病、消化不良、肝疾患、免疫機能障害と関連しています。
配線を組み込んだ臓器を作る
神経支配をバイオエンジニアリングされた臓器に導入するために、研究者たちは高度な3Dプリンティング、巧妙な足場設計、幹細胞由来の神経細胞を組み合わせています。押出型や光学ベースのバイオプリンティングは異なる細胞型や材料を精密なパターンに配置でき、特殊なハイドロゲルや高分子は長く分岐する神経線維を支持するように調整されます。既に、印刷された神経ネットワーク、神経—筋ユニット、現実的な電気活動を示す小型脳様組織が作られています。著者らは、膵臓、唾液腺、肝臓、脾臓の神経支配版を作るための実践的な設計図を示します:主要な臓器細胞を分離または誘導し、自律神経(交感神経と副交感神経)を適合するバイオインクに混ぜ、臓器形状にプリントし、移植前に神経が組織へ伸長できるようにバイオリアクターで成熟させる、という流れです。
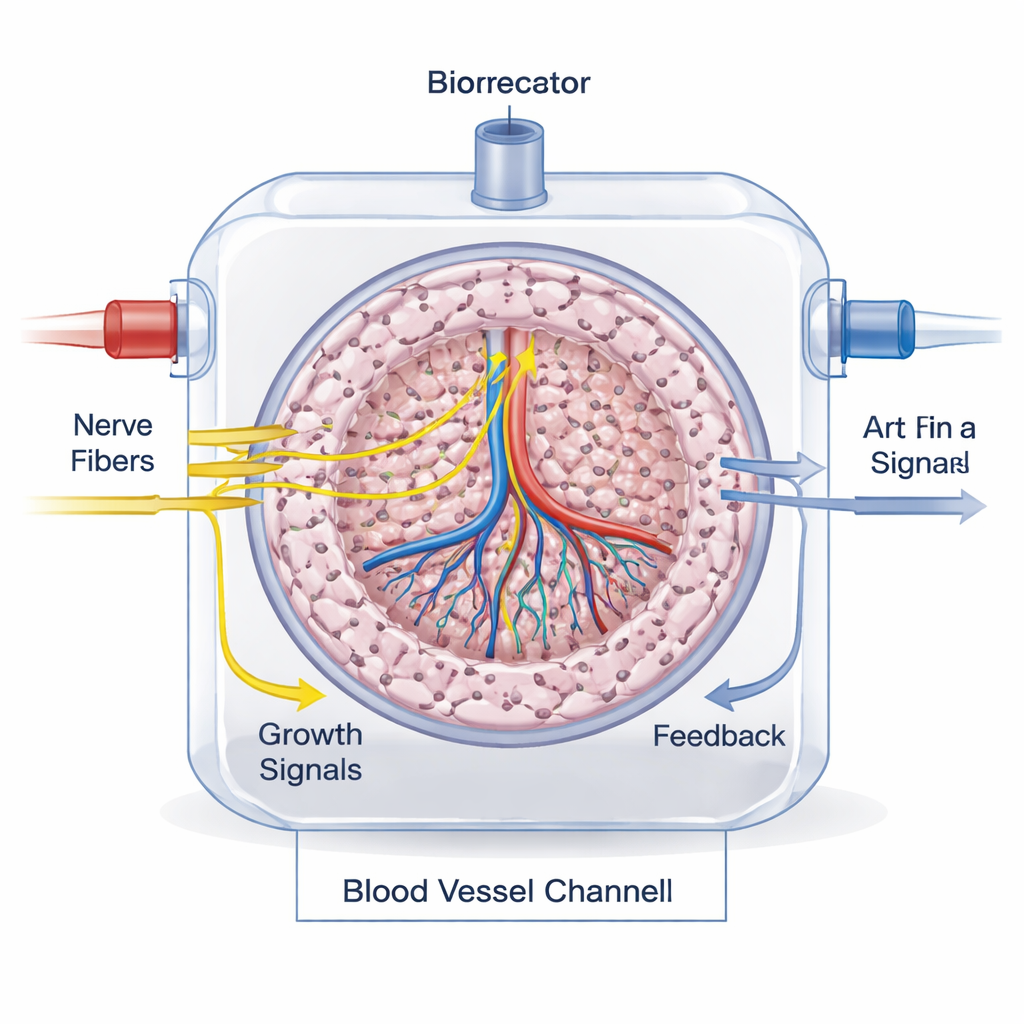
配線が機能しているかを測る
神経が本当に統合され機能しているかを確認することは大きな課題です。実験室では、研究者は神経特異的タンパク質を染色し、神経伝達物質を生化学的検査で測定し、生体イメージングで軸索の伸長や細胞の応答を観察します。マイクロフルイディクスの“臓器オンチップ”プラットフォームは現実的な血流や神経—臓器シグナル伝達のモデル化を助けます。動物実験や最終的には患者では、組織染色、神経トレーサー、そして交感神経または副交感神経線維を強調する特殊な放射性化合物を用いたMRI、CT、PETなどの現代的イメージング手法を組み合わせて神経支配を追跡できます。
概念から治療へ
記事は、神経は贅沢な付加機能ではなく、本当に機能する人工臓器にとって核心的要件であると結論づけます。有望な実験室レベルのデモから実用的な治療法へ移行するためには、複雑な神経ネットワークの大規模バイオプリンティングを改良し、細胞ソース(特にヒト幹細胞由来の自律神経ニューロン)を洗練させ、移植後の神経統合を監視する実用的な臨床イメージング手段を開発する必要があります。これらの障壁が克服されれば、次世代の工学臓器は失われた組織を置き換えるだけでなく、体の制御回路にシームレスに接続し、糖尿病、肝不全、ドライマウス(口腔乾燥)障害、免疫不全などに対してより信頼性が高く生体に近い治療を提供できる可能性があります。
引用: Das, S., Gordián-Vélez, W.J., Dave, J.R. et al. The nerve center of organ engineering. Nat Commun 16, 9834 (2025). https://doi.org/10.1038/s41467-025-64801-4
キーワード: 臓器工学, 神経支配, バイオファブリケーション, 3Dバイオプリンティング, 自律神経系