Clear Sky Science · ja
ホルマリン固定パラフィン包埋(FFPE)組織試料の光学的超解像組織学:課題と可能性
保存された組織試料からより多くを見出す
世界中の病院では、がんや腎障害などの病変を何年にもわたって調べられるように、患者の臓器の薄切片をワックスブロックに保管しています。本総説は、新しいタイプの光学顕微鏡がこれら日常的な試料を疾患を探る強力な窓に変え、従来の病院用顕微鏡では見えなかった微細構造を明らかにしている方法を説明します。これらの進展は、医師が病気をより早期に発見し、進行を理解し、治療をより正確に個別化するのに役立つ可能性があります。
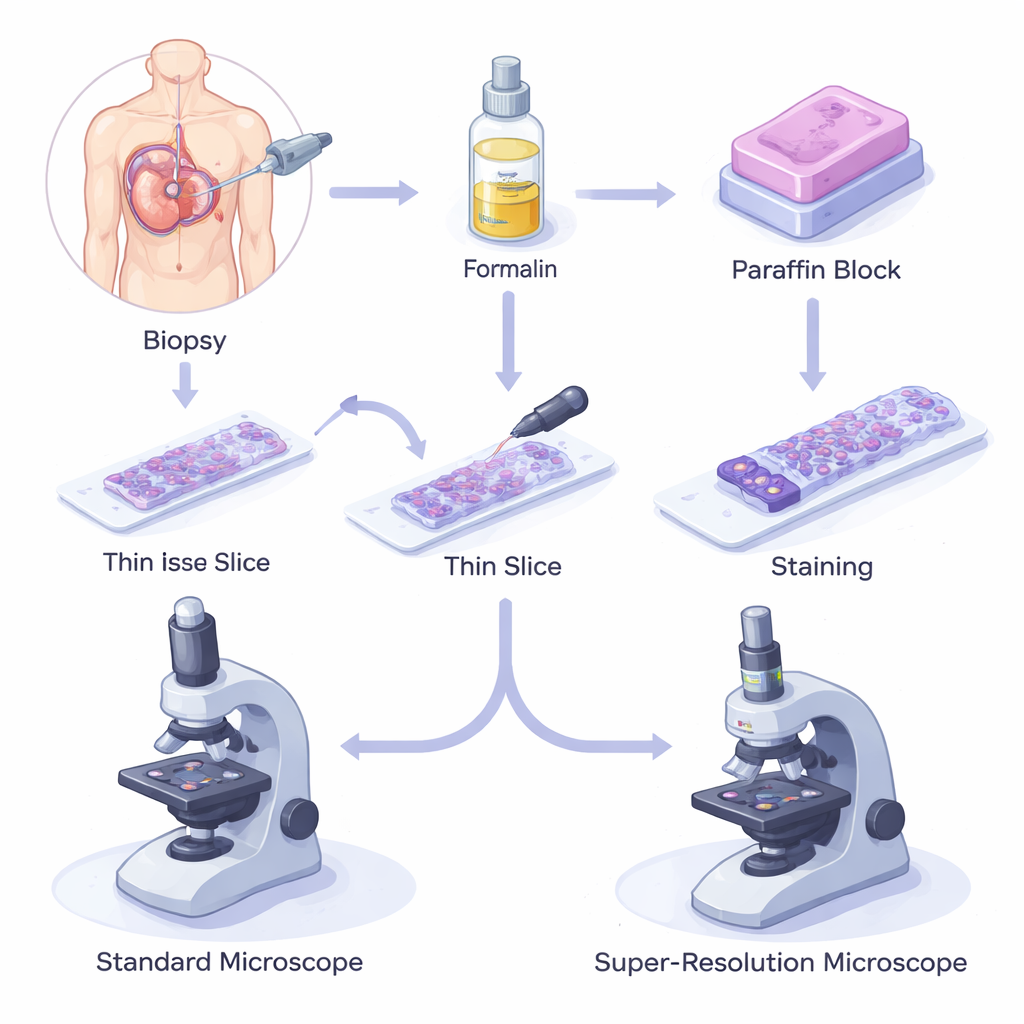
ワックス保存組織が現代医学を支える仕組み
生検では、患者から小さな組織片が採取され、腐敗を止めるためにホルマリンという薬剤で固定され、その後パラフィンワックスに埋め込まれます。ブロックは髪の毛のように薄く切られ、ガラススライドに載せられ、染色されて光学顕微鏡で観察されます。ホルマリン固定パラフィン包埋(FFPE)法は低コストで信頼性が高く、室温で数十年にわたって試料を保存できます。その結果、全世界のバイオバンクには何百万ものFFPE試料が蓄積されており、基礎生物学から高度な遺伝子・タンパク質研究に至るまでを支え、現代の診断と予後評価の基盤を形成しています。
従来の顕微鏡ではもう十分でない理由
従来の光学顕微鏡は光の物理に制約され、約250ナノメートルより小さい構造はぼやけてしまいます。腎臓の微細な濾過構造や神経細胞間の接続、核内のDNA構造の微小な変化など、多くの病気に関連する構造はこの限界より小さいため見落とされます。現在のワークフローでは、広い視野の概要把握に標準の光学顕微鏡を用い、ナノメートル単位の詳細には電子顕微鏡を併用することが多いですが、この方法は遅く高コストで、まったく別の試料調製を要します。したがって、研究者や臨床医は、既に使っている同じFFPE切片で大面積を迅速にスキャンしつつ、同時にナノスケールの特徴まで観察できる、単一で柔軟なシステムを求めています。
視界を鋭くする新しい手法
過去20年で、いくつかの「超解像」顕微鏡群が蛍光ラベルと巧妙な光学技術を用いて従来の解像度限界を破りました。単一分子局在法は分子をオン・オフさせて一つずつ位置を特定し、構造化照明は組織に縞模様の光を投影して計算で細部を復元し、誘導放出消光(STED)はドーナツ状のビームで極小の発光スポットを切り出し、ゆらぎに基づく手法は画像の微細な点滅を解析して構造を推定します。別の戦略である膨張顕微鏡は、ゲルで組織を物理的に膨張させることで複雑な光学系を避け、通常の顕微鏡でそれまで見えなかった詳細を観察可能にします。これらの方法はすでに乳房、結腸、膵臓、腎臓、脳、皮膚、胎盤などのFFPE試料に適用され、腫瘍でのミトコンドリアの変化、腎臓の濾過構造の破綻、アルツハイマー病でのタンパク質凝集の形成などを明らかにしています。
日常利用に向けた障壁
有望ではあるものの、これらの技術はまだ多くの病理検査室で日常的に使える段階には達していません。多くの超解像システムは遅く、視野が非常に狭いか、単一の高精細画像を構築するのに数万枚もの画像を必要とし、病理医が広範囲の組織を評価する上では現実的でありません。FFPE組織自体も光学的に扱いにくく、光を散乱し自然発光(バックグラウンド)を示し、標識すべき分子を覆い隠してしまうことがあり、これがぼやけた像や誤った構造の原因になります。ある方法は特殊な染料や専用のバッファー、多段階の化学処理を要求し、標準的な組織処理ワークフローに容易に組み込めないこともあります。加えて、市販機器は高価で操作が複雑、生成されるデータは大量の計算処理と保存容量を必要とします。
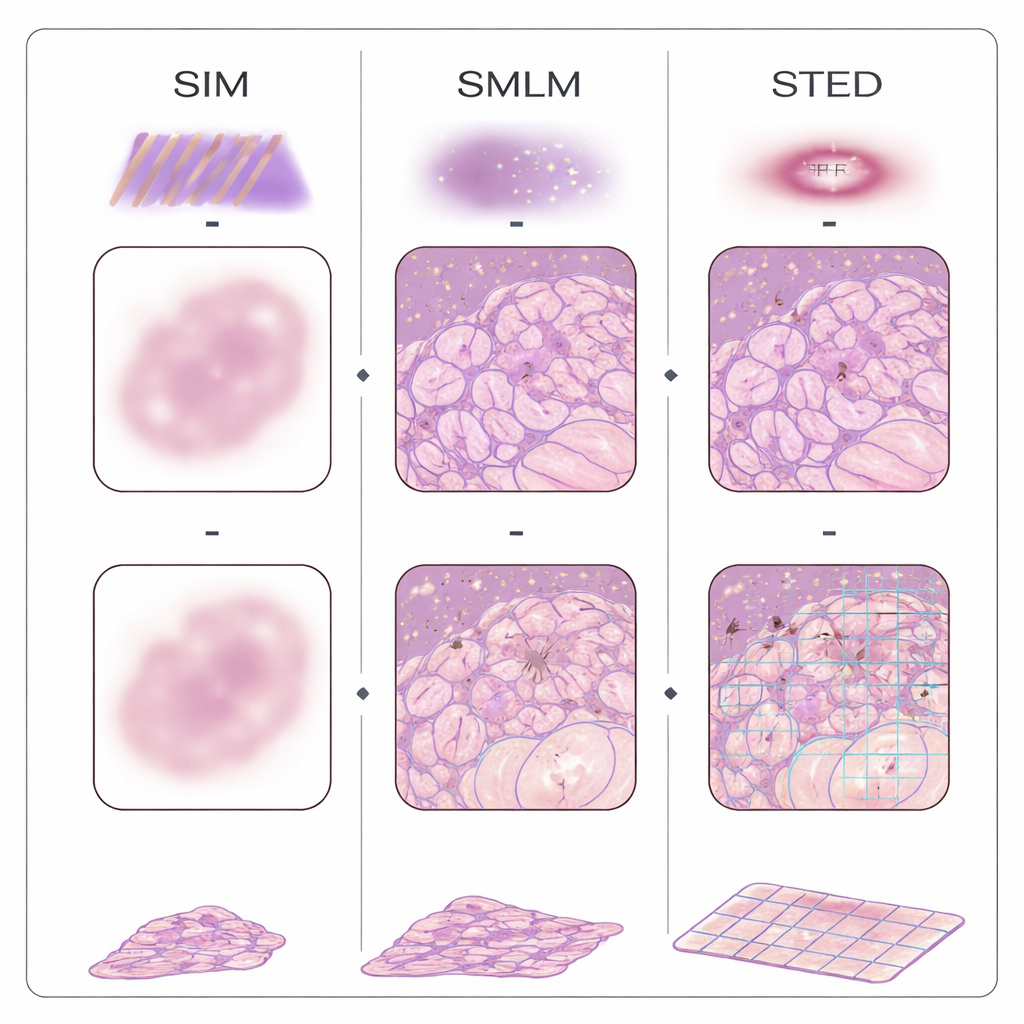
賢い光学と賢いソフトウェアの融合
これらの障害を克服するため、研究者たちは改良された光学系とラベルフリーイメージング、人工知能を組み合わせています。フーリエピティグラフィーや非線形光学顕微鏡のような高スループットで回折限界の手法は、大きくて無染色のFFPE切片でも迅速に走査し、組織構造の定量マップを提供できます。デジタル病理プラットフォームはスライド全体を高解像度で取得し、機械学習で腫瘍を検出したり、HER2、Ki-67、PD-L1のようなバイオマーカーをスコアリングしたりします。深層学習モデルは低解像度画像を超解像ビューに変換することさえ可能で、これにより一部の専用ハードウェアへの依存を減らし、既存の生検アーカイブをより有効活用できる可能性があります。
将来の患者にとっての意味
著者らは、ナノメートルスケールの詳細、高速性、妥当なコスト、そして現行の実験室ルーチンとの互換性を組み合わせた真の「FFPE超解像組織学」はまだ完全には実現していないが、達成可能な範囲にあると結論づけています。光学手法がより高速かつ堅牢になり、AIに基づく解析が成熟するにつれて、現在見逃されている組織の微妙な初期変化を明らかにし、診断精度を高め、より個別化された治療選択を導くツールとなり得ます。長期的には、保存されたすべてのワックスブロックを疾患の高精細地図に変えることが研究と臨床ケアの両方を変革する可能性があります。
引用: Villegas-Hernández, L.E., Dubey, V.K., Acharya, G. et al. Optical super-resolution histology of formalin-fixed paraffin-embedded tissue samples: challenges and opportunities. Nat Commun 16, 9760 (2025). https://doi.org/10.1038/s41467-025-64626-1
キーワード: 超解像顕微鏡, FFPE組織, デジタル病理学, 光学イメージング, がん診断