Clear Sky Science · ja
空間トランスクリプトミクスと組織形態の統合
組織を二つの方法でのぞく
医師や研究者は、組織でどの遺伝子が働いているかだけでなく、それらが正確にどこでオンになっているかを知りたいとますます考えています。並行して、病院の顕微鏡は日常的に病理医が利用する豊かな組織構造の画像を既にとらえています。本稿は、詳細な遺伝子活動マップと通常の顕微鏡画像という二つの見方を結びつけようとする新しい分野がどのようなものか、そしてその結合が早期診断の実現、がんのより良いグレーディング、病気の発生や拡がりに関するより深い洞察につながりうる理由を説明します。
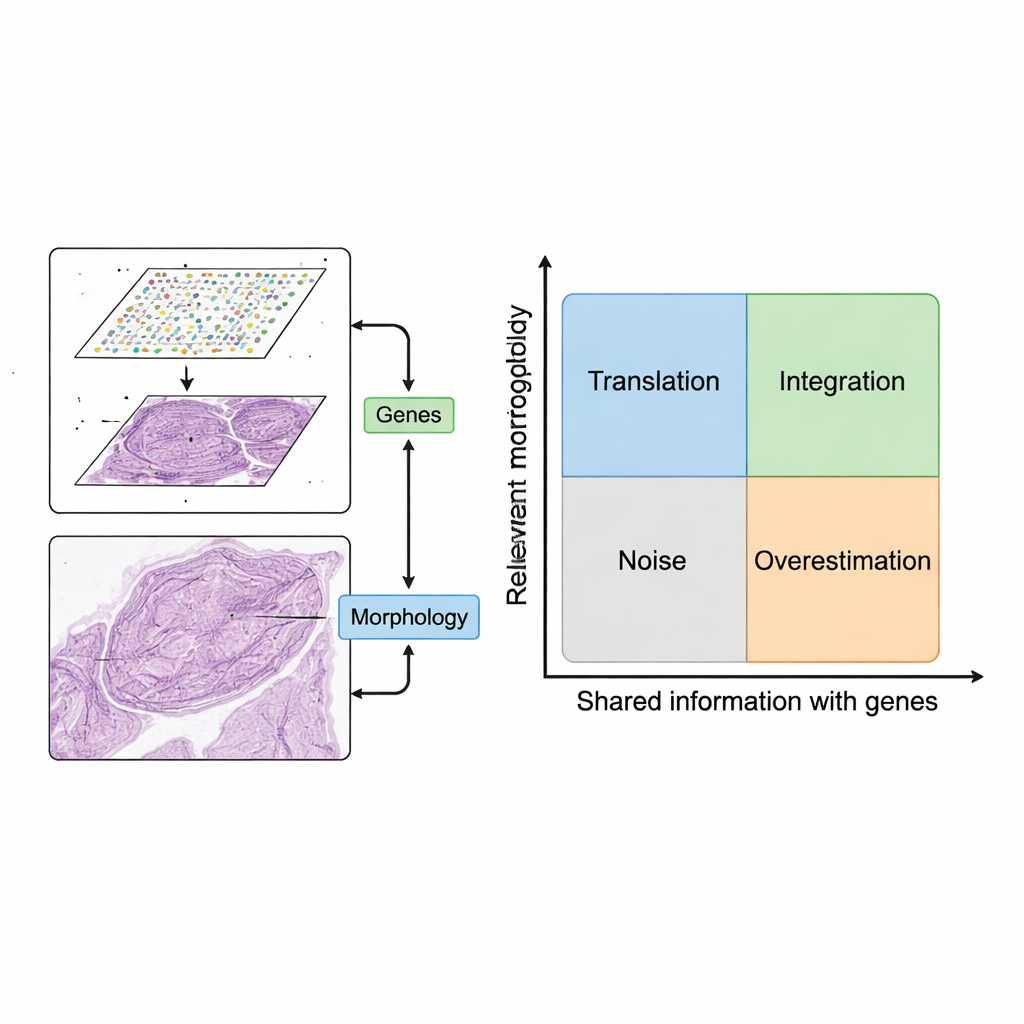
散在する細胞から遺伝子活動の地図へ
これまで強力な「オミクス」手法は組織を単一細胞の混合物に粉砕することを必要とし、それぞれの細胞がどこから来たかという位置情報を失わせてきました。空間トランスクリプトミクスは、各細胞の位置を保ったまま遺伝子活動を測定することでその状況を変えました。その結果、各スポットが遺伝子発現プロファイルと正確な座標を持つグリッドが得られます。この空間的な遺伝子データ自体は、すでに細胞の多様性や疾患の構造に関する新たなパターンを明らかにしています。しかし一度測定されるとそれは固定され、実験を繰り返すには高いコストがかかります。対照的に、広く用いられるヘマトキシリン・エオシン(H&E)などの標準染色で撮影された組織画像は安価で豊富にあり、細胞の形、密度、組織の配列に関する視覚的手がかりを含んでいます。
画像と遺伝子を結びつける二つの道
レビューは、これら二つのデータ源をともに利用するためのシンプルだが強力な枠組みを提案します。まず、画像パッチが近傍の遺伝子発現スポットと対応づけられます。次に、計算モデルが画像から形状、テクスチャ、配置といった特徴を抽出し、それを遺伝子発現のパターンと比較します。著者らは望ましい二つのシナリオを述べています。「翻訳(translation)」では、画像特徴が関連する遺伝子活動を密接に追跡するため、組織画像のみからどの遺伝子がオンかを予測できます。これは欠測した遺伝子測定値を補う、元のグリッドより細かい解像度を達成する、あるいは追加の実験を行わずに診療用スライドから遺伝子活動を推測するといった用途に使えます。「統合(integration)」では、画像特徴が遺伝子データでは捉えにくい緩やかな構造変化や微妙な組織配置など有用な情報を含み、組織内のより明確な領域や“ドメイン”の定義に寄与します。
追加情報が役立つとき、害になるとき
すべての画像特徴が利用に値するわけではありません。著者らは概念図を導入し、二つの軸で整理します:生物学的問いに対する画像特徴の関連性と、遺伝子情報との重なりの程度です。関連性も重なりもない特徴はノイズに過ぎず、例えば染色のアーティファクトがそれに当たります。遺伝子パターンを追うが臨床的意義の小さいハウスキーピング遺伝子に結びつく特徴は、論文上では良好に見えても臨床価値をほとんど追加しません。方法を「翻訳」「統合」「ノイズ」「過大評価」の四象限に整理することで、画像と遺伝子を組み合わせることが真の洞察をもたらす場合と、既知の情報を単に繰り返したり覆い隠したりする場合とを明確にします。
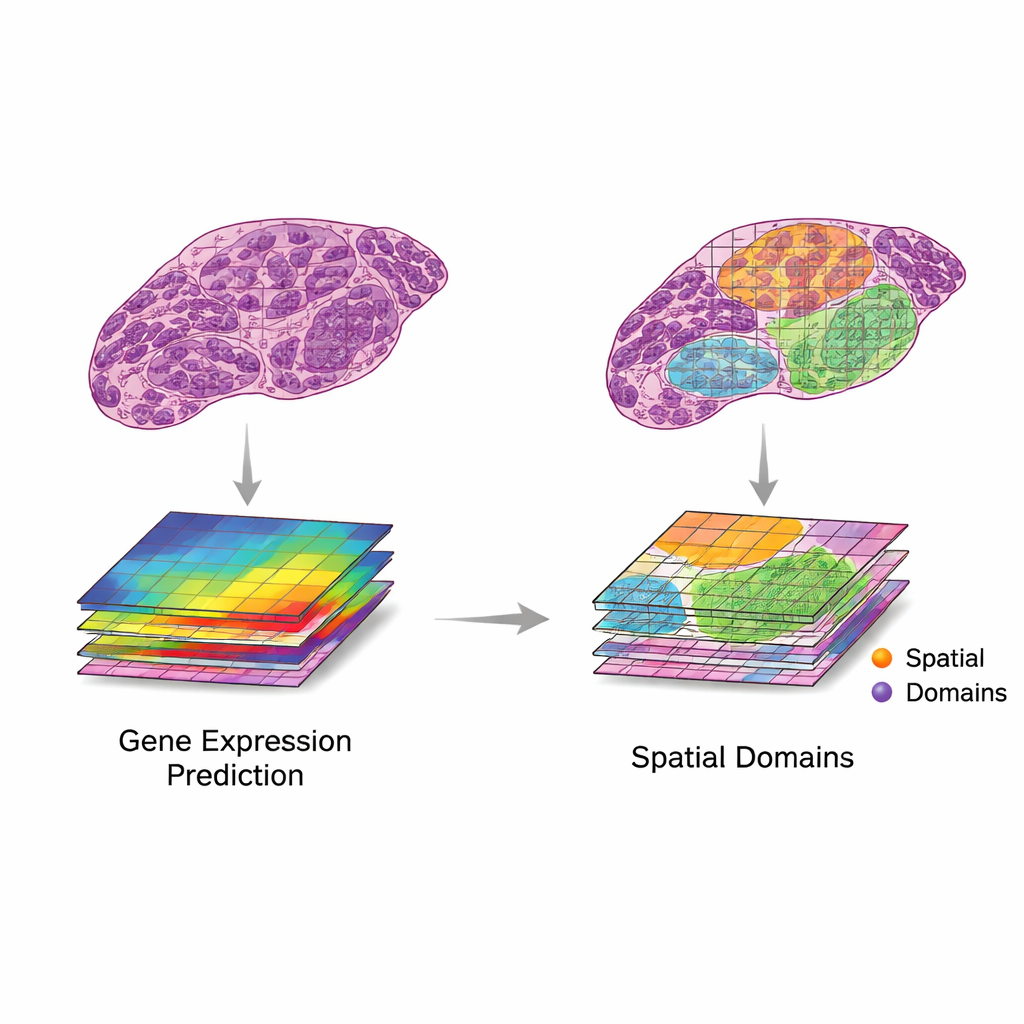
現行ツール、評価、そして成長の痛み
現在、翻訳と統合を現実データ上で実行しようとするAI手法が急速に進展しています。初期のシステムは畳み込みニューラルネットワークに依存していましたが、最近はトランスフォーマー、グラフニューラルネットワーク、多段階のマルチスケールモデルが採用され、小さな細胞構造からスライド全体の文脈までを取り込めるようになっています。これらの手法はH&E画像から遺伝子活動を予測したり、超解像マップを生成したり、異なる挙動を示す組織領域の同定を支援したりするために使われてきました。性能評価には、予測値と観測値の相関や、AI定義の領域と専門病理医のラベルとの一致といった統計指標が用いられます。しかし、データセットはまだ小規模かつ多様で、研究間の比較は困難です。報告される多くの改善は過学習を反映している可能性や、臨床では重要性の低い遺伝子やパターンでの成功にすぎない場合があります。
ここから何が生まれるか
著者らは、空間的な遺伝子マップと組織画像を組み合わせることは有望だがまだ初期段階の取り組みだと結論づけています。現行モデルはしばしば中程度の精度にとどまり、日常的な医療利用に備えるにはまだ十分ではありません。今後の進展は、特に数百万枚の病理スライドで訓練された大型の“ファウンデーションモデル”のようなより優れた画像特徴から、また患者ケアに実際に影響する遺伝子やパターンに焦点を当てることからもたらされると考えられます。慎重に設計された統合は、組織が現在示している見た目と遺伝子が予測する将来との不一致を検出することで、病気の早期警告を明らかにする可能性があります。要するに、この研究は日常的な顕微鏡画像を遺伝子情報で豊かにした地図に変え、医師が病気をより正確に理解し治療する手助けをするためのロードマップを示しています。
引用: Chelebian, E., Avenel, C. & Wählby, C. Combining spatial transcriptomics with tissue morphology. Nat Commun 16, 4452 (2025). https://doi.org/10.1038/s41467-025-58989-8
キーワード: 空間トランスクリプトミクス, 組織形態, デジタル病理学, 遺伝子発現予測, 画像解析AI