Clear Sky Science · ja
信頼でき完全な薬用植物ゲノムへの長い道のり
植物のDNA地図が人の健康にとって重要な理由
現在の最も強力な薬の多く—パクリタキセルのような抗がん薬からモルヒネのような鎮痛剤、そして抗マラリア薬アルテミシニンに至るまで—は植物に由来しています。それでも、多くの薬用植物については、研究者はDNAの完全な「取扱説明書」をまだ持っていません。このレビューは、新しいゲノム技術がこれらの説明書を読む能力をどのように変えつつあるか、なぜ現在の植物ゲノムがしばしば不完全または欠陥を抱えているか、そして真に正確なゲノムがより良い薬剤、持続可能な生産、および価値ある種の保全をどのように切り開く可能性があるかを説明します。
薬用植物の設計図を読むことの約束
何千年にもわたり、人々は植物療法に頼ってきましたし、現代薬理学も植物由来の天然物に大きく依存しています。アルカロイド、テルペノイド、フェノール化合物などのこれらの特化した分子は、植物DNAにコードされた複雑な代謝経路を通じて作られます。ごく最近まで、研究者は同位体トレーシングや一遺伝子ずつのクローニングのような遅く手間のかかる手法でこれらの経路を組み立てる必要がありました。手頃な価格で高スループットのDNAシーケンシングの登場が状況を一変させました。2025年2月までに、431件の薬用植物(203種に相当)のゲノムが解析され、研究者は経路遺伝子を体系的に探索し、有用な化合物がどのように制御されるかを理解し、これらの化学がどのように進化したかを調べるための手段を得ました。
シーケンスの急増、しかし多くは不完全なゲノム
PacBioやOxford Nanoporeのロングリードシーケンシング技術は、短リードのIlluminaデータやHi‑Cのような染色体レベルのマッピング手法と組み合わせることで、植物ゲノムの品質を劇的に向上させました。薬用植物のアセンブリのほぼ半数が過去3年だけで公開されており、最近の多くのゲノムは染色体スケールで構築されています。しかし、本レビューは量が質を上回ってきたことを示しています。ゲノムの半数以上が初期バージョンのままで、多くはドラフトレベルに留まり、染色体中心部や他の反復領域を完全に捕捉した「テロメアからテロメア」(T2T)のギャップのないアセンブリを持つ薬用植物はわずか11種に過ぎません。N50(連続性の指標)やBUSCOスコア(保存遺伝子の指標)のような標準的な指標は全体としては良好に見えるものの、重要な生合成遺伝子が存在する正確な箇所での決定的なギャップを覆い隠してしまうことがあります。
薬の遺伝子があるはずの場所に隠れたギャップ
現在のゲノムがどれほど実用的かを検証するため、著者らは9種のよく研究された薬用植物における既知で実験的に検証された経路遺伝子を調べました。染色体レベルのアセンブリでさえ、例えば人参のジンセノシドやキク科のArtemisia annuaにおけるアルテミシニンのような化合物の重要な酵素が完全に欠落しているか、部分的にしか捕捉されていない場合がありました。場合によっては、遺伝子自体は生のゲノム配列には存在するが、公式の遺伝子注釈では欠落または切断されていて見つけにくいこともありました。顕著な例として、クマリンを産生するハーブPeucedanum praeruptorumがあります。古い染色体レベルのゲノムは1つの重要な遺伝子を壊し、他の2つを見逃していましたが、より新しいT2Tアセンブリではこれらの遺伝子が回復され、いくつかが密に並んだ生合成遺伝子クラスターとして一緒に存在することが明らかになりました。こうしたクラスターの地図こそが、研究者が薬をより効率的に生産するために植物や微生物を設計する際に必要とするものです。
植物ゲノムの組み立てが難しい理由
薬用植物は、多くの作物種が抱える課題を超えた特殊な困難を呈します。それらのゲノムはしばしば高いヘテロ接合性(各染色体の2つのコピー間の多くのDNA差異)、頻繁な多倍性(複数の染色体セット)、および大量の反復DNAを含み、これらはアセンブリアルゴリズムを混乱させ、断片化や誤結合を引き起こします。解析された薬用植物の約3分の1はゲノム中の反復配列が70%を超え、4分の1以上が非常に高いヘテロ接合性を示します。高度に近交系の系統を作出したり単相組織を分離したりすることは有効ですが、多くの種でそれは遅く、高価で、生物学的に困難です。各親由来ハプロタイプを別々に組み立てる新しい戦略や、反復が多く多倍性を持つゲノムに調整されたより強力なアルゴリズムがこれらの障壁を和らげ始めていますが、まだ一般的には行われていません。
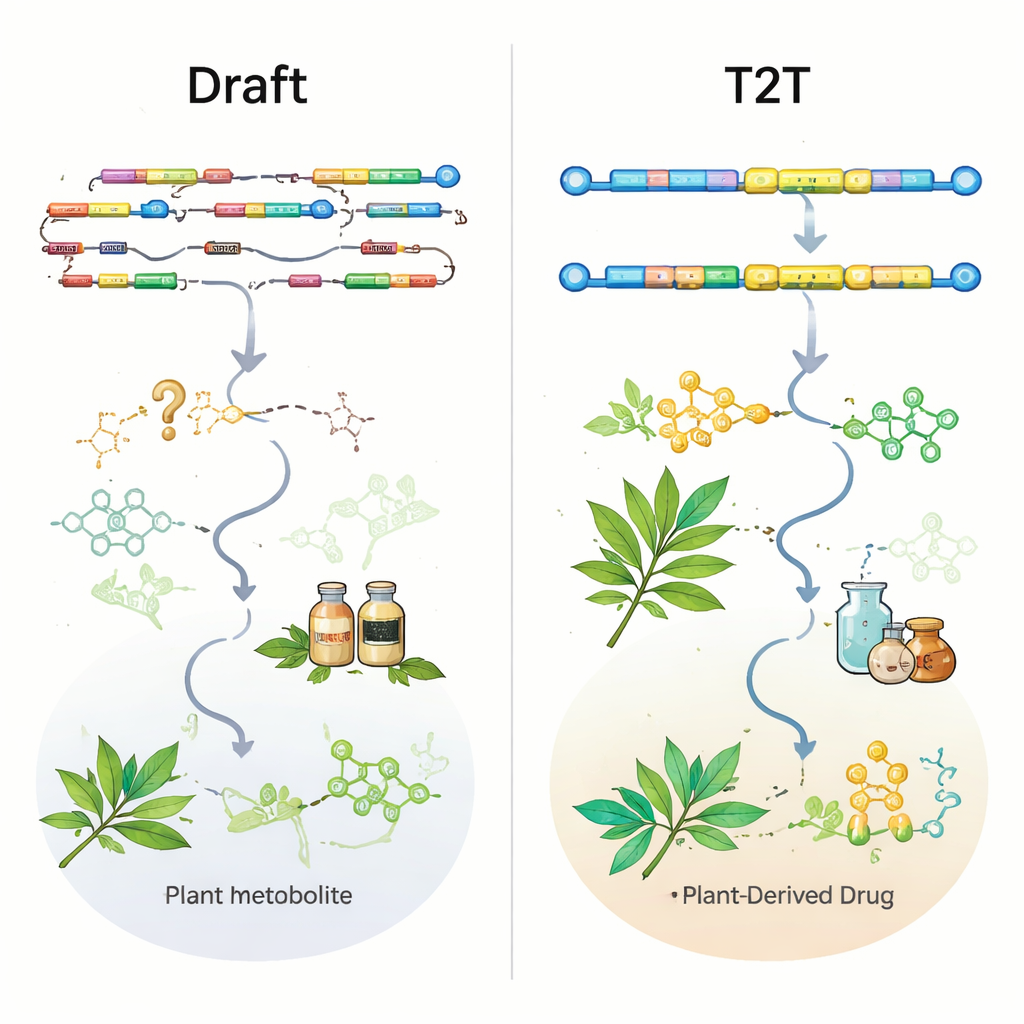
ゲノムから新薬へ——今後の方向性
ゲノムが十分に整備されれば、それは発見の強力な原動力になります。研究者は全ゲノムデータをトランスクリプトミクス、メタボロミクス、合成生物学と組み合わせて、高付加価値化合物の生産を制御する酵素、調節遺伝子、および生合成遺伝子クラスターを特定できます。これらの知見はすでにビンブラスチンやパクリタキセルなど、複雑な植物経路を酵母やモデル植物で再構築することを可能にし、安定した大規模なバイオ製造への道を開いています。将来を見据え、著者らは「種ごとに粗いゲノムを一つ」という発想から、個体内多様性を捉える複数の高品質なT2Tおよびハプロタイプ解決アセンブリへの転換を提案しています。これは作物研究でのパングノムに似ています。これらの参照ゲノムを大規模な再シーケンス、高度なフェノタイピング、そして新興の単一細胞・空間トランスクリプトミクスと結び付けることで、環境、細胞型、遺伝子ネットワークが薬用化学をどのように形作るかが明らかになるでしょう。
患者と地球にとっての意味
レビューの中心的なメッセージは、信頼できる完全な薬用植物ゲノムは贅沢ではなく、何世紀にもわたるハーブの知識を精密な現代療法へ変える基盤であるということです。より良いゲノムにより、研究者は薬の経路における欠落したステップを見つけ、重要な医薬品のより安全で豊富な供給を設計し、同じ化合物を生産できる代替種を特定できるようになります。また、ほとんどがまだゲノム資源を持たない脅かされた薬用植物の保全と持続可能な利用の指針ともなります。要するに、これらのゲノムを正確に地図化する作業を完遂すれば、創薬のスピードを上げ、供給網を安定させ、植物の多様性を保全することができ、それらは最終的に人間の健康に利益をもたらします。
引用: Cheng, LT., Wang, ZL., Zhu, QH. et al. A long road ahead to reliable and complete medicinal plant genomes. Nat Commun 16, 2150 (2025). https://doi.org/10.1038/s41467-025-57448-8
キーワード: 薬用植物ゲノミクス, 二次代謝遺伝子クラスター, テロメアからテロメアまでのゲノム, 天然物の生合成, 合成生物学