Clear Sky Science · ja
N末端アセチル化の影響を照らす:タンパク質から生理学へ
微小な化学タグがタンパク質の振る舞いを変える仕組み
体内のあらゆる細胞は、正しく折り畳まれ、適切な場所へ輸送され、分子機械として組み立てられ、損傷したら除去される必要がある多数のタンパク質で満たされています。本レビューは、多くのタンパク質の一端で起こる微妙だが極めて広範な化学変化――N末端アセチル化と呼ばれる――を取り上げ、この小さな“キャップ”が細胞増殖やストレス応答から心臓の発生や脳機能に至るまで、さまざまな過程をどのように制御するかを明らかにします。
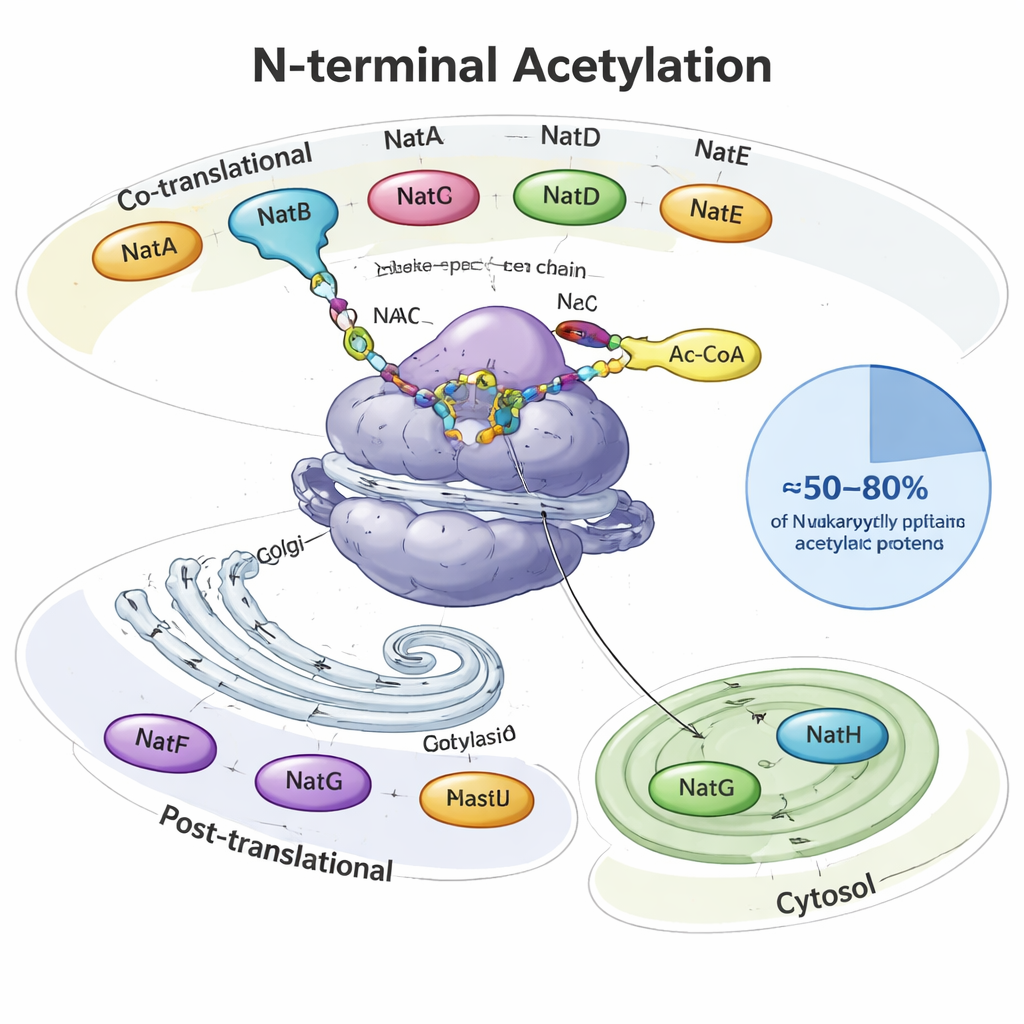
ほとんどの人が知らないタンパク質のキャップ
タンパク質が合成されるとき、それはリボソームという細胞の工場から伸びる糸のように現れます。その先端、N末端では多くの真核生物のタンパク質にアセチル基という炭素2つからなる小さなキャップが付加されます。この仕事を行うのはN末端アセチルトランスフェラーゼ(NAT)と呼ばれる特殊な酵素群で、供与体として一般的な代謝分子であるアセチル-CoAを用います。酵母、植物、動物では主に8種類のNAT(NatA–NatH)が役割を分担します。あるものはタンパク質が合成されている最中に働き、他は合成後に働いてゴルジ体や植物のプラスチドのような特定の局在に配置されています。これらは合わせて細胞内タンパク質の約半分から4分の5を修飾し、各NATは2〜4残基の開始配列を好んで識別します。
多様な酵素、それぞれの専門性
NatA、NatB、NatCは主要な働き手であり、リボソームに結合して「N末端アセチローム」の広範囲を担います。ヒトではNatAだけで約40%のタンパク質を修飾でき、通常は最初のメチオニンが切除されたタンパク質が標的です。NatBとNatCは最初のメチオニンを保持するタンパク質に作用しますが、隣接するアミノ酸残基の好みが異なります。他のNATはより選択的で、NatDはDNAを包装するごく限られたヒストンに焦点を当て、NatFはゴルジでの膜貫通タンパク質を標的にし、NatGは植物プラスチド内で働き、NatH(NAA80)は細胞骨格の主要成分であるアクチンの特殊な二段階成熟過程を完了させます。構造学的および生化学的研究を総覧すると、補助サブユニットがこれらの酵素をリボソームや膜に固定し、どのタンパク質に作用するかを微調整していることが示されています。
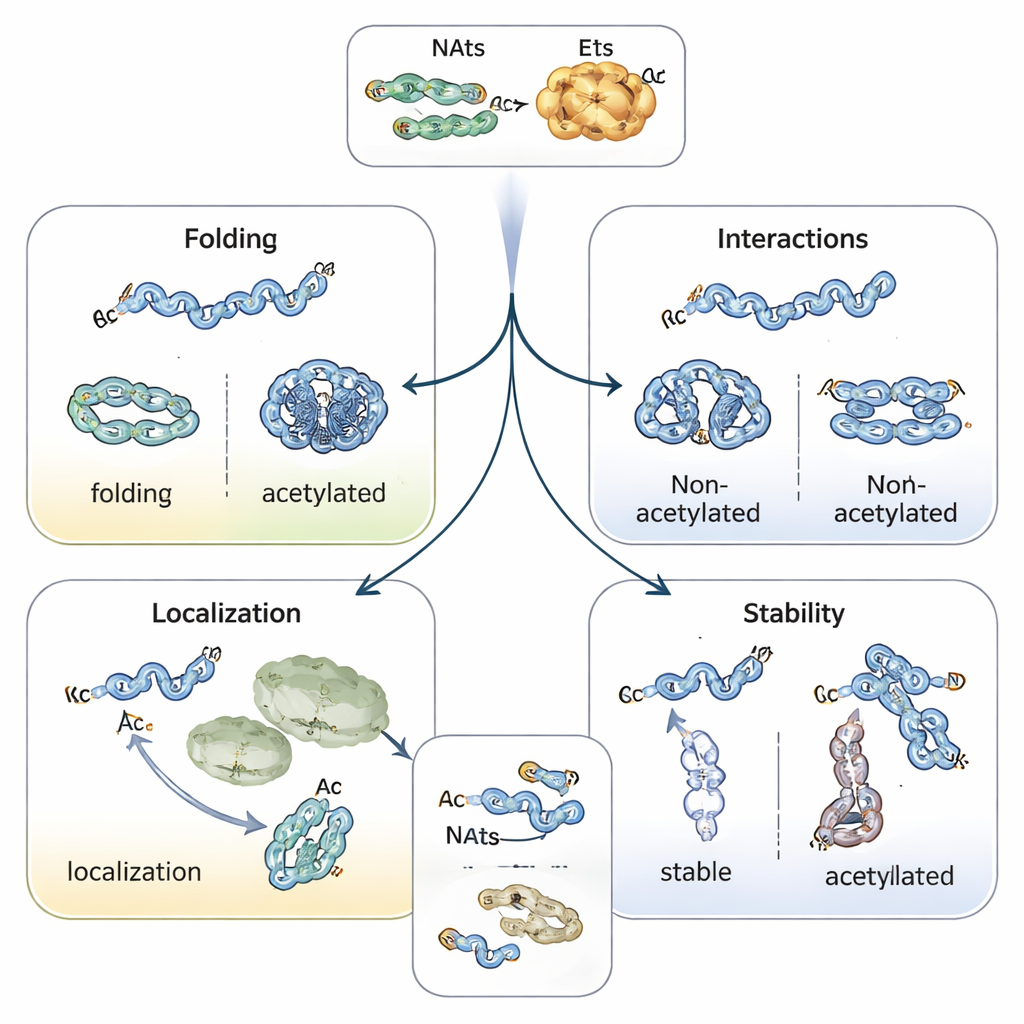
タンパク質の折り畳み、局在、寿命の制御
アセチルキャップの付加はタンパク質の先端の化学的性質を変え、多くの場合ヘリックス構造を安定化させ、折り畳み方に影響を与えます。例えば、パーキンソン病に関連するα-シヌクレインはN末端がアセチル化されると凝集しにくくなり、安全な構造を取りやすくなります。アクチンのパートナーであるトロポミオシンは、適切にアセチル化されているとアクチンフィラメントに結合してその調節をよりよく行えます。植物や動物では、N末端アセチル化が一種の住所ラベルとして働き、タンパク質が葉緑体、リソソーム、ゴルジなどに到達するのを助けることがあります。最も注目すべきは、タンパク質の寿命を決める役割です。保護されていないN末端はユビキチン付加酵素により「分解シグナル」として読まれることがあり、アセチル化はそのシグナルを覆いタンパク質を安定化するか、場合によっては誤折り畳みや不適切な複合体形成時にのみ認識される条件付きのタグを作り出します。
細胞生理から発生、疾患へ
N末端アセチル化は非常に多くのタンパク質に関与するため、NATの破綻は生物全体に広範な影響を及ぼします。モデル生物でNatA、NatB、NatCを除去すると、重篤な発生異常、ストレス応答の変化、場合によっては致死性を引き起こすことがあり、NatFやNatHのようなより専門的な酵素の欠損は脳の石灰化や難聴といったより限定的な問題を生じます。ヒトでは複数のNAT遺伝子の遺伝性変異が、知的障害、心奇形、筋力低下を伴う希少な神経発達症候群の基盤となっています。同じ機構はがんでも過剰に働いていることが多く、NATのレベル上昇は予後不良と相関し、腫瘍成長、転移、治療抵抗性を促進する可能性があります。N末端アセチル化の変化はα-シヌクレインやハンチンチンのような凝集しやすいタンパク質にも影響を与え、この修飾を神経変性疾患の機序に結びつけます。
今後の方向性と医療的可能性
著者らは、これらのN末端キャップを付加する主要な酵素の多くは特定されているものの、個々の標的タンパク質と制御ルールの理解はまだ一部にすぎないと結論付けています。重要なテーマは、タンパク質の先端でのアセチル化がしばしば早すぎる分解から保護する一方で、品質管理のための文脈依存的なシグナルをも作り出すという点です。どのユビキチンリガーゼがどのN末端パターンを読み取るか、そしてこれらのキャップを除去できる酵素が存在するかを特定することが主要な未解決の課題です。NATはタンパク質安定性、遺伝子調節、細胞ストレス応答の交差点に位置するため、選択的なNAT阻害剤――あるいは将来的に特定の疾患関連タンパク質のN末端アセチル化を調節するツール――は、がん、心疾患、神経変性に対する新しい治療法の有望な道となる可能性があります。
引用: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
キーワード: タンパク質修飾, N末端アセチル化, タンパク質品質管理, 神経変性疾患, がん生物学