Clear Sky Science · ja
CRISPR-AuNP: HSPCにおけるコスト効率が高くモジュール化可能な非ウイルス性遺伝子編集のための金ナノ粒子プラットフォームの物理化学的最適化
より多くの患者に遺伝子編集を届ける
CRISPRのような遺伝子編集ツールは、すでに遺伝性血液疾患の患者の生活を変えつつありますが、治療は依然として高価で技術的に難しく、限られた専門施設に限定されがちです。本論文は、ラボのベンチで数時間で調製できる小さな金ベースの粒子を用いて、血液形成幹細胞にCRISPRを届ける新しい方法を述べています。目的は強力な遺伝子編集アプローチをより単純に、安価に、そして世界のより多くの場所で導入しやすくすることです。
なぜ血液幹細胞が重要か
造血幹・前駆細胞は骨髄に存在し、体内のさまざまな血球を継続的に補充します。これらの細胞の病因変異を安全に修正できれば、一回限りの治療で鎌状赤血球症や特定の免疫不全症などの疾患に一生続く治癒をもたらす可能性があります。現在、これらの細胞にCRISPRを導入する最も一般的な方法はエレクトロポレーションであり、これは細胞膜に穴を開けるために電気パルスを用います。強力ですがエレクトロポレーションは細胞に負担が大きく、高価な装置や特殊な試薬を必要とし、資源の限られた環境では拡張や輸出が容易ではありません。より安全なウイルスベクターは多くの遺伝子療法に優れていますが、編集ツールを長期間産生し続けるため、オフターゲット変化のリスクが高まり、CRISPR導入には必ずしも適していません。
小さな金のデリバリー車の構築
研究者らは、CRISPR成分を表面に載せた以前に報告された金ナノ粒子システムを改善することを目指しました。従来の設計では、CRISPRの標的へ切断タンパク質を導くガイドRNAが金コアに直接固定され、その後Cas9タンパク質と組み合わされていました。この方式はある種のCRISPR酵素ではまずまず機能しましたが、多くの治療戦略の中心となるCas9では性能が劣りました。粒子組立時に用いる酸性条件下でCas9とそのガイドRNAがどのように振る舞うかを詳細に検討したところ、ガイドRNA二本鎖が金表面で不安定になり、粒子にほとんどあるいは全く能動的なCas9が結合しないことが判明しました。共焦点顕微鏡でも、細胞内区画からの脱出を助けるはずのポリマーコーティングが本来の働きをする前に剥がれてしまうことが示唆されました。
プラットフォームの段階的再設計
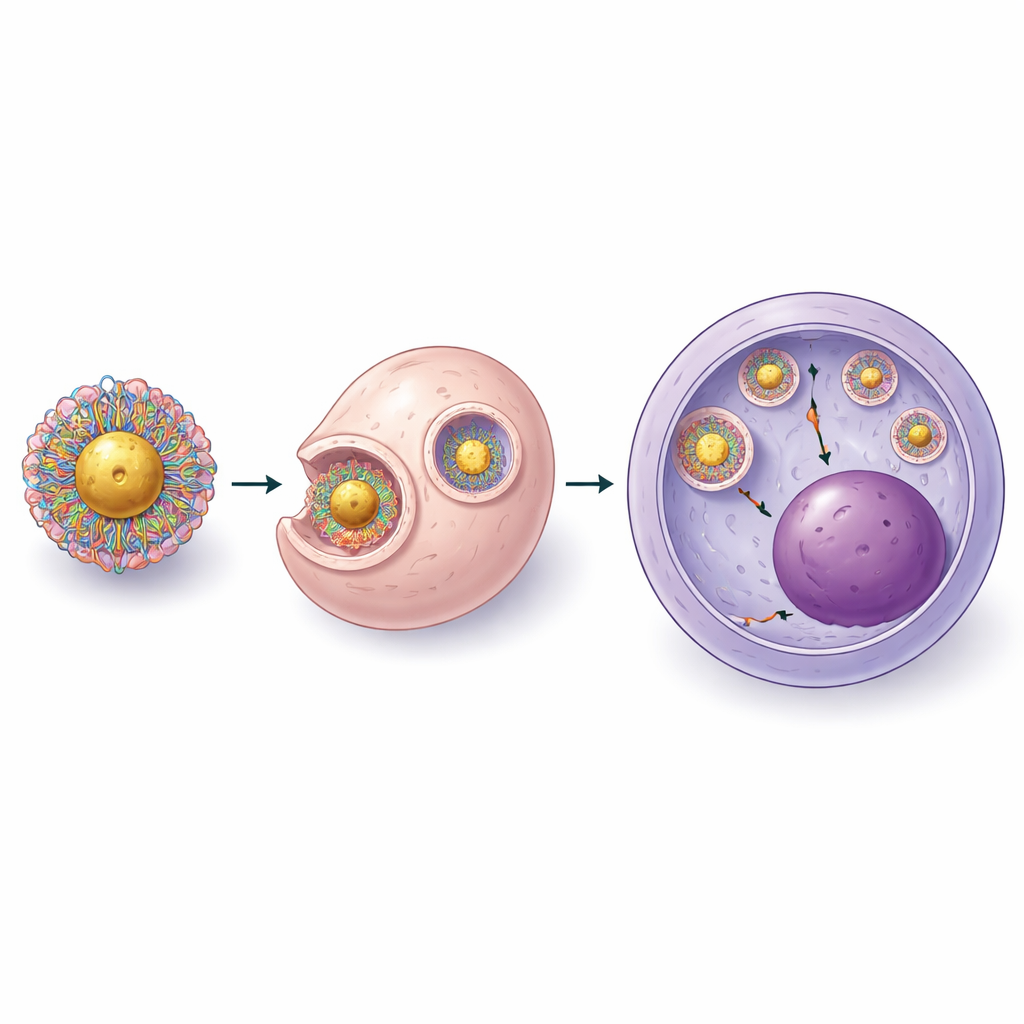
これらの問題を克服するため、研究チームはシステムを根本から三段階で作り直しました。まず、裸のRNAを金に固定してからタンパク質を加える代わりに、タンパク質とガイドRNAを含む完全なCRISPRリボヌクレオタンパク(RNP)複合体を先に形成してから金表面と接触させました。やや酸性の条件を見極めることで、これらの複合体が粒子に結合しつつ切断タンパク質の活性を保持できることを確認しました。次に、陽イオン性の鎖(細胞内区画からの脱出に必要)と、凝集を防ぐ親水性のポリエチレングリコール(PEG)セグメントを組み合わせた特別に設計されたポリマーでロードした粒子を被覆しました。サイズ、表面電荷、タンパク質含有量を測定することで、溶液中での安定性を保ちながら粒子当たり数十個のCRISPR複合体を再現性よく積載できることを示しました。
細胞の防御を突破する
より良い積載が実現しても、第2世代の粒子は依然として重要な障害に直面しました:CRISPRを細胞内の膜小胞(エンドソーム)から脱出させ、DNAが存在する細胞核へ到達させることです。そこでチームはポリマー層の化学組成とポリマー中の正電荷とCRISPR複合体の負電荷の比率を系統的に調整しました。短いPEG鎖を増やし、制御された数の硫黄含有アンカーを追加することで、粒子の安定性とエンドソーム膜を破壊する能力が向上し、細胞を損なうことなく有効性を高められることを発見しました。最終的な第3世代設計では、まずCRISPRとポリマーのコンパクトな複合体を作成し、それを濃縮した金コアに結合させました。電子顕微鏡は各金球の周りに薄いCRISPR・ポリマーの殻を示し、生きた幹細胞でのイメージングは貨物が細胞内に脱出して核に到達できることを確認しました。
複数のCRISPRツールにわたる編集結果
最適化した粒子の性能を評価するため、研究者らはほぼすべての血球の表面に存在し、フローサイトメトリーで容易に測定できるβ2-ミクログロブリンという遺伝子を標的にしました。第3世代の金プラットフォームを使用して、ヒト一次造血幹・前駆細胞でこの遺伝子の精確な破壊を10%以上達成しました。これは多くの治療用途で意味あるレベルと考えられ、かつ高い細胞生存率を維持しました。効率はエレクトロポレーションで得られる最高値より低いものの、金粒子システムは特殊装置を必要とせず、細胞への負担も最小限でした。重要なのは、同じプラットフォームがCas9、Cas12a、および新しい酵素Cas12a-M29-1を含む異なるCRISPRタンパク質でも同様の編集レベルと検出可能な毒性の欠如を示し、設計のモジュール性を強調した点です。
将来の治療にとっての意義
簡潔に言えば、この研究は、電気やウイルスを用いずに精巧に設計された小さな金ベースのキャリアが、感受性の高い造血幹細胞にCRISPRツールを届けられることを示しています。市販の材料を用いて100万細胞あたり70ドル未満でベンチ上で組み立て可能である点も重要です。今日の臨床最良法の効率に匹敵させるにはさらなる改良が必要であり、特に非常に高い割合の修復細胞が要求される疾患では課題が残りますが、このベンチで組み立てられるプラットフォームは高度な遺伝子編集を行うための実務上の障壁を下げます。追加の改良と安全性評価が進めば、こうしたナノ粒子は専門施設に限られた恩恵を超えてCRISPRベース療法の普及を助け、世界中の患者に治癒的治療をより実現しやすくする可能性があります。
引用: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
キーワード: CRISPR遺伝子編集, 金ナノ粒子, 造血幹細胞, 非ウイルス性デリバリー, ナノ医療