Clear Sky Science · ja
CmTSAスーパープレックス技術を用いた保存臨床検体のTME(腫瘍微小環境)構造を同定するための統合空間プロファイリングパイプライン
腫瘍の周囲にある見えない景観が重要な理由
がんは孤立して成長するわけではありません。免疫細胞や支持細胞、血管、瘢痕様の結合組織といった要素が取り囲み、総体として腫瘍の「微小環境」を形成しています。本論文は、病院で通常に採取・保存された組織検体を用いてその隠れた景観を詳細にマップする実用的な方法を示します。どの種類の細胞が互いに隣接しているか、そしてそれらが有益な近隣を形成しているのか有害な近隣を形成しているのかを明らかにすることで、この手法は患者のがんの挙動やどの治療が有効である可能性が高いかをよりよく予測するのに役立つ可能性があります。
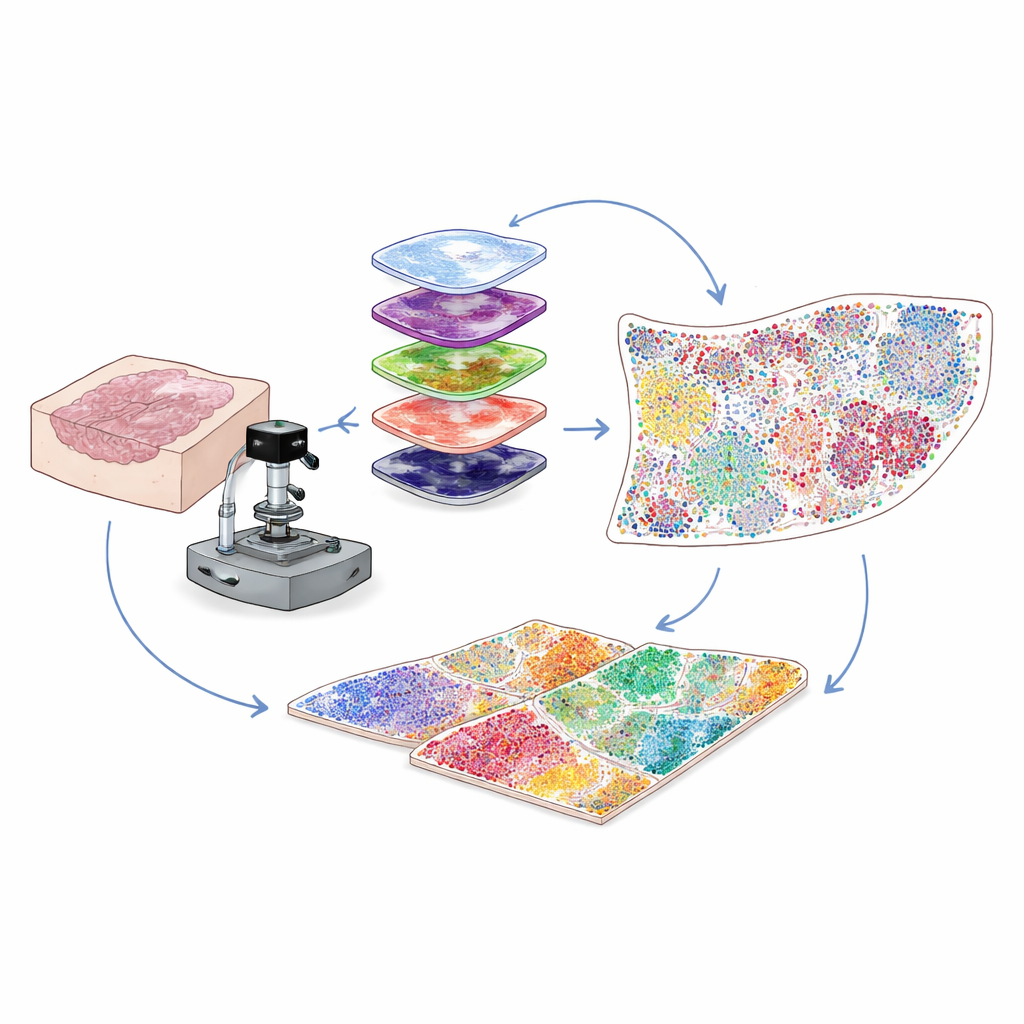
日常的な病院検体でより多くを可視化する
臨床で得られるがん検体の多くは、薄切のパラフィン包埋組織(FFPEブロック)として保存され、何年も保管できます。これらは研究にとって宝の山ですが、技術的な問題が研究を妨げてきました。すなわち、こうした試料は自然発光(バックグラウンド蛍光)が強く、重要なタンパク質からの弱いシグナルをかき消してしまうのです。著者らは、強く精密に調整した光と穏やかな化学処理を組み合わせることで、この背景蛍光だけを選択的に消去し、組織やタンパク質標的を損なうことなく問題を解決しました。この光学的・化学的ハイブリッドな「ブリーチング」工程により画像の明瞭さが飛躍的に向上し、従来は検出できなかった弱いタンパク質シグナルの検出が可能になります。
同一切片に数十種のタンパク質タグを描く
どの細胞が存在し何をしているかを理解するには、特定のタンパク質に結合する抗体で組織を標識します。従来の多重化法は、稀なタンパク質で信号が弱くなるか、同時に追跡できるマーカー数が限られていました。本研究では周期的なチラミド・シグナル増幅(cyclic tyramide signal amplification)と呼ばれる手法を用いています。各ラウンドで少数のマーカーを染め、酵素反応で明るく恒久的に付着する蛍光スポットとして発現させます。その後、抗体を穏やかに除去してもシグナルは残り、バックグラウンドを再ブリーチし、次のマーカー群を追加します。このサイクルを何度も繰り返し、細胞核からの一定のシグナルで画像を整列させることで、単一切片上でスライド全体を対象に30〜60種の異なるタンパク質を単一細胞分解能で安定的に可視化できます。
カラフルな画像を細胞ごとのアトラスに変換する
高プレックス画像は何百万ピクセルもの情報を含み、人間の目だけでは解析しきれません。そこで著者らはコンピュータビジョンのパイプラインを構築し、まず一般的な細胞セグメンテーション向けに開発された深層学習ツールを使って各細胞核を検出し輪郭を引きます。次に、各タンパク質の蛍光が膜にあるのか、細胞質にあるのか、核内にあるのかといった位置情報や論理ルールの組合せに基づき、腫瘍細胞、ヘルパーT細胞、キラーT細胞、B細胞、線維芽細胞などのタイプやサブタイプに各細胞を分類します。出力はスライド上の全ての細胞についてその同定結果と正確な座標を列挙したデジタルテーブルです。これにより複雑な画像が、腫瘍微小環境内で誰がどこにいるかを示す定量的な地図へと変換されます。
転帰を形作る細胞の近隣性を明らかにする
細胞は単独で作用することは稀で、重要なのはどのような隣人を持つかです。これをとらえるために研究者らは各細胞の周りに局所的な近隣を定義するさまざまな方法を試し、最終的に半径ベースのネットワーク手法を採用しました。各細胞の周りに人間の髪の毛ほどの太さの小さな円を描き、その中に誰がいるかをリストアップすると想像してください。周囲の円が類似した隣人の組み合わせを持つ細胞をグループ化することで、免疫細胞が豊富な領域や線維芽細胞が優勢なバリア、腫瘍が支配する領域など、繰り返し現れる「機能的ニッチ」を同定できます。この戦略を結腸組織に適用すると、半径ベースの近隣が既知の解剖学的構造とよりよく一致することが示されました。子宮頸がんの良好な転帰と不良な転帰を示す患者検体を比較すると、良好な転帰の患者では免疫細胞に富むニッチが腫瘍縁近くに集積する一方、不良な転帰の患者では腫瘍細胞を取り囲んで攻撃する免疫細胞を隔離しているような厚い線維芽細胞密集層が見られました。
空間マップから個別化治療へ
多数のタンパク質を高品質かつ手頃なコストで染色する工程と堅牢な画像解析を組み合わせることで、本研究は多数の標準的な病院検体に適用可能なエンドツーエンドのパイプラインを提供します。この手法は保存組織を、腫瘍細胞、免疫細胞、間質細胞がどのように配置・相互作用しているかの詳細な地図へと変換します。一般読者への要点は、細胞の種類だけでなく、その正確な近隣パターンががんの挙動に影響するということです。このプラットフォームは保護的な免疫ホットスポットの特定、抑制的な細胞バリアの同定、そして最終的にはより正確な予後予測やより細かく調整された免疫療法戦略の支援に役立つ可能性があります。
引用: Xiao, C., Zhou, R., Chen, Q. et al. Integrative spatial profiling pipeline for determining TME architectures in archival clinical specimens using CmTSA superplex technology. Cell Discov 12, 16 (2026). https://doi.org/10.1038/s41421-026-00874-9
キーワード: 腫瘍微小環境, 空間プロテオミクス, 多重イメージング, がん免疫学, 単一細胞解析