Clear Sky Science · ja
APOA2を介した内皮間葉転換とがん脂質代謝の再編がTGF-βを通じて抗血管新生薬耐性をもたらす
この発見が患者にとって重要な理由
医師は肝腫瘍への血流を断つことで腫瘍を飢餓状態にする薬をますます使うようになっていますが、多くの患者では一時的な効果の後に治療が効かなくなります。本研究は差し迫った疑問に応えます:なぜ一部の肝がんは血管遮断治療に耐性を獲得するのか、そしてそれをどう攻略できるのか?研究者たちは、血中の脂質輸送に関わるタンパク質と強力な成長シグナルとの間に隠れた協力関係を明らかにしました。それにより腫瘍は血管とエネルギー利用の両方を再配線し、治療の新たな標的を示唆します。
通常の命綱なしで生きることを学んだ腫瘍
肝がんの最も一般的な形である肝細胞がんは、新生血管に大きく依存して増殖します。進行例の標準薬はVEGFとその受容体VEGFR2を中心とした血管新生経路を阻害するよう設計されています。しかし多くの患者で腫瘍はこれらの薬剤にもかかわらず増殖を続けます。著者らは抗血管新生薬アパチニブに反応した患者と反応しなかった患者の腫瘍サンプルを比較し、APOA2という一つの遺伝子が際立っていることを見出しました。耐性患者の腫瘍では、血中脂質の輸送で知られるこのタンパク質の発現が著しく高かったのです。これはAPOA2が血管標的薬から腫瘍を回避させる助けとなっている可能性を示唆しました。
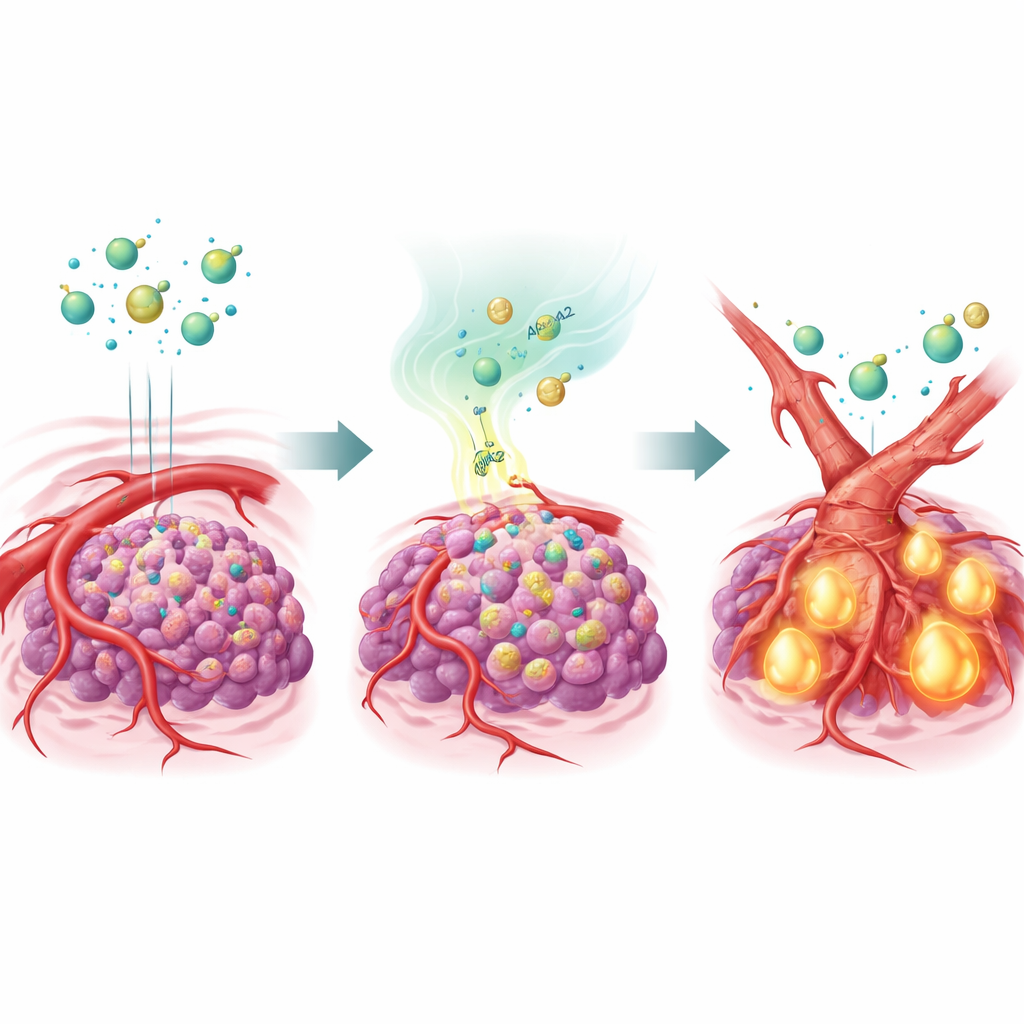
血管の形を変える脂質輸送タンパク質
この仮説を検証するため、研究チームは肝がん細胞にAPOA2を過剰発現させ、それらをマウスに移植しました。複数の抗血管新生薬で治療しても、APOA2高発現腫瘍は大部分で治療を無視し、血管が持続し腫瘍は増殖を続けました。詳細解析で、TGF-βと呼ばれる主要なシグナルがこれらの腫瘍で強く活性化され、腫瘍微小環境と動物の血中の両方でそのレベルが上昇していることが示されました。TGF-βは血管内皮細胞に作用し、内皮から間葉系への転換(endothelial-to-mesenchymal transition)という同一性の変化を促しました。これらの細胞がより瘢痕様で間葉系の性質に変わるにつれ、抗血管新生薬が狙う持ち手であるVEGFR2を大幅に失いました。結果として血管は薬剤がもはや標的にできない形へと再構築されたのです。
がん細胞に燃料を供給し続ける代謝の迂回路
物語は血管壁で終わりませんでした。APOA2が駆動する同じTGF-βシグナルは、がん細胞のエネルギー供給の仕組みも再プログラムしました。糖分解に主に依存していた代わりに、APOA2高発現細胞は周囲からより多くの遊離脂肪酸を取り込み、ミトコンドリアで脂肪酸酸化によりそれらを燃焼させるようになりました。栄養利用と酸素消費を測る実験は、これらの細胞がエネルギー源として脂質により依存するようになり、より多くのATPを産生することを示しました。この変化により、腫瘍細胞は血流が抗血管新生治療で制限されても速やかに分裂を続け、細胞死を回避できたのです。
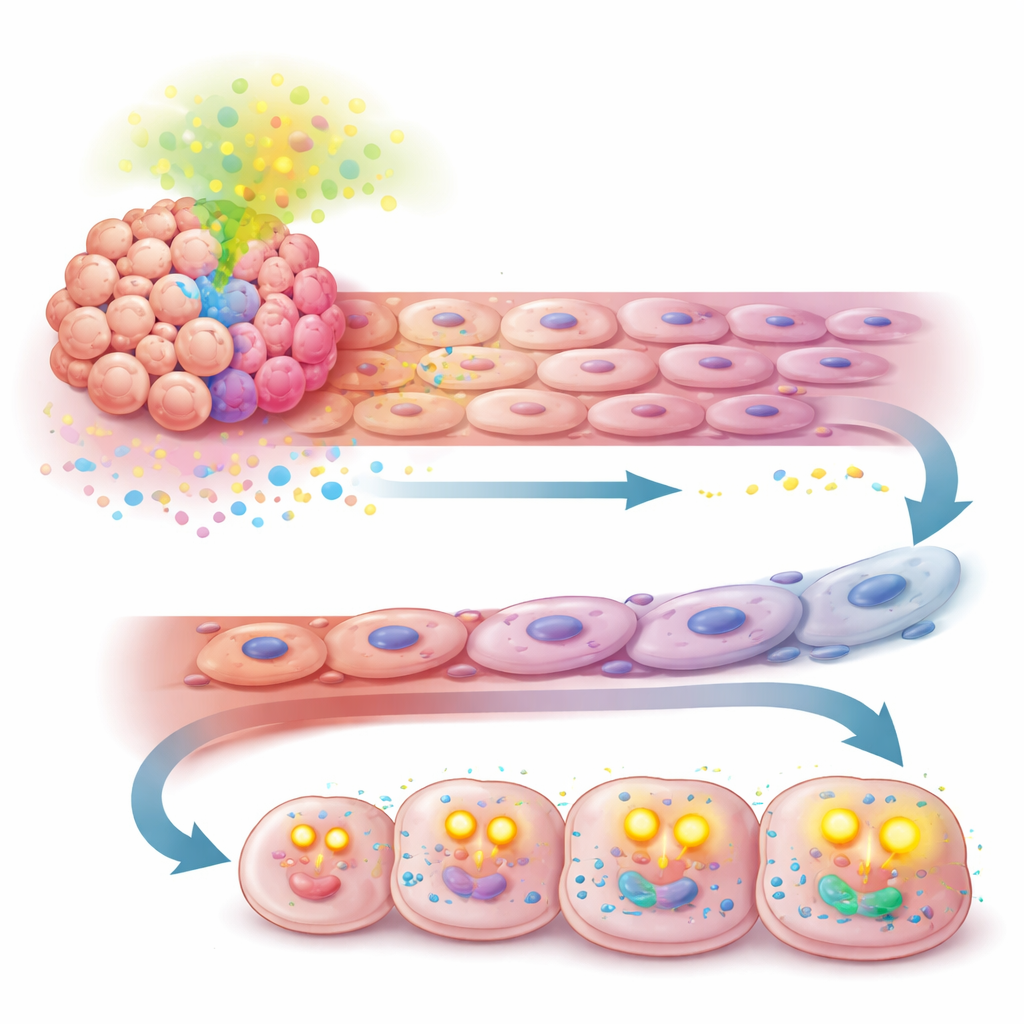
弱点を新たな治療標的に変える
決定的に、研究者らがTGF-βを阻害すると、APOA2が与えていた利点は失われました。マウスモデルでこのシグナルを抑えると、異常な血管変化が減少し、治療感受性が回復し、腫瘍増殖が遅延しました。さらに有望なのは、TGF-βと免疫チェックポイントPD-1を同時に遮断する二重抗体が、APOA2高発現腫瘍で単独療法よりも優れた効果を示したことです。これらの結果は、APOA2高発現で示される一部の肝がんが、従来のVEGF経路から血管と腫瘍代謝の両方を維持するTGF-β中心の経路へと静かに依存先を切り替えたことを示唆しています。
将来の肝がん治療にとっての意味
一般向けに言えば、主要なメッセージは次の通りです:一部の肝腫瘍は配管(血管)と電源(エネルギー供給)の両方を再配線することで、現在の血管遮断薬を回避します。脂質に関連するタンパク質APOA2はTGF-βシグナルを増幅し、その結果、既存薬が見つけられないように血管を覆い隠し、がん細胞に糖ではなく脂肪で生きる方法を学習させます。本研究は、腫瘍をAPOA2で検査することで標準的な抗血管新生薬の恩恵を受けにくい患者を特定し、TGF-βを阻害する薬、特に現代の免疫療法と組み合わせた治療に反応する可能性を示唆しています。要するに、腫瘍の適応メカニズムを明らかにすることで、血管とそれら耐性腫瘍が依存するエネルギー源の両方を標的にする、より個別化された戦略を示しています。
引用: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
キーワード: 肝細胞がん, 抗血管新生薬耐性, APOA2, TGF-βシグナル伝達, がん脂質代謝