Clear Sky Science · ja
ミトコンドリアの生物エネルギー—SASP相互作用が治療誘導性老化におけるセノリティックの有効性を決める
“ゾンビ”がん細胞を消し去るのが難しい理由
現代のがん治療薬の多くはすべての腫瘍細胞を即座に死滅させるわけではありません。代わりにいくつかの細胞は分裂を止めて生き残る、いわば「ゾンビ」細胞のような停滞状態、すなわち老化(セネセンス)に入ります。治療によって誘導されたこれらの老化細胞は当初は有益に働くこともありますが、長期間残ると再発や耐性、治療の副作用を助長する可能性があります。したがって、研究者たちは老化細胞を選択的に死滅させるセノリティック薬を検討しています。本論文は一見単純な問いを投げかけます:なぜある治療誘導性老化がん細胞はセノリティックに曝されると死ぬのに、他はしぶとく生き残るのか?
過去を覚えている発電所
研究の中心にあるのは細胞内の小さな発電所、ミトコンドリアです。著者らは、ミトコンドリアが糖類、脂肪、アミノ酸などさまざまな燃料を燃やすやり方が、BCL‑xLという生存タンパクを標的とするセノリティック薬に対する感受性に影響するかどうかを検討しました。ハイスループットアッセイ(MitoPlate S‑1)を用い、さまざまながん細胞株のミトコンドリア活性を、老化を誘導する複数の処理(DNA損傷薬、分裂阻害剤、酸化ストレス、細胞周期阻害剤)前後で機能的に“フィンガープリント”しました。すると、治療誘導性老化は単一の均一なミトコンドリア状態を生み出すわけではなく、各薬剤がそれぞれ独特の「生物エネルギーの刻印」を残し、ミトコンドリアがどの程度広範かつ強くさまざまなエネルギー源にアクセスできるかを変化させることが分かりました。重要なのは、この柔軟性は既存のベースラインの上に重なっていることで、親細胞の元々のミトコンドリア構成が、後のどの程度のセノリティック反応が発揮されうるかの上限――“天井”――を設定している点です。
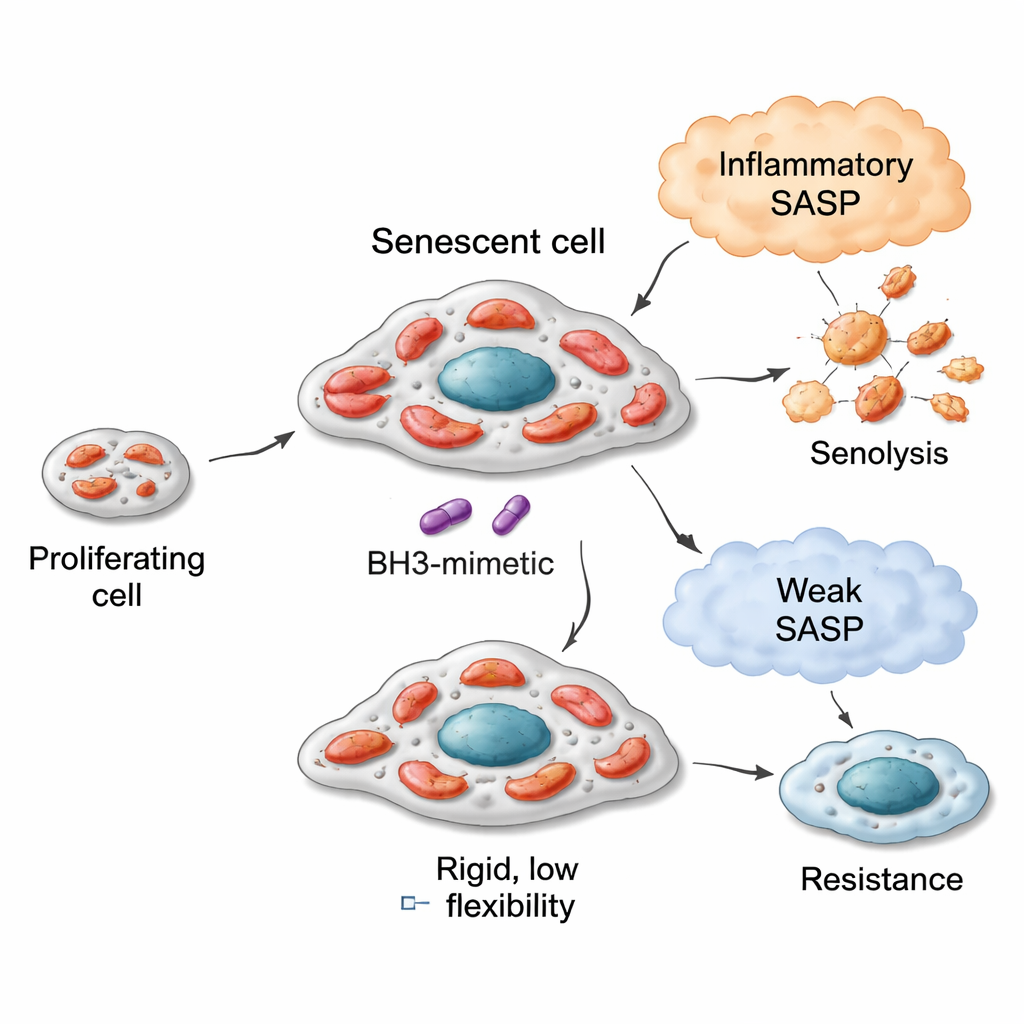
可変なエンジン、異なる燃料、そしてセノリティック感受性
肺がん、乳がん、結腸がんモデルでは、より柔軟なミトコンドリアを持つ老化細胞――より広い配列の燃料を酸化できる細胞――は、ナビトクラクス(ABT‑263)やA1331852のようなBCL‑xLを標的とするセノリティックに対して脆弱である傾向がありました。例えば、薬剤ブレオマイシンで老化に導かれた肺がん細胞は、多くの基質を精力的に利用するミトコンドリアを発達させ、とくに脂肪酸分解や特定のアミノ酸経路に関連する基質を活発に使いました。これらの細胞はセノリティックに非常に感受性が高かった。一方、CDK4/6阻害剤(パルボシクリブ)で老化に追い込まれた細胞は代謝的レパートリーが狭く、同じセノリティック薬には反応が乏しかった。しかしこの関係には限界がありました:乳がん細胞は老化後に代謝的に柔軟になることもありましたが、出発点のミトコンドリアがアポトーシスへ“準備”されていなかったため、最大のセノリティック反応は控えめでした。アポトーシス機構に欠陥のある結腸がん細胞は、代謝がどう変化しても抵抗性を維持しました。ひとつの単純な指標――ベースラインで細胞が燃料であるスクシネートをどれだけ酸化できるか――がこの遺伝的なミトコンドリア能力の簡便な指標として機能しました。
代謝が炎症と語り合うとき
老化細胞は、周囲の組織に影響を与える分泌性の炎症・成長因子のカクテルであるSASPで悪名高いです。研究チームは、ミトコンドリア代謝がこの分泌挙動とどう結びつくかを、転写因子NF‑κBによりスイッチされるマイクロRNA miR‑146aのレポーターを組み込んだ細胞を用いて探りました。全体的なSASPプロファイルは主に細胞種に依存していましたが、特定の老化状態だけがこのNF‑κB/miR‑146a軸を活性化することが分かりました。そしてそれらはBCL‑xLセノリティックに良く反応する同じ状態でした。重要なのは、これらの“炎症性SASP陽性”老化細胞は脂肪酸酸化の利用が増え、長鎖脂肪酸をミトコンドリアに搬送する遺伝子の転写上方制御を示していたことです。脂肪酸のミトコンドリアへの流入を阻害する薬剤エトモキシルで阻害すると、miR‑146aの活性化は抑えられましたが、老化そのものは完全には逆転しませんでした。これはミトコンドリアの燃料選択が、炎症性でセノリティックに寛容なSASPの成立を助けていることを示唆します。
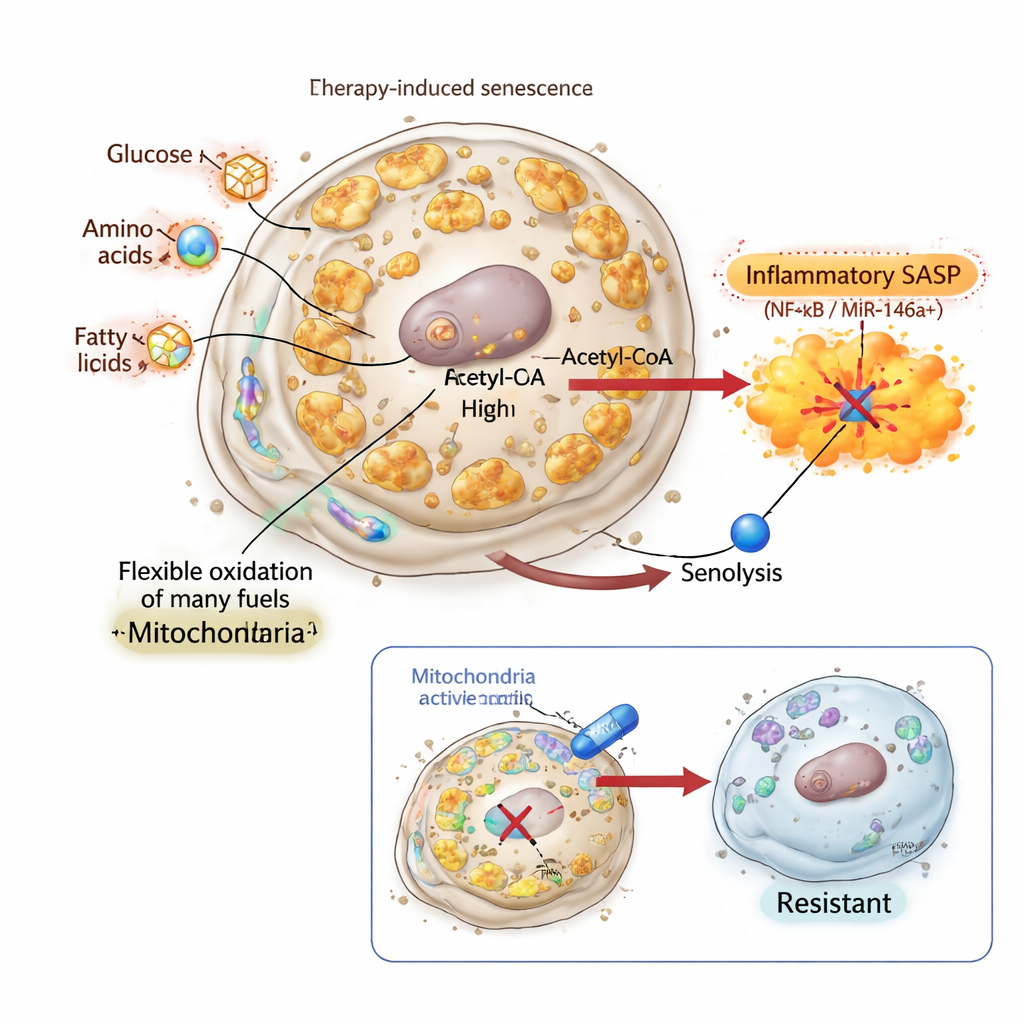
シグナルを消し、殺せない老化細胞を作る
炎症性SASPがセノリティックによる細胞死に本当に必要かを検証するために、研究者らはインフラクロメンに着目しました。インフラクロメンはクロマチンタンパク質HMGB1およびHMGB2に結合し、SASP遺伝子の活性化におけるそれらの役割を阻害します。肺がんおよび乳がん細胞では、インフラクロメンは古典的な老化表現型を誘導しました:細胞は大型化し分裂を停止し、老化マーカーが蓄積しました。ミトコンドリア量と生物エネルギー活性は大幅に上昇し、燃料利用も明確に再編されました。しかしSASPは抑制され、miR‑146aレポーターはほとんど沈黙したままでした。驚くべきことに、これらSASP非発現の老化細胞は、ミトコンドリアが生物エネルギー的に活性で再プログラムされ、抗アポトーシス遺伝子BCL2の発現が低下しているにもかかわらず、BCL‑xL標的のセノリティックに完全に抵抗性を示しました。これはミトコンドリアの変化だけでは不十分であり、ミトコンドリア駆動の炎症性アウトプットがなければセノリティックの“二撃”は失敗することを示しています。
今後のがん治療への含意
一般読者向けに言えば、本研究の結論は治療誘導性“ゾンビ”がん細胞を殺すには多層的な回路が支配しているということです。第一に、腫瘍細胞のミトコンドリアの元々の健全さと配線が、セノリティック薬が到達し得る限界を決めます。第二に、老化を引き起こす特定の治療がミトコンドリア代謝をより柔軟にするか狭めるかで、細胞がアポトーシスの瀬戸際に近づくか遠ざかるかが決まります。第三に、そして最も決定的なのは、代謝の再配線が炎症性SASPプログラムを有効にして核と対話しない限り、セノリティック薬はうまく機能しないという点です。その炎症性クロストークが欠けると、老化細胞は薬剤耐性の行き止まり状態になり得ます。実用的には、将来の治療は腫瘍でのミトコンドリアの柔軟性とSASP炎症の両方を機能的に評価し、それに基づいて老化誘導薬とセノリティックを組み合わせることで、単に細胞を停止させるだけでなく、確実に除去できるよう最適化することが示唆されます。
引用: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
キーワード: 細胞老化, ミトコンドリア, セノリティクス, がん代謝, 炎症性SASP