Clear Sky Science · ja
FLT3-ITD 急性骨髄性白血病細胞モデルにおけるカボザンチニブ耐性を緩和するための代謝シグネチャの変調
がん治療にとってなぜ重要か
多くの現代のがん薬は腫瘍細胞内の単一の異常タンパク質を標的にするよう設計されています。こうした標的療法は劇的な寛解を引き起こすことがありますが、がんはしばしば適応して再発します。本論文は、血液がんの一種である急性骨髄性白血病(AML)が、カボザンチニブという標的薬に対してどのように耐性を獲得するか、そしてがん細胞のエネルギー利用を再配線することでその耐性をどうやって克服できるかを検討しています。
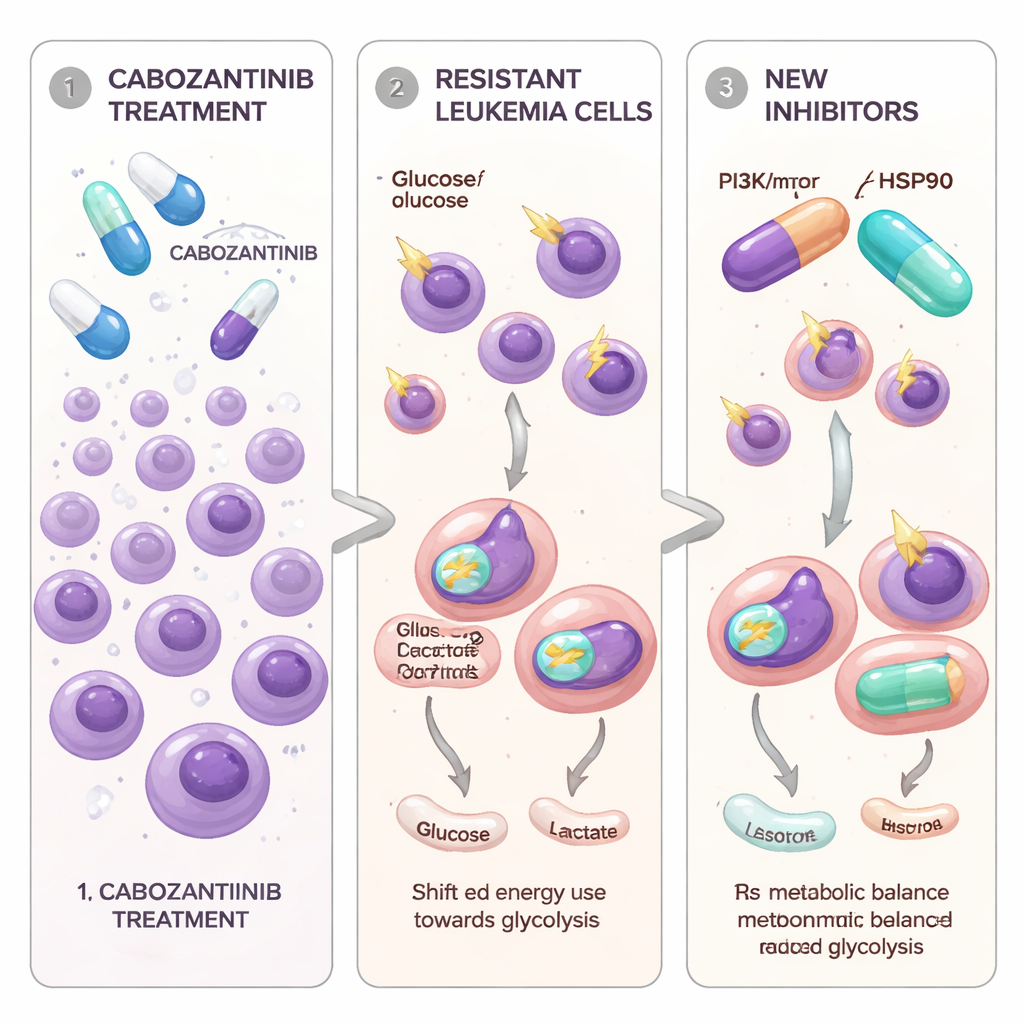
標的薬をかわすことを学んだ白血病細胞
研究者らは、FLT3-ITDという増殖シグナルのスイッチに変異を持つAML細胞に注目しました。これは特に攻撃性の高い病態を促すことで知られています。カボザンチニブは既にいくつかの固形腫瘍で用いられている経口薬で、培養中のFLT3駆動型白血病細胞を強力に抑えることができます。患者で時間経過とともに起きる現象を模倣するため、研究チームは2つのFLT3変異AML細胞株を徐々に増加するカボザンチニブ濃度に曝露し、生き残って再増殖する細胞を得ました。これらの新しい細胞集団(Molm13-XRおよびMV4-11-XR)は、もとの“親”細胞に比べてはるかに高濃度のカボザンチニブに耐性を示しました。また、別の承認済みFLT3標的薬であるソラフェニブやクザルチニブにも感受性が低下した一方で、ギルテリチニブには引き続き脆弱でした。
がんが生き残るための遺伝的調整
詳細を調べると、これらの薬剤耐性白血病細胞はFLT3遺伝子に新たな変化を持っていました。耐性の両系統は、FLT3のキナーゼ領域の重要な部位にD835Yと呼ばれる同じ点変異を獲得しており、これは複数の薬剤に対する耐性のホットスポットとして知られています。MV4-11-XR系ではさらに1.3キロベースの異常な欠失が生じ、FLT3の一つのエクソンが失われ、薬剤結合に重要な領域の一部が消失していました。これらの変化は長期のカボザンチニブ曝露中に選択されたようで、変異型FLT3の頻度は耐性細胞で出発時より大幅に増加していました。同時に、FLT3下流の主要なシグナル経路(ERK、STAT5、AKTなど)がより強く活性化され、耐性細胞での増殖促進とコロニー形成能の増大を支持していました。
がん細胞は燃料システムを切り替える
研究チームは耐性が遺伝的変化だけでなく、細胞のエネルギー供給方法とも関係するかを調べました。RNAシーケンシングと専用の代謝検査を用いると、一貫したパターンが見られました:カボザンチニブ耐性細胞は、酸素が十分にある状況でもグルコースの速やかな分解である解糖(グリコリシス)に大きく依存していました。これらの細胞はグルコース取り込みが増加し、乳酸の産生が増え、主要酵素であるGAPDHの活性が高まり、複数の解糖関連遺伝子の発現が上昇していました。対照的に、より効率的なエネルギー生産を担うミトコンドリアは活動性と量が低下していました。酸素消費の測定では基礎的および最大のミトコンドリア呼吸がともに低下し、細胞内の活性酸素種が増加しており、ミトコンドリアがストレスを受け低機能であることを示していました。
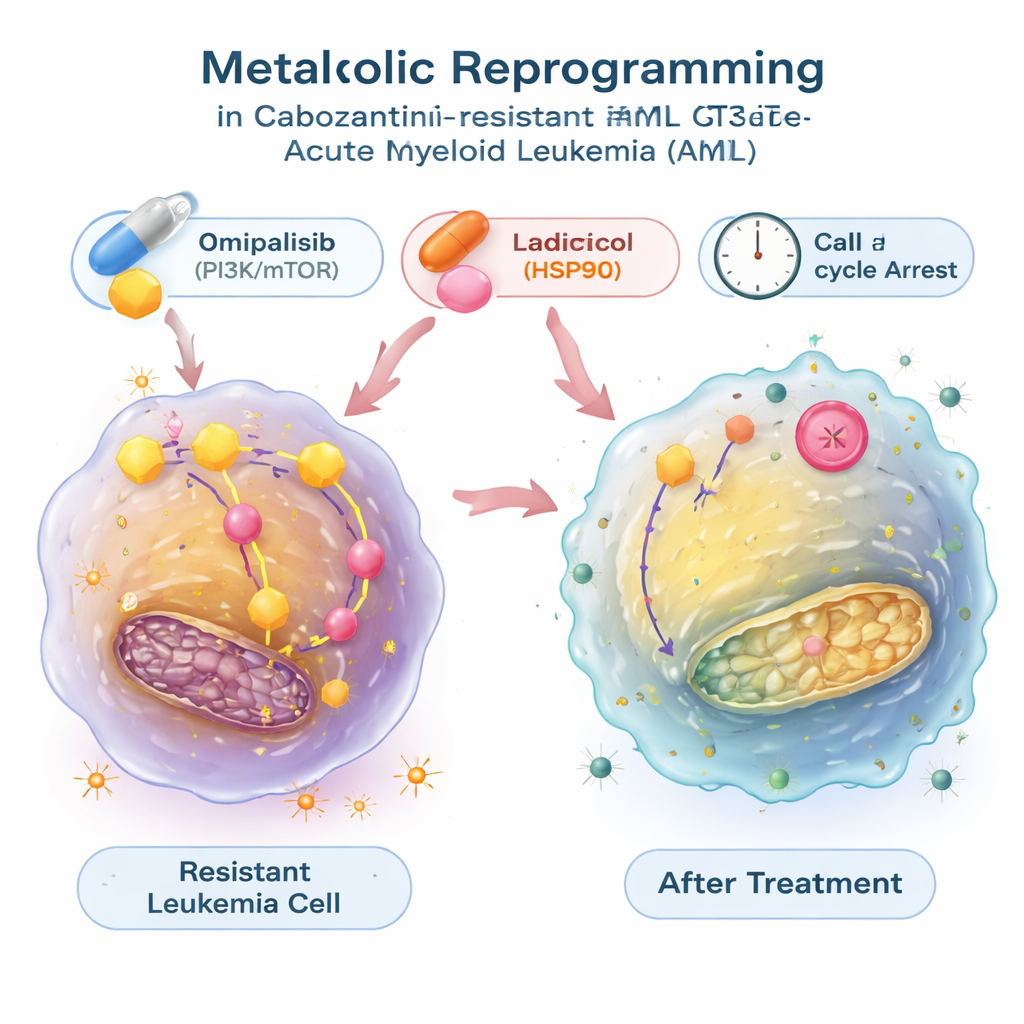
代謝スイッチを元に戻す薬剤の探索
このエネルギー転換を逆転できるかを確認するため、研究者らは遺伝子発現パターンと数千の化合物の効果を結びつけた大規模な公開データベースを利用しました。耐性白血病細胞の代謝シグネチャを打ち消すと予測される薬剤を探索し、二つに絞り込みました:シャペロンタンパク質HSP90を阻害するラジコシルと、成長と代謝を制御するPI3K/mTOR経路を阻害するオミパリシブです。実験室での試験では、両化合物は耐性細胞の増殖を遅らせるだけでなく、過剰な解糖も低下させ、グルコース取り込みや乳酸放出を正常化し、解糖関連遺伝子の発現を抑えました。これらの化合物は白血病細胞を細胞周期の休止状態へと誘導し、ラジコシルの場合は顕著なプログラム細胞死(アポトーシス)を誘発しました。カボザンチニブと併用すると、オミパリシブは(あるモデルではラジコシルも)相乗的に作用し、薬剤耐性細胞をより殺しやすくしました。
将来の白血病治療への示唆
専門外の読者に向けた要点は、白血病細胞が標的薬の標的分子を変異させるだけでなく、エネルギーを作り使う方法を変えることで薬を逃れることがあるということです。この研究は、カボザンチニブ耐性のAML細胞がミトコンドリア機能を低下させつつ「糖を燃やす」戦略を採ることを示しています。オミパリシブやHSP90阻害剤のように、この再配線された代謝を支える経路を標的にすることで、カボザンチニブや類似治療への感受性を回復できる可能性があります。これらの知見は患者ではなく細胞モデルに基づくものですが、標的薬に代謝調節薬を組み合わせることが、FLT3変異AMLにおける耐性の遅延または克服に有望なアプローチであることを示唆しています。
引用: Fu, YH., Ng, K.M., Tseng, CY. et al. Modulating metabolic signatures to mitigate cabozantinib resistance in FLT3-ITD acute myeloid leukemia cell models. Cell Death Discov. 12, 98 (2026). https://doi.org/10.1038/s41420-026-02957-8
キーワード: 急性骨髄性白血病, 薬剤耐性, FLT3変異, 癌の代謝, カボザンチニブ