Clear Sky Science · ja
骨細胞由来リポカリン-2は鉄依存的フェロトーシスとWnt抑制を通じて局所的に骨形成を制御する
骨細胞が静かに全身の健康を形作るとき
多くの人は骨を堅い足場と考えますが、骨は常に再構築と修復を行う細胞で満ちています。本研究は、骨細胞が作る小さなタンパク質リポカリン-2が、鉄とエネルギーの扱いを乱すことで内部から骨を静かに弱らせうることを明らかにします。この隠れた過程を解き明かすことは、骨粗しょう症や加齢に伴う骨減少に対する新たな治療の指針となる可能性があります。
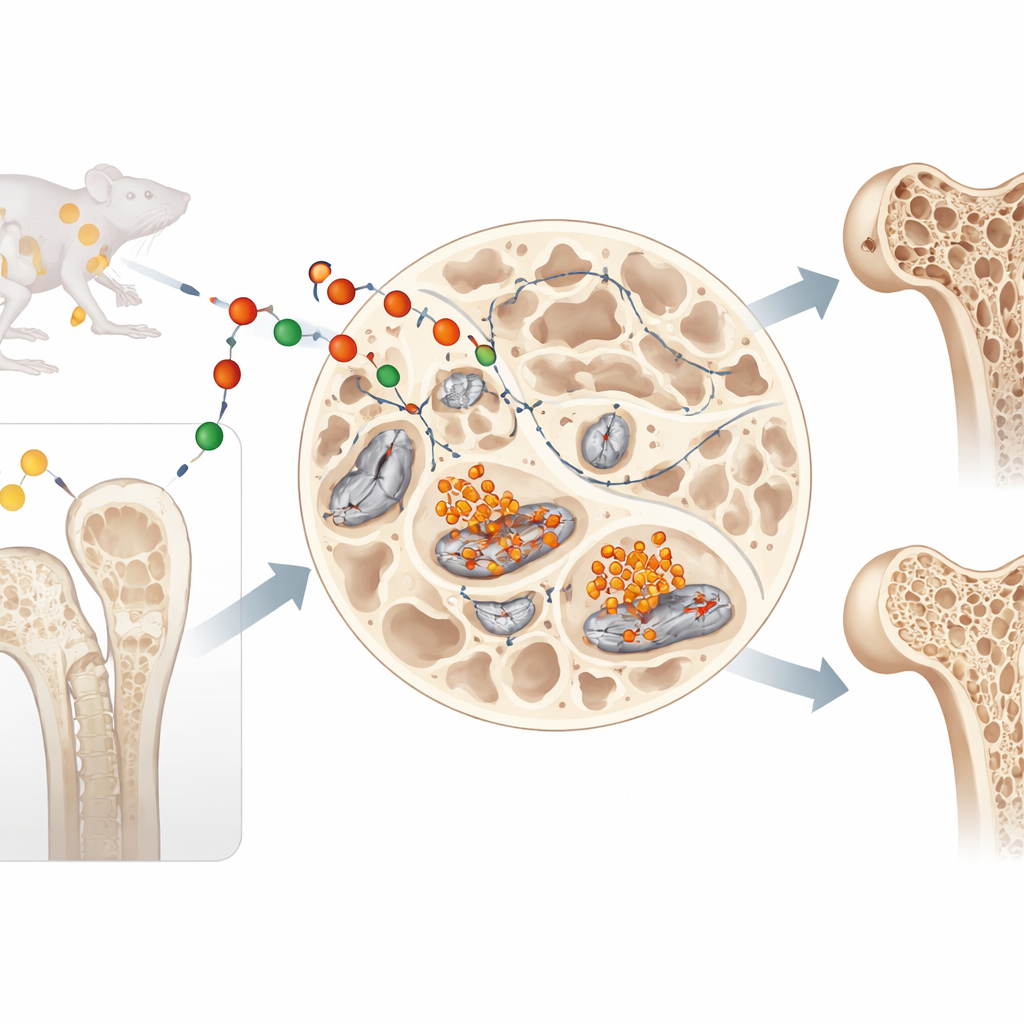
二面性をもつメッセンジャータンパク質
リポカリン-2は血流を介して移動するホルモンとして、食欲や体重の制御に関与したり、鉄を結合して感染防御に寄与したりすることが知られてきました。しかし本論文の著者らは別の問いを立てました:リポカリン-2は、それが作られる骨の内部では何をしているのか?彼らは、力学的刺激を感知し骨の改変を指示する長寿命の埋没細胞であるオステオサイトに着目しました。研究チームは、オステオサイトが成熟するにつれてリポカリン-2の産生を維持するだけでなく実際に増加させることを見いだし、骨格内部で強い局所的役割を果たしていることを示唆しました。
鉄過負荷と“さび”のような細胞死
リポカリン-2が鉄を運搬できることから、研究者らはそれがオステオサイト内での鉄蓄積を促すかどうかを調べました。培養された骨細胞にリポカリン-2を加えると、細胞内に鉄が蓄積し、有害な活性酸素が増加し、脂質に富む細胞膜が深刻に損傷されました。これらはフェロトーシスと呼ばれる比較的新しく認識された細胞死の特徴であり、鉄が“さび”のように破壊的な化学反応を引き起こします。鉄をキレートする化合物で遮断すると損傷と細胞死は完全に防がれ、過程が鉄依存であることが確認されました。
関門受容体とミトコンドリアの崩壊
リポカリン-2がどのように鉄をオステオサイトに運び込むのかを理解するため、研究チームは細胞表面の特定受容体SLC22A17に注目しました。この受容体をオステオサイト様細胞で減少させると、リポカリン-2はもはや鉄の流入、酸化ストレス、あるいはフェロトーシスを引き起こさなくなり、鉄過負荷の条件下でも同様でした。さらに研究は、リポカリン-2が細胞の発電所であるミトコンドリアを損なうことを示しました。過剰なリポカリン-2はミトコンドリア膜電位の喪失とエネルギー産生の低下を引き起こし、リポカリン-2を除くとミトコンドリア機能は回復しました。オステオサイトでリポカリン-2が欠損するマウス骨では、ミトコンドリア呼吸や品質管理を支える遺伝子がオンになり、これらの細胞がよりエネルギー的に健全であることを示唆しました。
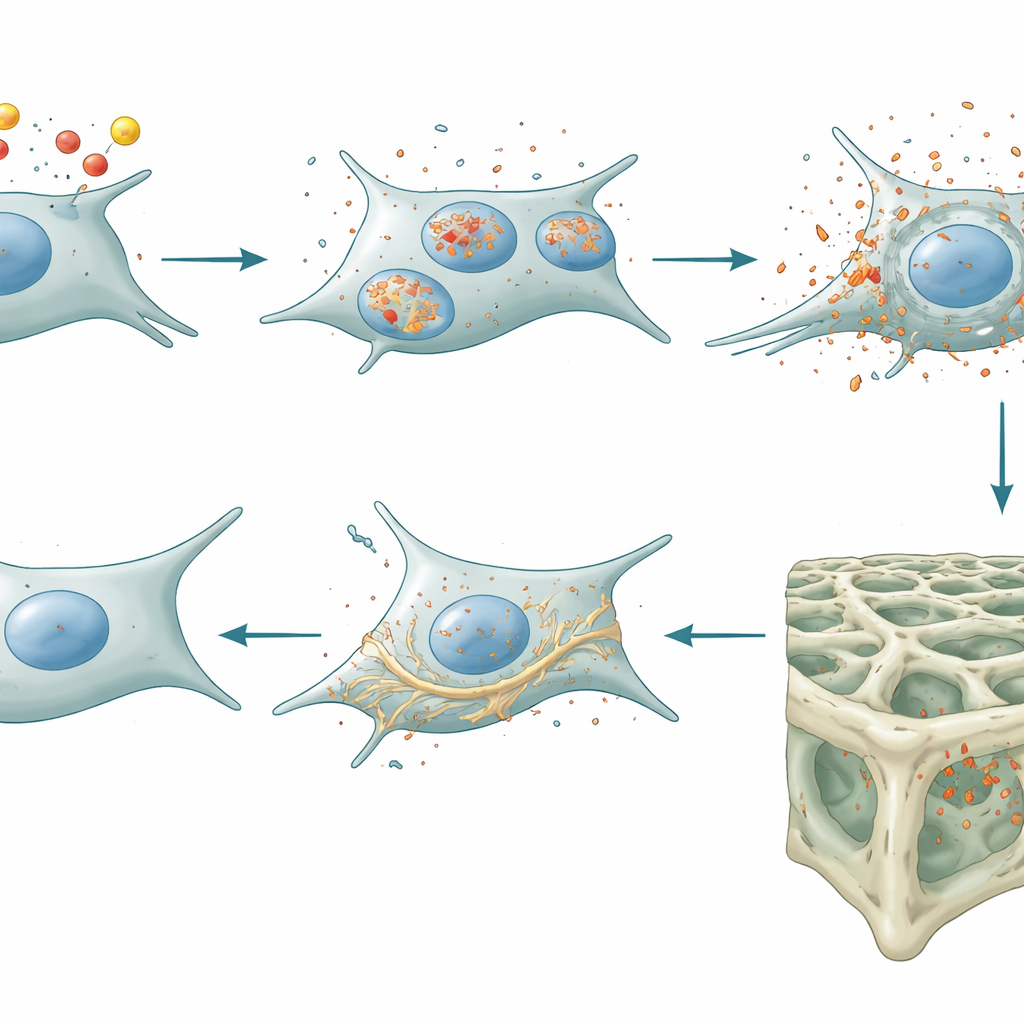
細胞ストレスから骨の弱化へ、そしてブレーキを外す効果
研究者らは次に、骨形成の後期段階細胞およびオステオサイトで特異的にリポカリン-2を欠損させるよう遺伝子改変した個体を調べました。これらの動物は骨細胞内の鉄蓄積が少なく、フェロトーシスに対抗する抗酸化防御が強化されていました。重要なのは、彼らが骨形成を主導する主要経路であるWnt/β-カテニン経路に対してブレーキとして働く二つのタンパク質—スクレロスチンとDKK1—の産生が低下していたことです。そのブレーキが緩まることで、骨を作るオステオブラストを促すシグナルが増加しました。マイクロCTスキャンや骨標識実験は結果を裏付けており、オステオサイト由来リポカリン-2を欠くマウスは海綿状(びまん)骨の量と連結性が増加しており、主に骨形成の増加によって実現していました。体重、血糖コントロール、代謝、活動レベルは正常のままであり、効果が全身ホルモン作用ではなく骨局所に限られていることを示しました。
骨を強く保つために意味すること
簡潔に言えば、本研究は骨細胞内のリポカリン-2が局所的なスイッチとして働き、鉄レベルを上げ、ミトコンドリアに負担をかけ、細胞をフェロトーシスに備えさせ、主要な成長経路を抑えることで新しい骨形成を制限することを示しています。この内部のブレーキを取り除くと、オステオサイトはより健康になり、骨形成を促すシグナルを多く発し、全身の代謝を乱すことなく海綿骨はより密でつながりの良い構造になります。リポカリン-2のレベルと鉄の不均衡は加齢や慢性炎症で増すため、リポカリン-2とその受容体系を標的にすることは、骨が内部から“さびる”のを防ぐ新しい手段を提供する可能性があります。
引用: Khanal, V., Carroll, M., Moradi, F. et al. Osteocytic Lipocalin-2 regulates bone formation locally through iron-dependent ferroptosis and Wnt suppression. Cell Death Discov. 12, 113 (2026). https://doi.org/10.1038/s41420-026-02956-9
キーワード: 骨の健康, 骨細胞(オステオサイト), 鉄代謝, フェロトーシス, Wnt シグナル伝達