Clear Sky Science · ja
膠芽腫の脆弱性を解き明かす:制御された細胞死経路を標的とした革新的治療法
脳腫瘍における細胞死が重要な理由
膠腫は成人において最も頻度が高く、致死的になり得る脳腫瘍のひとつです。外科手術、放射線、化学療法を組み合わせても再発しやすく制御が難しいことが多い。レビュー記事では新たな攻め口――細胞がプログラムされた死に方の多様性を利用する――を検討します。こうした“自己破壊”経路を理解し操作することで、膠腫細胞の弱点を露呈させ、将来の治療をより効果的かつ個別化されたものにすることが期待されています。
膠腫は標準治療をどう回避するか
膠腫は脳の支持細胞から発生し、増殖が緩慢なものから膠芽腫のような高度に侵襲的なものまで幅があります。予後不良の原因は複数にわたり、遺伝子変異、エピジェネティックな変化、死にくい幹様細胞、異常な血管供給、強い免疫抑制環境が絡み合っています。さらに血液脳関門により薬剤が腫瘍に届きにくいことも問題です。これらが組み合わさることで腫瘍細胞は手術や標準薬を生き延び、ストレスに適応し、最終的に再成長します。 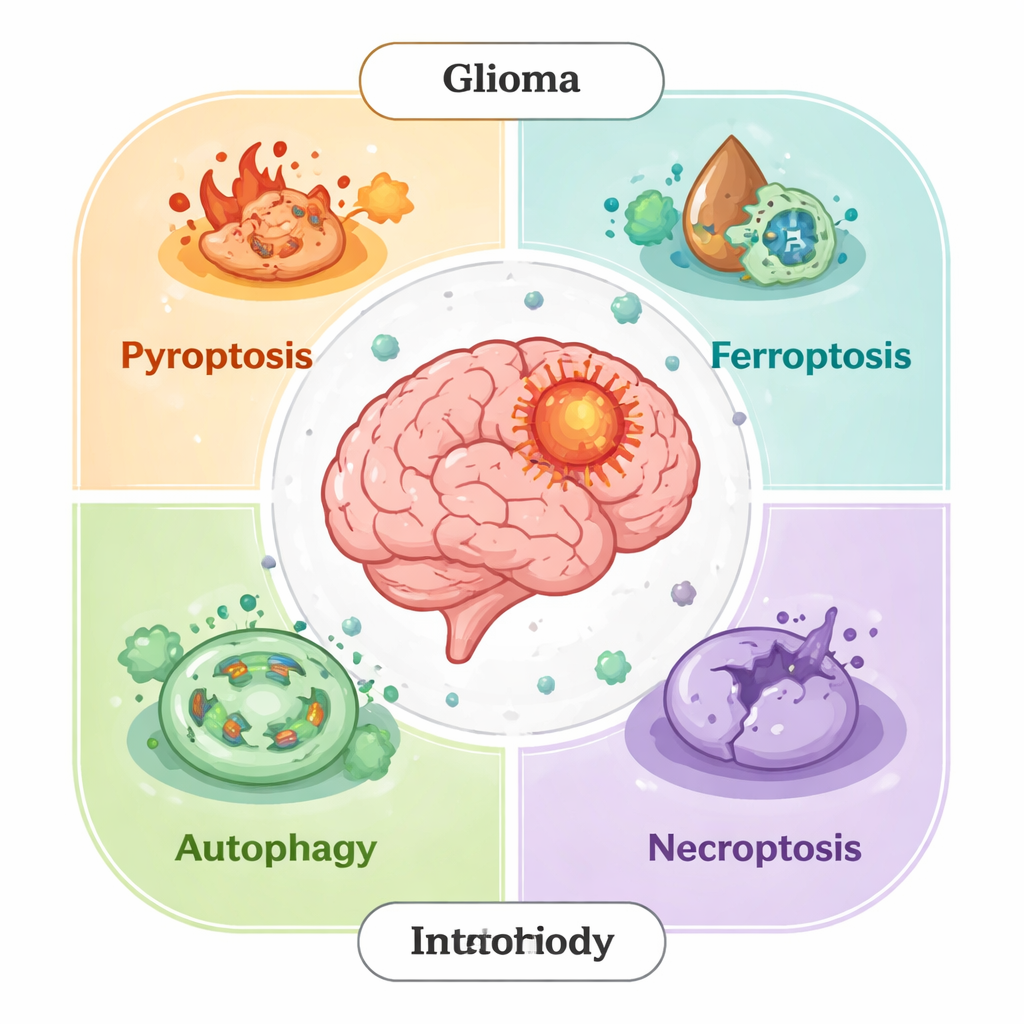
細胞自己破壊の多様な顔
長年、科学者はアポトーシスと呼ばれる主要なプログラム細胞死に注目してきましたが、それが全てではないことが明らかになっています。膠腫細胞はパイロトーシス(炎症性の破裂)、フェロトーシス(鉄依存の膜損傷)、ネクロプトーシス(制御された細胞破裂)、およびオートファジー依存性の死など、他の制御された経路でも死に至ります。健常組織ではこれらの過程が損傷細胞を除去しがんを防ぎますが、腫瘍では膠腫細胞がこれらの経路を再配線し、死のシグナルを遮断したり抗酸化防御を高めたり、オートファジーを生存手段に変えたりして治療抵抗性を獲得し、成長に有利な微小環境を作り上げます。
死の経路を治療に転換する
これらの死の経路を問題としてではなく武器として使う研究が進んでいます。パイロトーシスを誘導する戦略では、賢いナノ粒子、光加熱、遺伝子改変ウイルス、薬剤を含むハイドロゲルなどを用いて膠腫細胞を膨張・破裂させ、免疫系に知らせる危険シグナルを放出させます。フェロトーシスを基盤とするアプローチは、GPX4などの重要な保護酵素を阻害したり、グルタチオン合成を妨げたり、脂質代謝の扱いを変えたりして腫瘍細胞を鉄依存の崩壊に追い込みます。こうした戦術の多くは、グラフダイインやその他のナノ粒子など高度な担体で送達され、血液脳関門を越えて腫瘍内に薬剤を濃縮し、健常な脳組織をなるべく温存することを目指します。 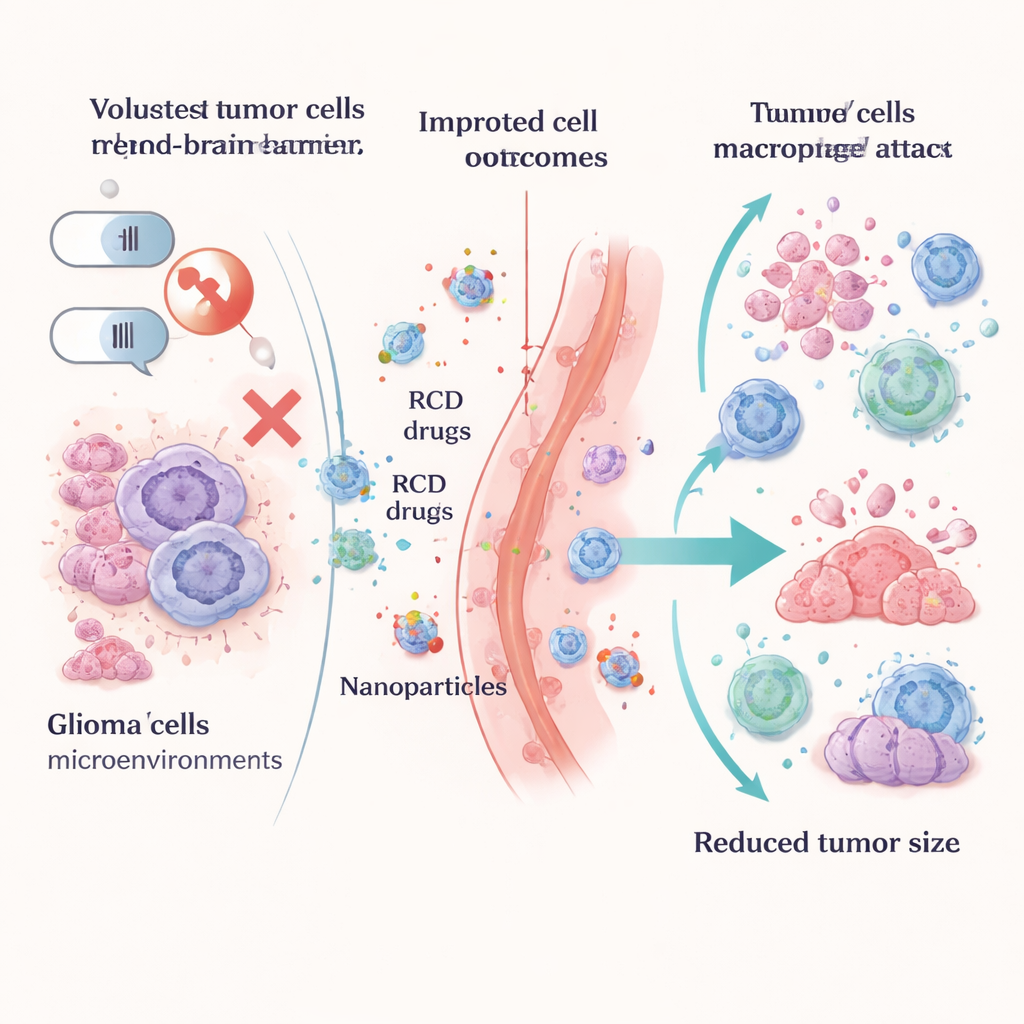
腫瘍の免疫環境を再起動する
ネクロプトーシスに着目した治療は、標準的な死のシグナルに反応しなくなった細胞の抵抗を克服することを目標としています。シコン(シコン酸化物)、エモジン、セラストロール誘導体などの天然物は膠腫細胞をネクロプトーシスへと押し込み、細胞死だけでなく免疫細胞を腫瘍へ引き寄せる分子を放出させます。同時に研究者はオートファジーを探り、時には放射線や化学療法をやり過ごすための“自己清掃”を阻止するためにそれを遮断し、時には限界を超えてオートファジーを促進して細胞死を誘導します。クロロキンやヒドロキシクロロキンのような薬剤を用いた初期の臨床試験は、オートファジーが患者で安全に調節可能であることを示していますが、明確な生存利益はまだ証明されていません。
研究室の発見から個別化医療へ
これらの概念を実臨床の治療へ変換するには依然として困難が伴います。膠腫は患者ごと、さらには同一腫瘍内でも大きく異なるため、単一の細胞死経路戦略がすべてに適合するわけではありません。血液脳関門は依然として薬物送達を妨げ、免疫微小環境は巧妙な治療の組み合わせでさえ効果を弱める可能性があります。著者らは有望な方向性を挙げています:フェロトーシス誘導剤と免疫チェックポイント阻害剤の併用、腫瘍溶解性ウイルスとがん細胞の“食べてください”シグナルを高める薬剤の組み合わせ、選択的な化学放射線療法にオートファジー調節剤を加えることなどです。マルチオミクスプロファイリングとより良いバイオマーカーが、どの患者がどの戦略の組み合わせから利益を得やすいかを特定するのに役立つはずです。
展望:腫瘍に自己破壊を選ばせる
簡潔に言えば、この記事は膠腫治療の将来は、腫瘍細胞に慎重に制御された方法で自己破壊ボタンを押させることにあると結論づけています。パイロトーシス、フェロトーシス、ネクロプトーシス、オートファジー依存性の死をどう誘導し連携させるかを学び、これらを現代の免疫療法や精密な薬物送達と組み合わせることで、現在は厳しい診断である膠腫をより管理可能で最終的には治癒可能なものに変えていくことが期待されます。
引用: Guo, J., Zong, L., Huang, Y. et al. Unlocking glioma vulnerabilities: targeting regulated cell death pathways for innovative therapies. Cell Death Discov. 12, 95 (2026). https://doi.org/10.1038/s41420-026-02949-8
キーワード: 膠腫, 制御された細胞死, パイロトーシス, フェロトーシス, 膠芽腫治療