Clear Sky Science · ja
膵臓がんにおけるミトファジー:機序の洞察と新規治療戦略への示唆
膵臓がんで細胞の発電所が重要な理由
膵管腺がんは最も致死率の高いがんの一つであり、その一因は腫瘍が医師の投げかけるほとんどすべての治療に素早く耐性を獲得する点にあります。本レビューは、その耐性の物語における意外な登場人物──ミトファジー、すなわち損耗したミトコンドリアという小さな「発電所」を識別して再利用する細胞の内在的システム──に焦点を当てます。膵臓がんがこの掃除機能をどう乗っ取り、利用するかを理解することは、より効果的で持続性のある治療法への新たな道を開く可能性があります。
細胞の清掃班とがんの生存戦術
ミトコンドリアは単にエネルギーを生み出すだけでなく、代謝、細胞死、そして活性酸素種のような有害分子の処理を制御する役割を担います。ミトコンドリアが損傷したり過剰になったりすると、細胞はミトファジーを用いてそれらにタグを付け除去します。このプロセスには主に二つの経路があります。ひとつはPINK1/Parkin経路として知られ、損傷センサーであるPINK1と標識付け酵素Parkinが故障したミトコンドリアを破壊対象としてマークします。もうひとつはBNIP3、NIX、FUNDC1といった受容体タンパク質がミトコンドリア表面に存在し、同じ標識工程を経ずにそれらをオートファゴソーム(細胞の廃棄袋)に直接つなげるものです。これらの経路はしばしば協調して働き、低酸素や薬剤曝露などのストレスに応じてミトコンドリアの在庫を柔軟に適応させます。 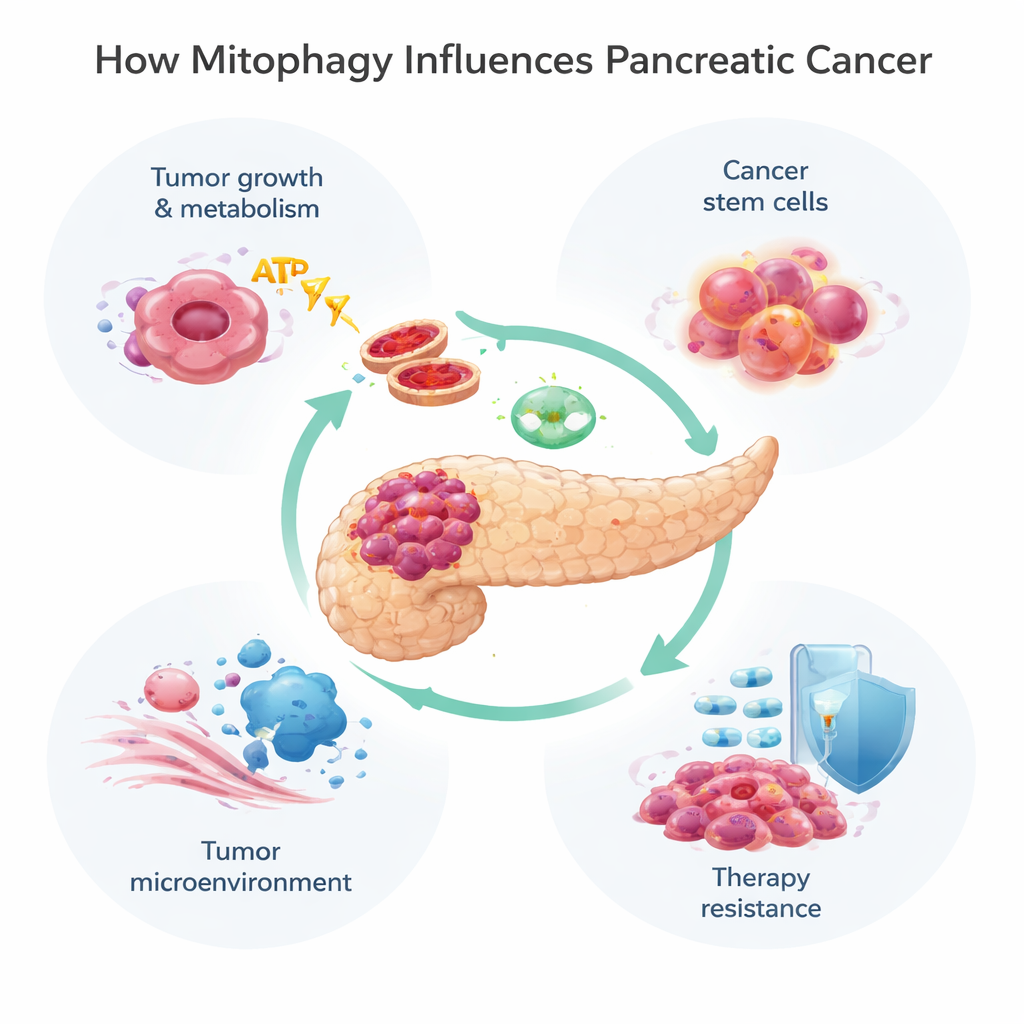
膵臓腫瘍がエネルギー利用を再構築する方法
膵臓腫瘍は過酷な環境に生きています:血流や酸素供給が乏しく、濃密な瘢痕様組織に囲まれています。生き残るためにがん細胞はエネルギーシステムを再配線し、多くの場合ミトコンドリアでの酸素依存的な呼吸から、より原始的な糖分燃焼過程である解糖系へとシフトします。ミトファジーはこのシフトを微調整する役割を果たします。腫瘍の初期形成では、PINK1やParkinの喪失が鉄の蓄積、過剰な活性酸素種、解糖系への傾斜を許し、がん形成を促進します。一方でミトファジー因子NIXは、機能するミトコンドリアをも除去してしまい、細胞をさらに解糖代謝へと押し、成長を速めることがあります。これに対してBNIP3はより複雑な振る舞いを示します:初期に発現し、進行した多くの腫瘍では以後サイレンシングされ、再発現させるとがん細胞の増殖を遅らせることがあるため、あるミトファジー経路はがんを抑制し、他は促進すると示唆されます。
がん幹細胞と腫瘍の周囲環境
すべてのがん細胞が同じではありません。少数のサブセット、しばしばがん幹細胞と呼ばれる細胞は自己複製し、新しい腫瘍を起こし、化学療法に特に耐えやすい性質を持ちます。膵臓がんでは、これらの細胞は代謝的に柔軟であり続けるためにミトファジーに依存しています。ISG15と呼ばれる修飾タンパク質がこの過程を支持し、幹様性を維持することで、ミトファジーが再発や治療失敗に直接結びつきます。がん細胞自身を越えて、ミトファジーは腫瘍微小環境――腫瘍を取り巻く支持細胞、免疫細胞、結合組織などの混合体――も形作ります。たとえばがん関連線維芽細胞は“逆ウォーバーグ効果”に駆り立てられ、自らミトファジーと解糖を高め、腫瘍に対してエネルギーに富む副産物を供給することがあります。ミトファジーはまた、MHC‑Iのような免疫フラグや腫瘍が隠れるために用いるPD‑L1のようなブレーキの表示を変化させることで、免疫細胞ががんを認識・攻撃する様子にも影響を及ぼします。
清掃を阻むか促すかで薬剤反応が変わる理由
ゲムシタビンのような化学療法薬や、一般的なKRAS‑G12D変異に対する新しい標的薬を含む多くの標準的・実験的治療はミトコンドリアに損傷を与えます。腫瘍細胞はしばしばミトファジーを活性化してその損傷を除去し、死から逃れます。研究はPINK1駆動のミトファジーが化学療法や一部の天然化合物の殺傷効果を弱め、がん細胞の生存を助けうることを示しています。他方で、ある条件下ではBNIP3やNIXを介してミトファジーを過度に促進すると、あまりに多くの機能的ミトコンドリアを失わせ、エネルギー危機を招いて細胞死に至らしめる可能性があります。この二面性により、ミトファジーは腫瘍を治療から守る一方で、適切に操作すれば腫瘍をより脆弱にすることもできます。 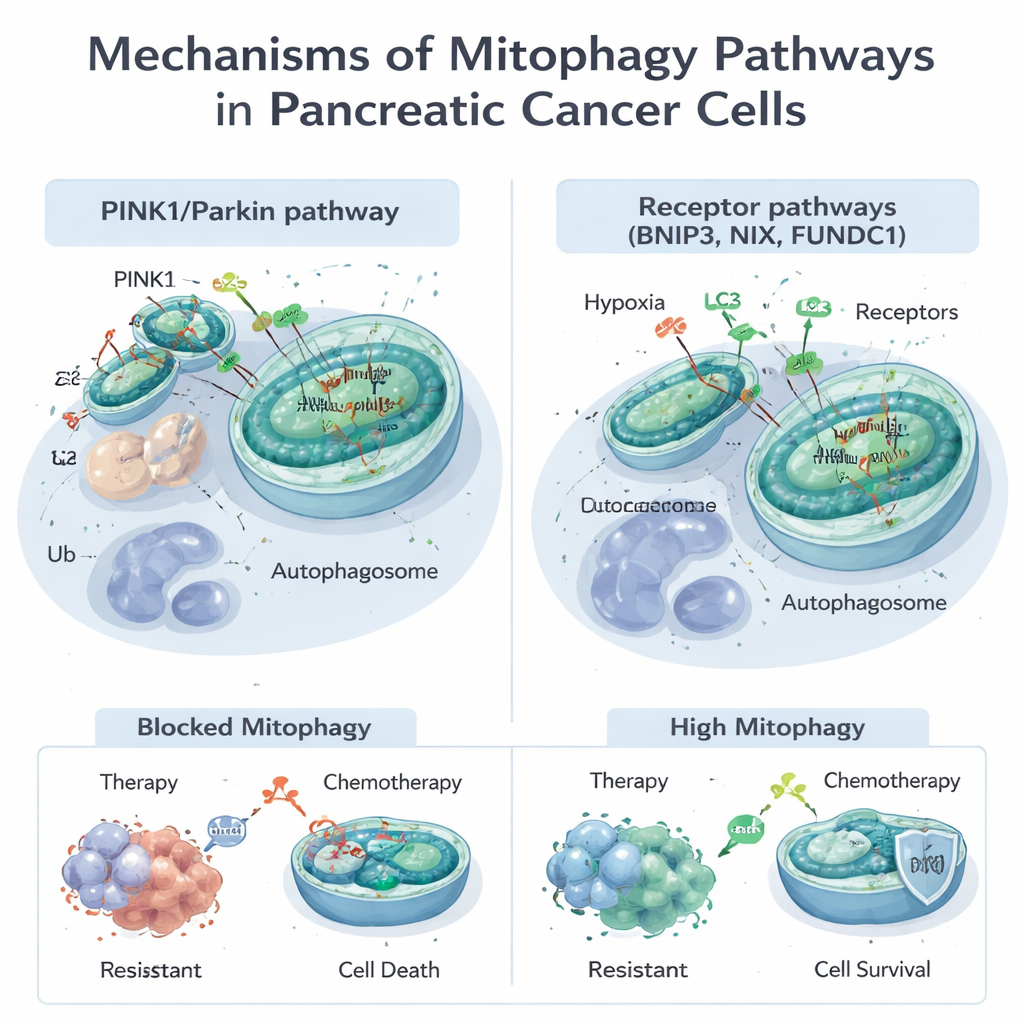
新しい治療アイデアと適切な患者選別の必要性
ミトファジーは代謝、ストレス応答、細胞死の交差点に位置するため、併用療法の魅力的な標的です。現在の薬剤戦略の多くは間接的に作用します:一部の化合物はミトコンドリアの分裂と融合を妨げ、クロロキンやヒドロキシクロロキンのような薬は廃棄袋と酸性分解隔室の融合を阻害してリサイクル過程の最終段階を遮断します。これらの薬剤を標準化学療法と併用する臨床試験が膵臓がんでいくつか進行中です。しかしこれまでの結果はまちまちで、一部の患者は利益を得る一方で得られない患者もいます。問題の一端は、腫瘍が基礎的なミトファジー活性や代謝プロファイルにおいて大きく異なる点にあります:ある腫瘍はミトコンドリア呼吸に強く依存し、別の腫瘍は解糖に依存します。著者らは、将来の成功はミトファジー活性やエネルギー利用によって患者を分類するより良いバイオマーカーや遺伝子署名の開発、そしてオートファジーを単にオン・オフするのではなく特定のミトファジー経路を選択的に調整するより精密な薬剤の開発に依存すると主張します。一般読者への要点は、ミトコンドリアのこの清掃システムを読み取り慎重に調整する術を学ぶことで、膵臓がんを手強い敵からより管理可能な疾患へと変えられる可能性がある、ということです。
引用: Wang, Z., Lyu, Z., Palmen, R. et al. Mitophagy in pancreatic cancer: mechanistic insights and implications for novel therapeutic strategies. Cell Death Discov. 12, 93 (2026). https://doi.org/10.1038/s41420-026-02948-9
キーワード: 膵臓がん, ミトファジー, ミトコンドリア, 化学療法耐性, 腫瘍代謝