Clear Sky Science · ja
DIAPH3の喪失がマウスでの膠芽腫発生を加速する
この脳研究が重要な理由
膠芽腫は最も致命的な脳腫瘍の一つであり、手術、放射線、化学療法を行っても多くの患者は1年余りしか生存できません。本研究は基本的だが重要な問いを立てます:脳細胞内のどのような初期変化がそれらを攻撃的な腫瘍へと駆り立て、なぜこれらの腫瘍は放射線で死ににくいのか?マウスの脳細胞で単一の構造タンパク質を追跡することで、研究者らはその喪失がどのように染色体を不安定化させ、腫瘍の出現を早め、がんの幹様細胞が本来なら破壊されるはずの放射線を耐え抜くのを助けるかを明らかにしました。
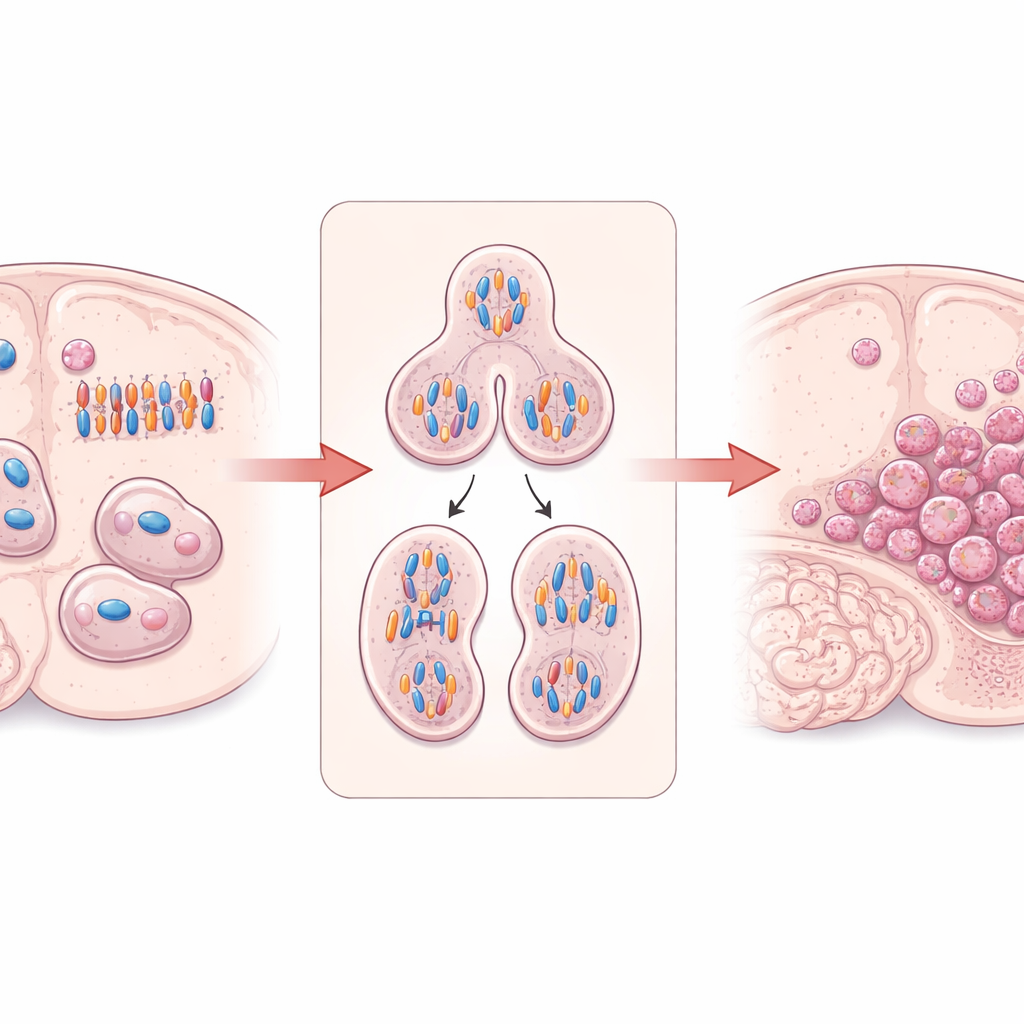
細胞分裂を整える“ビルダー”
本研究はDIAPH3に焦点を当てています。DIAPH3はアクチンフィラメントや微小管といった細胞内の足場を構築・整理するのに寄与するタンパク質です。分裂する脳の幹細胞では、DIAPH3は複製された染色体を引き離す紡錘体の形成や、細胞を二つに分ける過程に不可欠です。以前の研究では、発生中のマウス脳でDIAPH3が欠損すると、分裂中の細胞が染色体を誤って扱い、異常な染色体数(非整倍性)、細胞周期の停滞、細胞死を引き起こすことが示されていました。興味深いことに、DIAPH3遺伝子を含むヒト染色体13の小領域は膠芽腫で頻繁に欠失し、DIAPH3の高発現が一部の患者で予後良好と関連することから、このタンパク質が脳で腫瘍抑制因子として働く可能性が示唆されています。
腫瘍を生じさせるためのマウス脳の遺伝子操作
DIAPH3の喪失が実際に脳腫瘍を促進するかを確かめるため、研究チームは皮質を形成する幹細胞で選択的に二つの遺伝子を欠失できるマウスを作成しました:Diaph3と、よく知られたゲノムの番人であるp53をコードするTrp53です。この領域でDiaph3だけが欠損したマウスは、2年経っても腫瘍を発生させなかったため、p53が高度に異常な細胞を取り除けることを示唆します。対照的に、Trp53単独欠損、あるいはTrp53とDiaph3の両方が欠損したマウスは、最終的に顕微鏡下でヒトの病変に極めて類似した高悪性度のびまん性膠腫を形成しました。繰り返しの超高磁場MRIスキャンにより、両遺伝子を欠く動物は腫瘍を早期に検出され、寿命中盤までに嗅球に特に大型の膠腫を持つ頻度が、Trp53欠損のみのマウスより高いことが示されました。腫瘍の成長速度自体は発生後は両群で類似しており、変わったのは腫瘍が現れるまでの時間でした。
染色体の混乱と遺伝子発現の再配線
DIAPH3喪失がなぜ腫瘍の発症を早めるのかを探るために、研究者らは腫瘍が目に見える前の若いマウスの嗅球で遺伝子発現を調べました。Diaph3とTrp53の両方を欠く動物では、Trp53単独変異体と比較して126個の遺伝子が発現量に差を示し、そのうちほぼ半数が以前にがんと関連付けられていました。多くの変化はVEGF、MAPK、RAS、Rap1、cAMPシグナル伝達やGタンパク質共役受容体ネットワークを含む、細胞増殖、移動、血管新生を駆動する経路に集中しており、この分子学的変化は細胞がより早期にがん様状態へと押しやられていることを示唆していました。完全に形成された腫瘍の全ゲノムコピー数解析は、DIAPH3欠損が小さな局所的なDNA変化を大幅に増やすのではなく、むしろ大きな全染色体の獲得や喪失を増強していることを明らかにしました—これは染色体分配の不調から生じる非整倍性に一致します。
内在するDNA損傷とより頑強な腫瘍幹細胞
非整倍性の腫瘍細胞は、細胞核全体に広がるDNA切断マーカーγ-H2AXの上昇という形でより多くの内在的DNA損傷を抱えていました。それでもこれらの腫瘍が成長を続けたことは、損傷を許容する仕組みを獲得していることを示唆します。既に成立した腫瘍での遺伝子発現を比較すると、DIAPH3喪失により数百の遺伝子が変動しており、その中には多くの二重変異腫瘍でFGFR2という増殖因子受容体の著しい増幅と過剰発現が含まれていました。FGFR2は膠芽腫細胞のDNA修復機構を促進することが知られており、その活性化は放射線耐性と関連づけられています。チームはマウス腫瘍から膠腫の幹様細胞を分離し、臨床的に関連のある線量の電離放射線に対する応答を調べました。治療前は幹様細胞の頻度は両遺伝型で類似していましたが、照射後、DIAPH3欠損腫瘍由来の培養ではTrp53単独腫瘍由来よりおよそ2倍の活性な幹様細胞が残存し、より高い放射線抵抗性を示しました。
脳腫瘍にとっての意味
総じて本研究は、DIAPH3が脳の幹細胞が適正な染色体数で分裂することを助ける番人として機能することを描いています。DIAPH3とp53の両方が欠けると、細胞分裂は誤りやすくなり、全染色体の喪失や獲得が起こり、DNA損傷が蓄積します。細胞は死ぬのではなく、一部はFGFR2のような修復関連因子を増幅して適応し、非整倍性で高悪性度の膠腫へと変貌し、その幹様細胞は放射線に対して異常に耐性を持ちます。マウスモデルがヒト膠芽腫の全ての特徴を再現するわけではありませんが、これらの知見はDIAPH3が予後の潜在的バイオマーカーであり、腫瘍発生、ゲノム安定性、治療応答を制御する過程の結節点であることを支持します—将来的に既存治療をより効果的にするための新しい治療戦略の道を開く可能性があります。
引用: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
キーワード: 膠芽腫, 染色体不安定性, 脳腫瘍幹細胞, 放射線耐性, 腫瘍抑制遺伝子