Clear Sky Science · ja
GGCTが駆動する代謝の指揮:グルタミンをグルタチオン合成へ振り向けつつ、腫瘍増殖のためにブドウ糖のアナプレローシスを強化する
がん治療でこれが重要な理由
がん細胞は急速に増殖するため、大量の燃料を消費し、自らの代謝が生む有害な副産物から絶えず身を守らなければなりません。本研究は、あまり知られていない酵素GGCTが肝臓や前立腺の腫瘍で、グルタミンとグルコースという二つの一般的な栄養素を巧みに振り分け、増殖を支える一方で活性酸素種と呼ばれる有害分子を抑えるのに役立っていることを明らかにします。この代謝の綱渡りを理解することは、腫瘍を飢餓状態にする、または防御を突破する新たな治療戦略を開く可能性があります。
腫瘍細胞が燃料と防御を両立させる方法
腫瘍細胞はグルタミンに強く依存しています。グルタミンは二重の役割を果たし、細胞の主要なエネルギー産生サイクルに分解されて供給源となるだけでなく、強力な抗酸化物質であるグルタチオンの前駆体にもなります。著者らはまず、肝臓の腫瘍でグルタミン濃度が周辺の正常組織より高いこと、そしてより多くのグルタミンで培養されたがん細胞がシャーレ内およびマウス内でより速く分裂することを確認しました。グルタミンが不足すると、細胞は成長を鈍らせ、主要な細胞周期タンパク質が減少し、動物の腫瘍は縮小します—部分的には抗酸化防御が弱まり活性酸素が蓄積するためです。
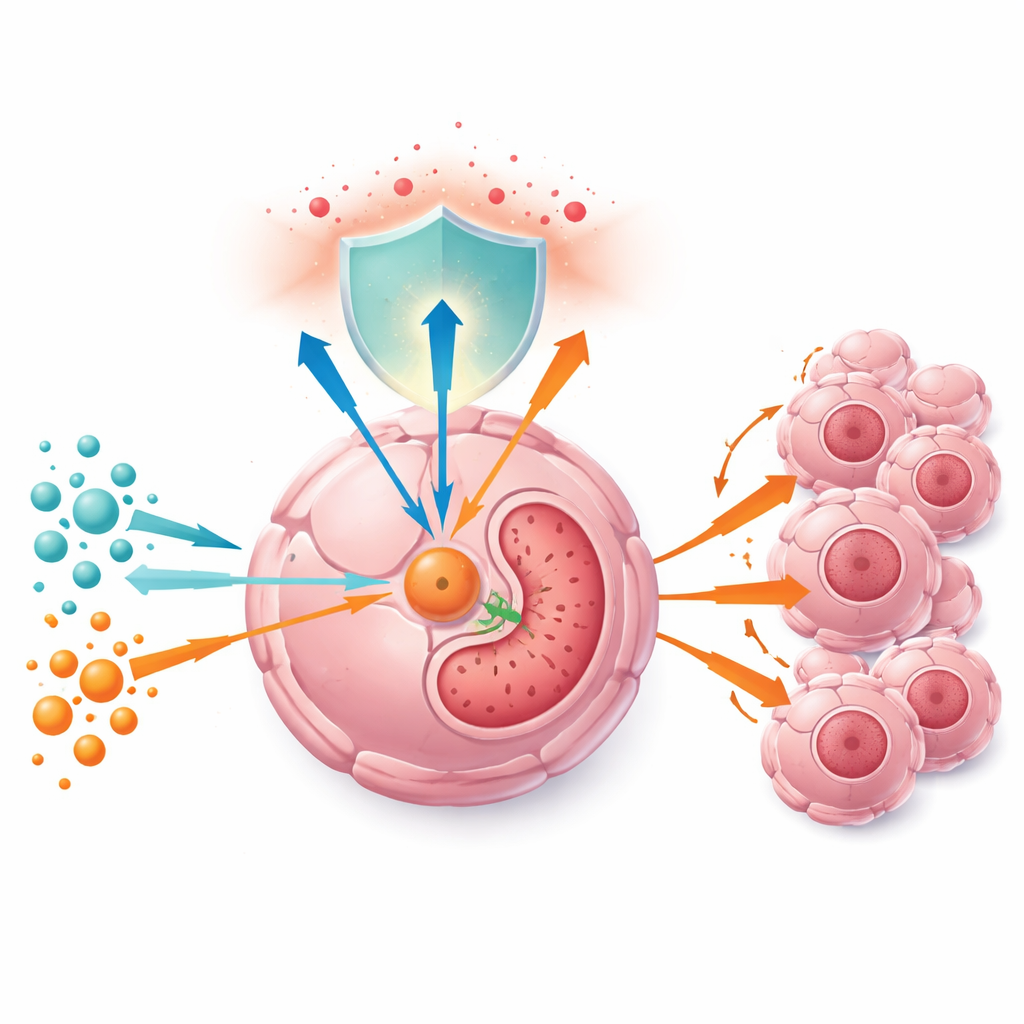
見過ごされていた代謝スイッチ
患者試料と大規模がんデータベースを横断的に調べると、酵素GGCTは正常組織に比べて肝臓および前立腺腫瘍で一貫して多く発現しており、GGCTの高発現は予後不良を予測することがわかりました。腫瘍試料と培養細胞の両方で、GGCTのレベルはグルタミン濃度とともに上昇し、腫瘍がこのタンパク質を通じてグルタミンの利用可能性を“読み取って”いることを示唆します。研究者らは制御の連鎖を解明しました:グルタミンは増殖促進因子c‑Mycを活性化させ、c‑Mycは小さな制御RNAであるmiR‑29b‑3pを抑制します;miR‑29b‑3pが低いとGGCTの抑制が解除されて蓄積します。グルタミン不足ではこの連鎖が逆転し、miR‑29b‑3pが上昇してGGCTのメッセージがより速く分解され、酵素レベルが低下します。
グルタミンの振り分けとより多くのブドウ糖の取り込み
GGCTが細胞内で実際に何をしているかを調べるために、著者らはその発現を低下または増強させ、細胞挙動と数百に及ぶ代謝物を測定しました。GGCTをサイレンシングすると細胞は分裂サイクルで停滞し、コロニー形成が縮小し、グルタチオンは著しく低下し活性酸素は増加しました;化学的抗酸化剤の添加は成長を部分的に救済しました。顕微鏡下でミトコンドリアは異常に伸長し酸素消費効率が低下し、それに対して細胞は糖分解(グリコリシス)を増強して補償しようとしました。詳細な代謝プロファイリングは、GGCTが失われると中央のエネルギーサイクルの中間体が減少し、過剰発現では増加することを示しました。
炭素原子の行方をたどる
次にチームは、標識したグルタミンとグルコースの原子が腫瘍代謝をどのように流れるかを追跡しました。GGCTを過剰発現させると、標識グルタミンがエネルギーサイクルへ行く割合は減り、代わりに新たに合成されたグルタチオンへより多く振り向けられ、抗酸化防御を支えました。同時に、標識ブドウ糖はサイクルへの寄与を強め、振り向けられたグルタミンを補っていました。正常な酵素活性を欠くGGCTの変異体はこれらのシフトも増殖促進も引き起こせず、GGCTの触媒機能が重要であることを示しました。重要な点として、ピルビン酸の追加やエネルギーサイクルへの流入を調整すると細胞のエネルギー水準は回復したものの、活性酸素は低下せず、GGCTが主にエネルギー供給の単純な変化ではなくグルタチオンを介してレドックスバランスを制御していることが示されました。
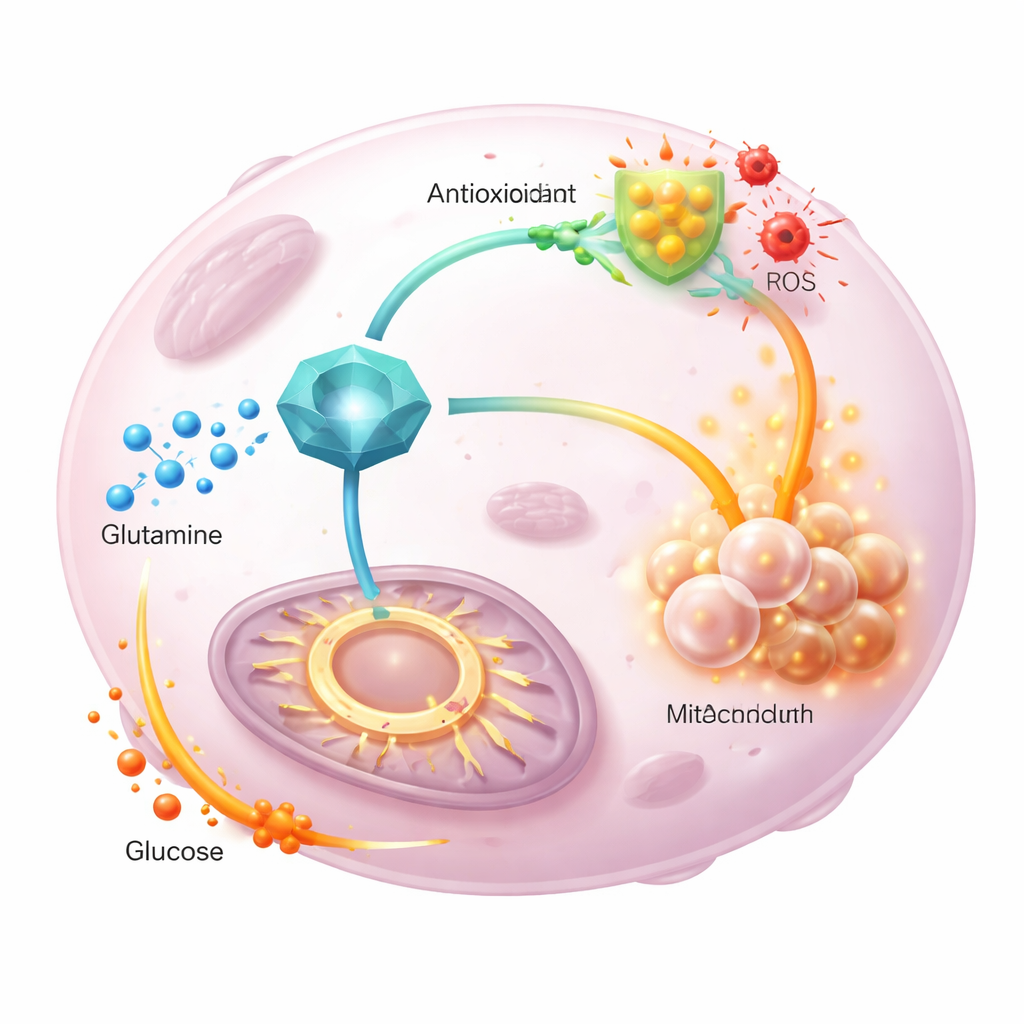
将来の治療への示唆
総じて、本研究はGGCTを中心的な調整者として位置づけます。GGCTはグルタミンの役割を分割させ、より多くを抗酸化物質合成へ振り向ける一方で、ブドウ糖をエネルギーサイクルへ引き入れて細胞分裂を維持させます。動物モデルではGGCTをノックダウンすると腫瘍増殖が遅くなり、グルタチオンが減少し酸化ストレスが上昇し、これらの効果は抗酸化薬で部分的に逆転しました。一般の読者に向けた要点は、一部のがんがGGCTを代謝の切替盤として利用して生き延びていることであり、このスイッチを無効化する薬は腫瘍の酸化ダメージに対する防御を脆弱にすると同時に栄養素の柔軟な利用を乱し、既存の治療をより効果的にする可能性があるということです。
引用: Yang, L., Sun, H., Wang, R. et al. Metabolic orchestration driven by GGCT: diverting glutamine to glutathione biosynthesis while enhancing glucose anaplerosis for tumor proliferation. Cell Death Dis 17, 358 (2026). https://doi.org/10.1038/s41419-026-08619-y
キーワード: がん代謝, グルタミン, グルタチオン, 酸化ストレス, GGCT酵素