Clear Sky Science · ja
脂肪細胞への分化誘導はEMT高発現の膵管癌細胞を静止した脂肪様状態へと再プログラムし、転移を抑制する
攻撃的ながん細胞を無害な脂肪に変える
膵臓がんは早期に広がり、標準治療に耐性を示すことが多いため最も致死率の高いがんの一つです。本研究はまったく異なる発想を探ります。すなわち、腫瘍細胞を毒殺したり飢餓状態に追い込むのではなく、最も危険ながん細胞を分裂せず体内を移動しない脂肪様の細胞へと誘導できないだろうか、というものです。研究者たちは、非常に攻撃性の高い膵臓がん細胞を安定した脂肪細胞様の状態へと押し込み、マウスにおいて腫瘍成長を遅らせ転移を減らしたことを示し、この難治性疾患を制御する新たな手法の可能性を示唆しています。
なぜ膵臓がんは止めにくいのか
膵管腺癌は膵臓がんの主要な型であり、予後は極めて不良です:診断から5年生存する患者はおよそ8人に1人しかいません。問題の一端は、多くの腫瘍細胞がEMTと呼ばれる形質可塑性の高い状態にあり、これが細胞の運動性、侵襲性、薬剤耐性を高めていることです。この状態を駆動する多数のシグナルを阻害する試みは限られた効果しか上げていません。一方で、膵臓やその腫瘍が脂肪細胞を蓄積する傾向を示すことが知られており、この細胞同一性の柔軟性を利用できるかもしれないという疑問がわきます。著者らは、EMTが強い膵臓がん細胞はすでに変化する準備ができている可能性があり、それらを侵襲的な状態ではなく、穏やかな脂肪様の同一性へと再方向付けできるのではないかと考えました。
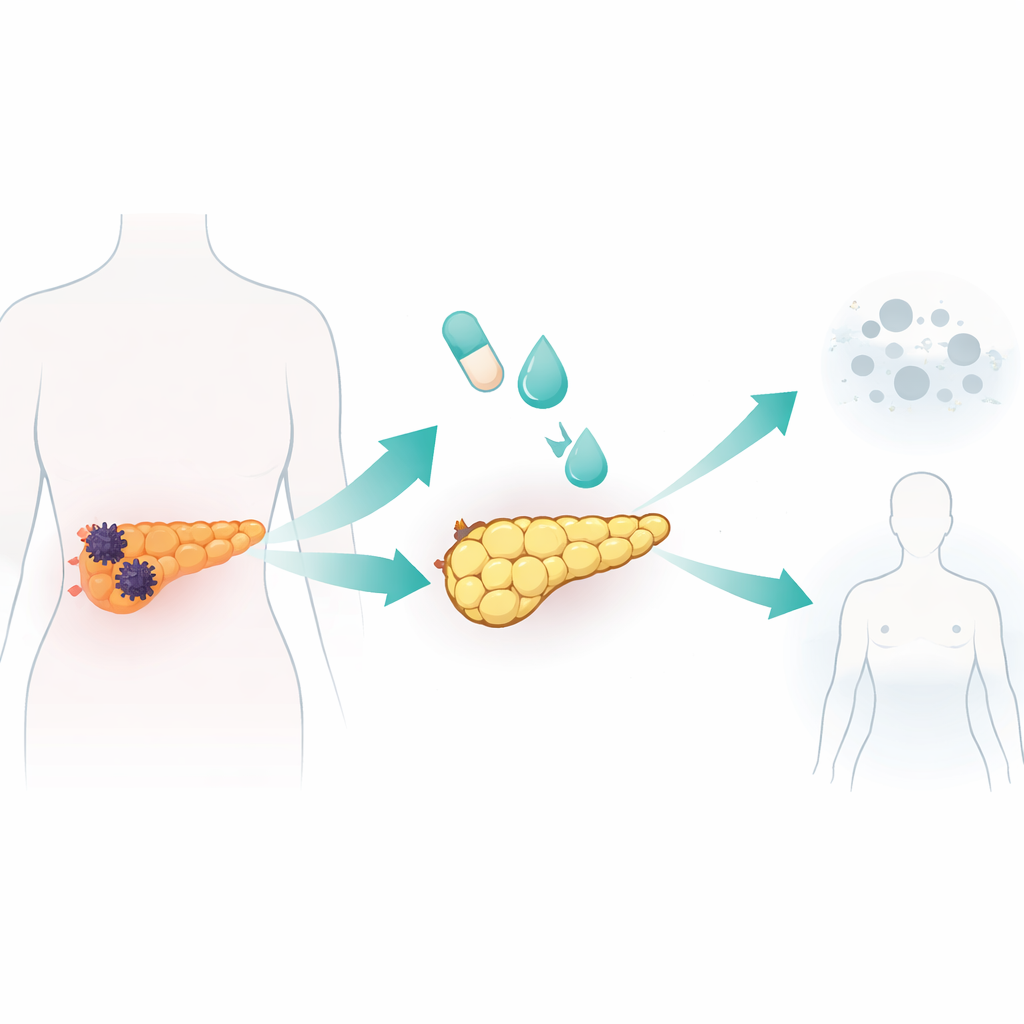
培養下でがん細胞を脂肪様細胞へ再プログラムする
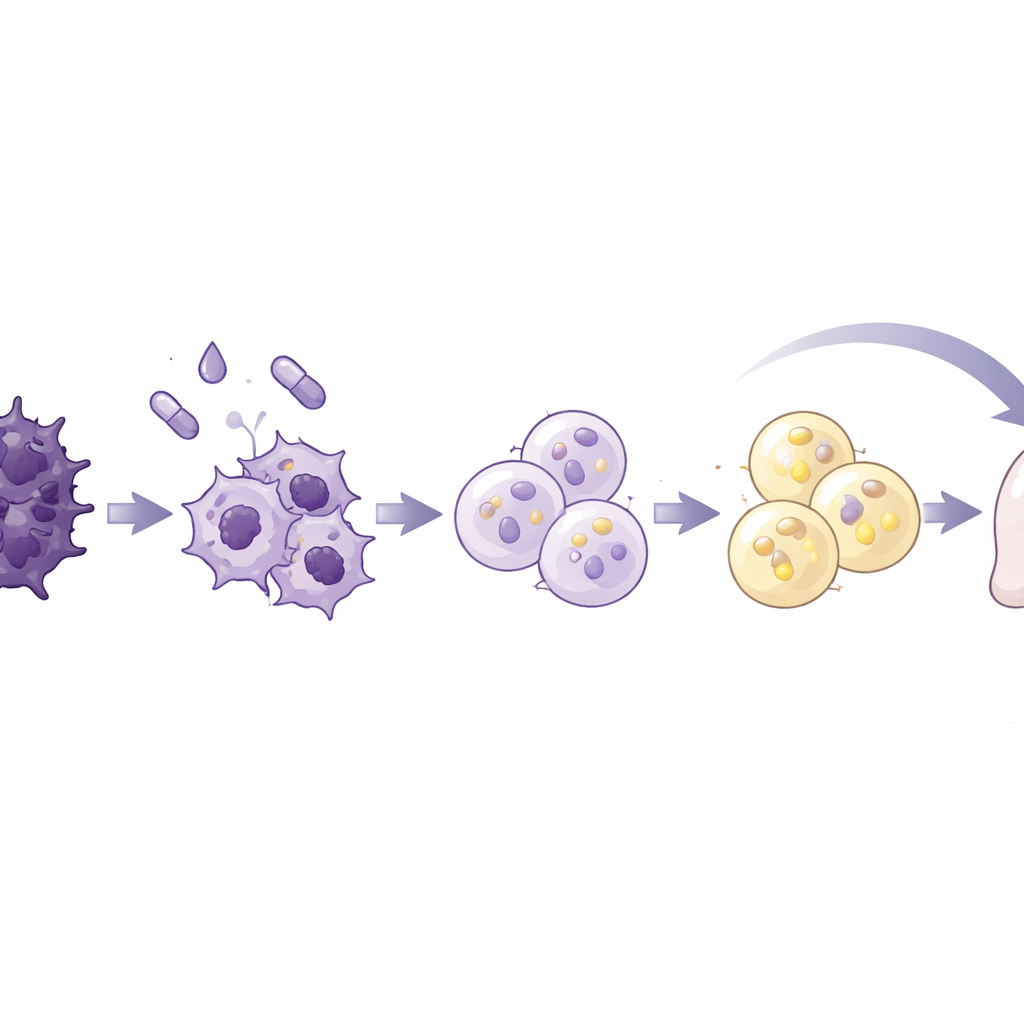
研究チームは、脂肪生物学や乳がん研究で用いられてきた標準的な脂肪分化カクテルを7種類のヒト膵臓がん細胞株と1つの正常膵臓細胞株に適用しました。この混合物はインスリンとステロイド、脂肪のマスターレギュレーターを活性化する薬剤ロシグリタゾン、そして細胞可塑性を解放するシグナルタンパク質BMP2を組み合わせたものでした。とくにAsPC-1というがん株が強く反応しました。10日間でこれらの細胞は大きく丸くなり、脂質滴で満たされるようになり、脂肪細胞の特徴を示しました。成熟脂肪細胞に典型的な遺伝子やタンパク質が発現し、アディポネクチンの分泌や貯蔵脂肪の動員といった脂質代謝も活性化しました。重要なのは、これら転換された細胞が増殖を停止し、細胞周期の早期段階で滞留し、未処理のがん細胞に比べて移動や侵襲が大幅に減少したことです。
細胞内部のがんプログラムを封じる
分子レベルで何が起きているかを調べるため、研究者らは転換後の細胞のDNAパッケージングと遺伝子発現を解析しました。クロマチン(遺伝子アクセスを制御するDNA–タンパク質複合体)が全般的に締め付けられ、遺伝子発現が全体的に低下するという、非増殖細胞に特徴的な変化が見られました。マトリックス分解酵素や主要なEMT制御因子を含む、EMT、侵襲、転移を支持する遺伝子は強く抑制される一方で、脂肪関連遺伝子は増強されました。全体の遺伝子シグネチャーは、間葉様で高移動性の同一性から成熟脂肪細胞に近いものへと移行しました。細胞増殖や主要なEMT駆動因子であるTGF-βへの応答に結び付くシグナルは抑えられ、脂質処理や細胞接着に関連する経路は強化されました。これらの変化は、単に速度が落ちただけでなく、細胞の同一性が根本的に書き換えられたことを示唆します。
マウスで戦略を検証する
次に研究者らは、この強制的な脂肪様転換が生体内で腫瘍制御に寄与するかどうかを調べました。ヒト膵臓がん細胞をマウスの膵臓または脾臓に移植して原発腫瘍と肝転移のモデルを作成しました。ロシグリタゾンとBMP2で処理したマウスは膵腫瘍が小さくなり、腫瘍内に豊富な脂質滴と脂肪細胞マーカーが認められ、EMTや侵襲関連遺伝子のレベルが低下しました。転移モデルでは、治療は初期の腫瘍播種には影響しなかったものの、時間とともに肝臓の腫瘍負荷の拡大を未治療群と比較して遅らせました。重要なのは、周辺の正常膵臓組織には明白な脂肪様転換が見られず、腫瘍内の脂肪様状態は薬剤中止後少なくとも1か月持続したことから、ある程度の持続性と特異性が示唆された点です。
将来のがん治療にとっての意義
本研究は刺激的な概念を支持します:可塑性が高くEMTに富む膵臓がんに対しては、「殺すのではなく変換する」ことで、危険で遊走しやすい腫瘍細胞を安定した非分裂の脂肪様細胞へ向け直し、転移しにくくすることが可能かもしれません。これは細胞とマウスモデルでの初期段階の研究であり、すべての膵臓がんが同じように反応するわけではありませんが、増殖シグナルを単に遮断するのではなく細胞同一性を変えることによって作用する新しい治療の道を開きます。将来的には、このような転換分化アプローチを標的薬や免疫療法と組み合わせることで、膵臓がんをより静かで管理しやすい状態に保ち、致命的な転移のリスクを減らす可能性があります。
引用: Qian, Y., Yan, Z., Wang, J. et al. Adipogenic transdifferentiation reprograms EMT-high PDAC cells into a post-mitotic adipocyte-like state and limits metastasis. Cell Death Dis 17, 330 (2026). https://doi.org/10.1038/s41419-026-08613-4
キーワード: 膵臓がん, 細胞可塑性, 転換分化, 上皮―間葉転換, 脂肪様細胞