Clear Sky Science · ja
新規ビグアナイド4CによるEGFR抑制がBRCA2およびRad51のダウンレギュレーションを介して卵巣がんのPARP阻害剤感受性を高める
この研究が重要な理由
卵巣がんと診断された多くの人にとって、現在の標的薬は腫瘍が特定の遺伝的欠陥を持つごく少数の患者にのみ有効です。本研究は、PARP阻害剤と呼ばれる重要な薬剤群の恩恵を、そうした変異を欠くより大多数の患者にまで広げる方法を探ります。新規の実験化合物を既存薬と組み合わせることで、研究者たちはがん細胞を致命的な行き止まりに追い込みつつ、健康な組織をなるべく温存する戦略を示しています。
現行の卵巣がん治療における障害
卵巣がんは発見が遅れることが多く、女性に影響を与える最も致死率の高いがんの一つです。オラパリブのようなPARP阻害剤は著しく有効な場合がありますが、主にBRCA1やBRCA2に関連するDNA修復経路に欠損のある患者に限られます。しかし、ほとんどの腫瘍は修復機構が健全であり、これらの薬剤が引き起こすDNA損傷を修復してがん細胞が生き残ってしまいます。修復チームの重要な構成要素として、BRCA2とRad51という2つのタンパク質があり、相同組換えと呼ばれる過程で切断されたDNA鎖を修復します。がん細胞でこの修復経路を選択的に弱める方法を見つければ、PARP阻害剤をはるかに多くの患者に有用にできる可能性があります。
よく知られた増殖スイッチの役割
研究チームは、腫瘍細胞表面に存在し増殖を促すことで知られる表皮成長因子受容体(EGFR)に着目しました。彼らは、EGFRが成長シグナルを送るだけでなく、正常なBRCA遺伝子を持つ卵巣がん細胞ではEGFRの高発現が患者生存率の低下やPARP阻害剤への耐性と結びついていることを見出しました。培養細胞やマウスでEGFRを減らしたり抑えたりすると、腫瘍はオラパリブに対してはるかに脆弱になりました。研究者たちは、EGFRがDNA損傷後にBRCA2とRad51を細胞核へ送り込み、そこで切断部位を修復して治療の影響を緩和していることを示しました。EGFRの酵素活性を単に阻害するだけでは不十分であり、この修復経路を大きく乱すにはEGFRタンパク質の総量を低下させる必要がありました。
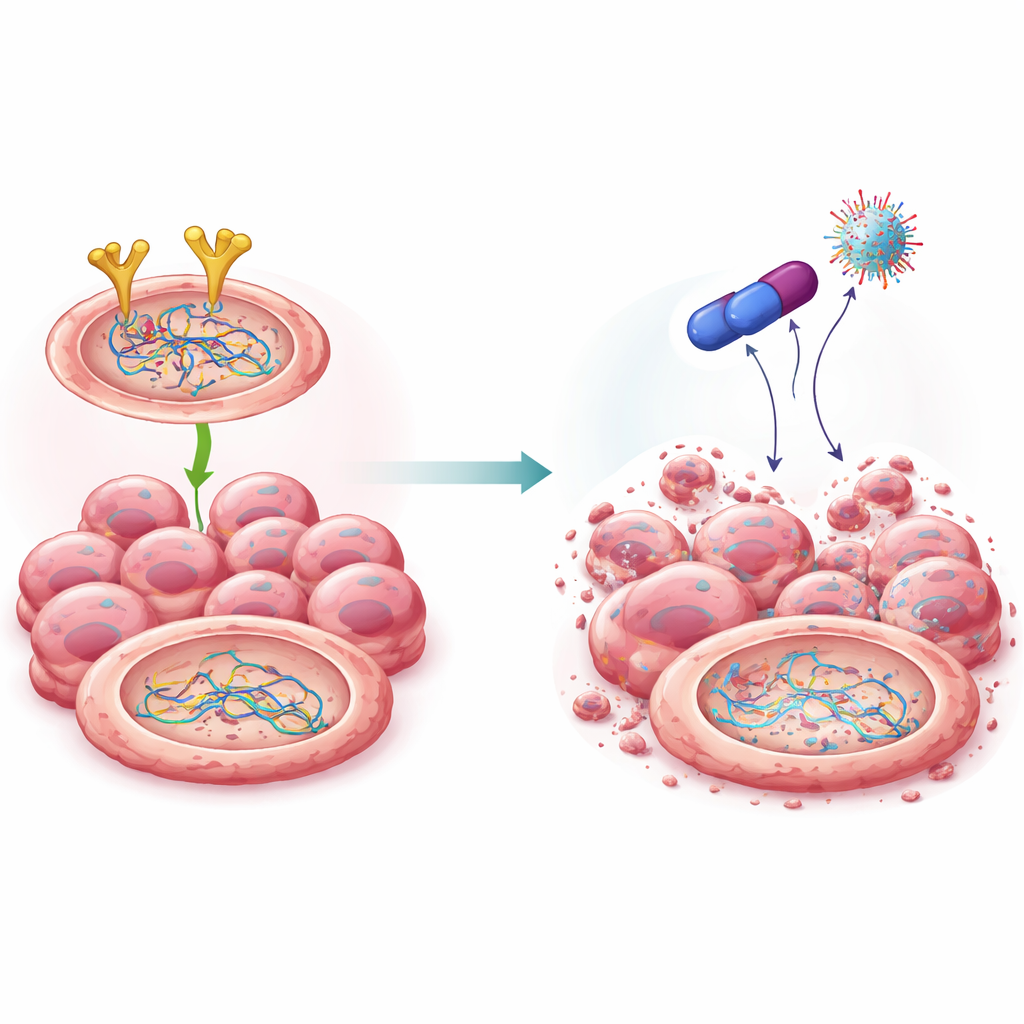
修復チームを無力化する新規化合物
ビグアナイド群に関する先行研究を基に、科学者たちはいくつかの化学的類縁体を合成し、その中で際立った分子4Cを同定しました。この化合物は卵巣がん細胞に強い毒性を示す一方で、正常細胞には比較的穏やかでした。計算モデルと実験により、4CがEGFRに直接結合し、細胞のタンパク質分解機構によってEGFRを破壊するよう標的化することが示唆されました。既存の一部のEGFR薬とは異なり、4Cは活性を単に抑えるのではなくEGFRの総量そのものを減少させました。EGFRレベルが低下するとBRCA2とRad51の安定性も低下し、これらは分解の標的となり、効率的なDNA修復を支えられなくなりました。重要なのは、この剪定が遺伝子そのものを変えるのではなくタンパク質レベルで起きていることです。
細胞内の救済経路を遮断する
本研究は、DNA損傷と腫瘍生存を結ぶより詳細な一連の出来事を明らかにしました。PARP阻害剤がDNAを傷つけると、別のセンサー蛋白質であるATMが核から細胞質へ信号を送ります。これに応じてEGFRはBRCA2やRad51と結びつき、これらを核へ移行させ修復を行わせます。研究者たちは、c-Cblという第三のタンパク質が通常BRCA2やRad51の破棄をタグ付けする働きをしていることを見出しました。EGFRはこれら修復タンパク質へのアクセスを巡ってc-Cblと競合し、破壊の標的にされるのを防いでいました。4CがEGFR量を低下させると、c-CblはBRCA2やRad51により容易に結合できるようになり、タグ付け・分解・喪失が進みます。核内の修復タンパク質が減るとDNA傷害が蓄積し、がん細胞はPARP阻害剤に対して格段に感受性を増します。
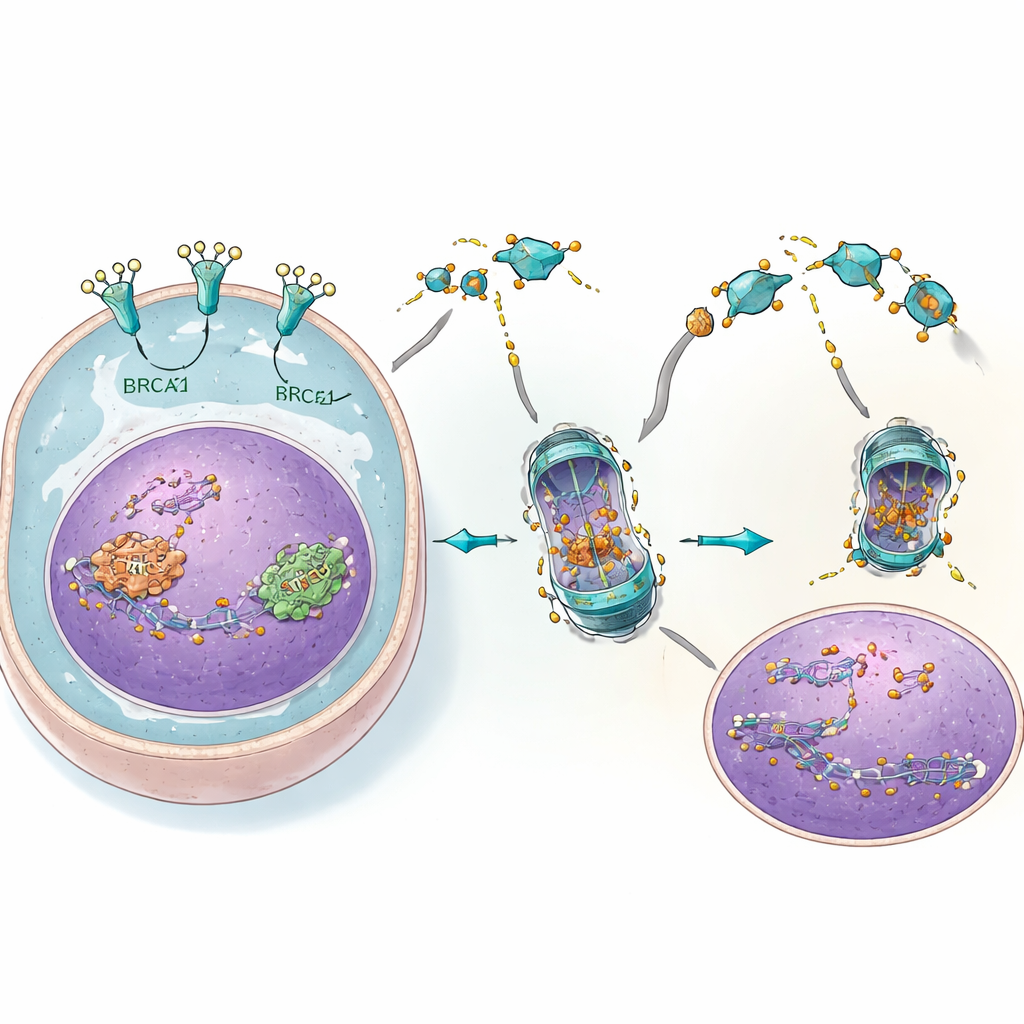
細胞から動物へ:強力な組み合わせ療法
培養細胞とマウスモデルの両方で、4CとPARP阻害剤の併用は強力な相乗効果を示しました。単剤では抵抗性を示したBRCA遺伝子が正常な腫瘍が、両剤を併用すると劇的に縮小するか増殖が停止しました。DNA損傷のマーカーは急増し、修復機構が圧倒されていることが示唆されました。同時に、肝臓や腎臓などの主要な臓器や正常細胞にはほとんど有害な影響が見られず、これはそれらがEGFRレベルが低くこの特定の修復ショートカットに依存していないためと考えられます。この併用の利益は卵巣がん細胞の体内への広がりを抑える効果にも及びました。
患者にとっての意義
本研究は、がん細胞の強みを弱点へと転換する方法を示唆します。新規化合物4CでEGFRを標的とすることで、研究者たちはBRCA2とRad51が提供する保護をはぎ取り、遺伝的に修復機構が正常な腫瘍をPARP阻害剤に対してBRCA変異腫瘍のように振る舞わせることに成功しました。この強制的な脆弱性、いわゆる「合成致死」は、既存薬の適用範囲を多くの卵巣がん患者に広げ、副作用を管理可能なままにする可能性があります。4Cはまだ実験段階であり、より進んだモデルや臨床試験での広範な検証が必要ですが、本研究は腫瘍細胞内の特定の修復補助因子を解体することで治療成績を改善する明確な設計図を示しています。
引用: Xiao, D., Yao, J., Yang, X. et al. Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51. Cell Death Dis 17, 317 (2026). https://doi.org/10.1038/s41419-026-08556-w
キーワード: 卵巣がん, PARP阻害剤, EGFR, DNA修復, 標的治療