Clear Sky Science · ja
核内ミオシン1はゲノムの構造を脂肪組織の再編、代謝性炎症、マウスの肥満と結びつける
細胞の“骨格”が体脂肪に影響する理由
肥満はしばしば食事や運動不足のせいにされますが、細胞の奥深くではDNAの折りたたみ方や読み取り方も均衡を崩す要因になり得ます。本研究は、細胞核内でDNAの配置を助ける小さなモータタンパク質、核内ミオシン1(NM1)が、脂肪細胞の形成、エネルギー貯蔵、炎症の引き金に思いがけない役割を果たすことを明らかにしました。このタンパク質を欠くマウスを調べることで、遺伝子の物理的な配置と不健康な内臓脂肪や代謝障害の発生との直接的な結びつきが明らかになりました。
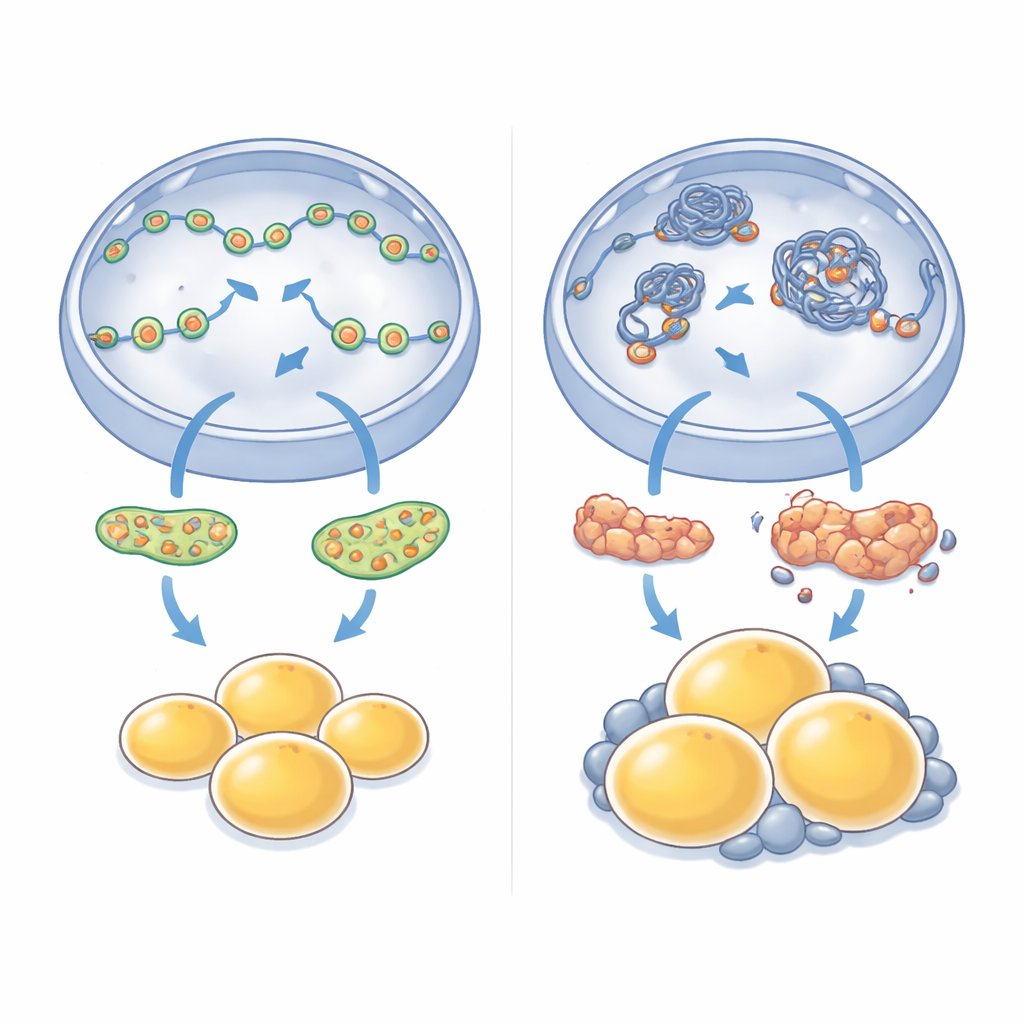
幹細胞から脂肪細胞へ
脂肪細胞は多様な前駆細胞である間葉系幹細胞から発生します。通常、これらの前駆細胞は増殖し、エネルギー利用を切り替え、多数の小さく機能的な脂肪細胞へと成熟して余剰のカロリーを安全に蓄えます。研究チームは、NM1がないとこの秩序だった過程が崩れることを見出しました。正常マウスとNM1欠損マウスから採取した幹細胞を培養して脂肪細胞化を誘導したところ、NM1欠損では移行を完遂する細胞が著しく少なくなりました。成熟した細胞も通常より明らかに大きく、脂肪を多く含む一方で、健康的な脂肪細胞に見られる遺伝子やタンパク質の指標を欠いていました。この「細胞数は少ないが個々は肥大する」というパターンは、不健康な脂肪組織の特徴です。
遺伝子の折りたたみ方が脂肪細胞の振る舞いをどう形作るか
NM1は核内で働き、重要な遺伝子がオンになるようにDNA領域のアクセス性を保つのに寄与します。NM1喪失が細胞挙動をどう変えるかを知るために、研究者らはオープンなDNA領域のマップとNM1のある細胞とない細胞での遺伝子発現データを重ね合わせました。その結果、脂肪細胞形成、脂滴の取り扱い、ミトコンドリアの維持に必要な多くの遺伝子が、NM1欠損時にアクセス性と発現の両方を失っていることがわかりました。同時に、成長やシグナル伝達に関わる他の遺伝子群はより開いた状態になり、発現が上がっていました。これはNM1が重要な交通整理役であり、適切な遺伝子ネットワークが健康的な脂肪細胞の発達と代謝を促すように、開閉のバランスを維持していることを示します。
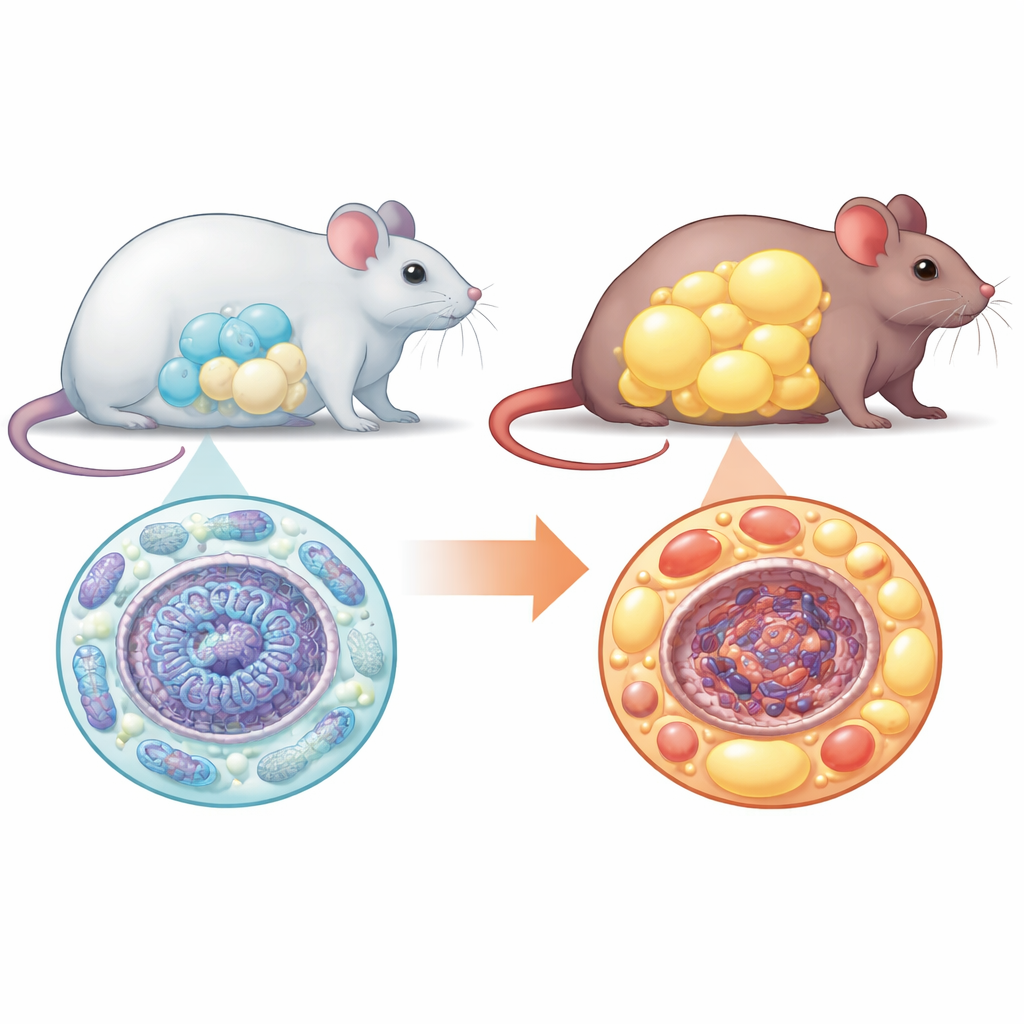
局所的変化が全身の体重増加へと広がるとき
この単一の核内モータを失った影響はシャーレ内の細胞にとどまりませんでした。NM1欠損マウスは、食べる量が増えていないにもかかわらず、徐々に正常な同腹仔よりも体重が増加しました。スキャンや組織解析では、特に腹部の内臓周りに脂肪が明らかに蓄積しており、これらの部位の個々の脂肪細胞は著しく肥大していました。内臓脂肪でどの遺伝子が上昇または抑制されているかを調べると、エネルギー利用、インスリンシグナル、組織再編に関わる経路が広範に再プログラムされていることが分かりました。脂肪細胞の成長や拡張に関連する遺伝子はしばしば増強され、一方で健康的な脂肪細胞形成の中心的な制御因子はいくつか抑えられており、培養した幹細胞で見られた欠陥と一致していました。
炎症を伴う脂肪と乱れたエネルギー機構
大きさ以上に、NM1欠損マウスの脂肪組織は炎症と代謝ストレスの兆候を示していました。詳細な経路解析は、インターフェロンγや腫瘍壊死因子のような分子によって駆動される免疫シグナルの強い活性化を浮き彫りにし、これらはインスリン抵抗性や代謝性疾患に寄与することが知られています。同時に、落ち着いてエネルギー効率の良い脂肪組織を支える調節因子は抑制されていました。さらに研究は、NM1の喪失がミトコンドリア──細胞のエネルギーエンジン──の乱れと結びつくことを示しました。ミトコンドリアの品質管理や効率的なエネルギー産生と迅速な解糖への切り替えを通常監督する遺伝子群が誤調節されており、NM1が欠けると脂肪細胞がより効率の悪い、ストレスに弱いエネルギー戦略をとることを示唆しています。
マウスとヒトに共通するシグナル
この核内モータ経路が人にも関係するかを問うために、著者らはヒトの内臓脂肪に関する大規模な遺伝データセットを調べました。彼らはNM1のヒト相同であるMYO1Cに注目し、周辺遺伝子の活性を調節するバリアントのネットワークを解析しました。すると、マウスで見られた多くのテーマ──細胞骨格制御、免疫シグナル、代謝調節──がMYO1Cを中心としたヒトの遺伝子ネットワークにも現れていました。NM1欠損のマウス脂肪で変化したいくつかの遺伝子は、このヒトのネットワークにも組み込まれており、脂肪組織の再編や代謝に関連づけられています。この種を超えた重なりは、類似した核内の仕組みがヒトの肥満リスクに影響を与え得ることを示唆します。
肥満と代謝健康にとっての意義
総じて、この研究はNM1が単なる核内の補助因子以上の存在であり、DNAの組織化と脂肪細胞の成長、エネルギー貯蔵、免疫系との対話をつなぐ中心ハブであることを示しています。NM1が欠けると、脂肪前駆細胞の遺伝子スイッチが誤設定され、ミトコンドリア機能が低下し、脂肪細胞は増殖する代わりに肥大し、内臓脂肪は炎症を帯びる──これは肥満やインスリン抵抗性で見られる不健康な脂肪に類似した組み合わせです。一般読者へのメッセージは、核内のDNAの物理的配置とその補助因子が、組織を健康的な拡張へ導くか有害な拡張へ導くかを左右し得るということです。NM1やそのヒト相同体MYO1Cのようなタンパク質は、いずれ脂肪組織を内側から再形成することを目指した治療の標的となり、肥満関連疾患に対するより精密な対策を提供する可能性があります。
引用: Khalaji, S., Venit, T., Lukáčová, Z. et al. Nuclear Myosin 1 links genomic architecture to adipose tissue remodeling, metabolic inflammation and obesity in mice. Cell Death Dis 17, 270 (2026). https://doi.org/10.1038/s41419-026-08525-3
キーワード: 脂肪形成, クロマチン, ミトコンドリア, 内臓脂肪, 代謝性炎症