Clear Sky Science · ja
SETD2によるヒストン3リジン36の三重メチル化は腸幹細胞のエピジェネティックな風景を形作り、脂質代謝を調整して細胞老化を緩和する
加齢とともに腸の幹細胞が重要である理由
腸の内層の奥深くでは、小さな幹細胞が休むことなく組織を更新し、私たちが食物を消化し栄養を吸収するのを助けています。加齢とともにこれらの幹細胞は疲弊し、腸は病気に対して脆弱になり、修復が遅くなります。本研究は、DNAを包むタンパク質に付く微妙な化学的標識が腸幹細胞を若々しく保つしくみ、その喪失が細胞内の脂肪燃焼をどのように乱すか、そして慎重に選ばれた薬剤がいつかこの衰えを遅らせる可能性があるかを探ります。
過酷な環境にある老化する細胞
腸の内面は体内で最も速く再生する組織のひとつです。クレフトと呼ばれる小さな窪みの底にある幹細胞は、数日ごとに何十億もの細胞を置き換えるために分裂します。この絶え間ない仕事には脂肪の分解など多くのエネルギー供給が必要です。同時に、これらの幹細胞はヒストンタンパク質上の化学的標識――どの遺伝子が活性化または抑制されるかを決める“エピジェネティック”コード――によって制御されています。著者らはその中でもH3K36三重メチル化と呼ばれる標識に注目し、SETD2という酵素がこの標識を作ることから、加齢に伴う腸幹細胞の活力低下がこの標識の変化と結びつくかを検討しました。
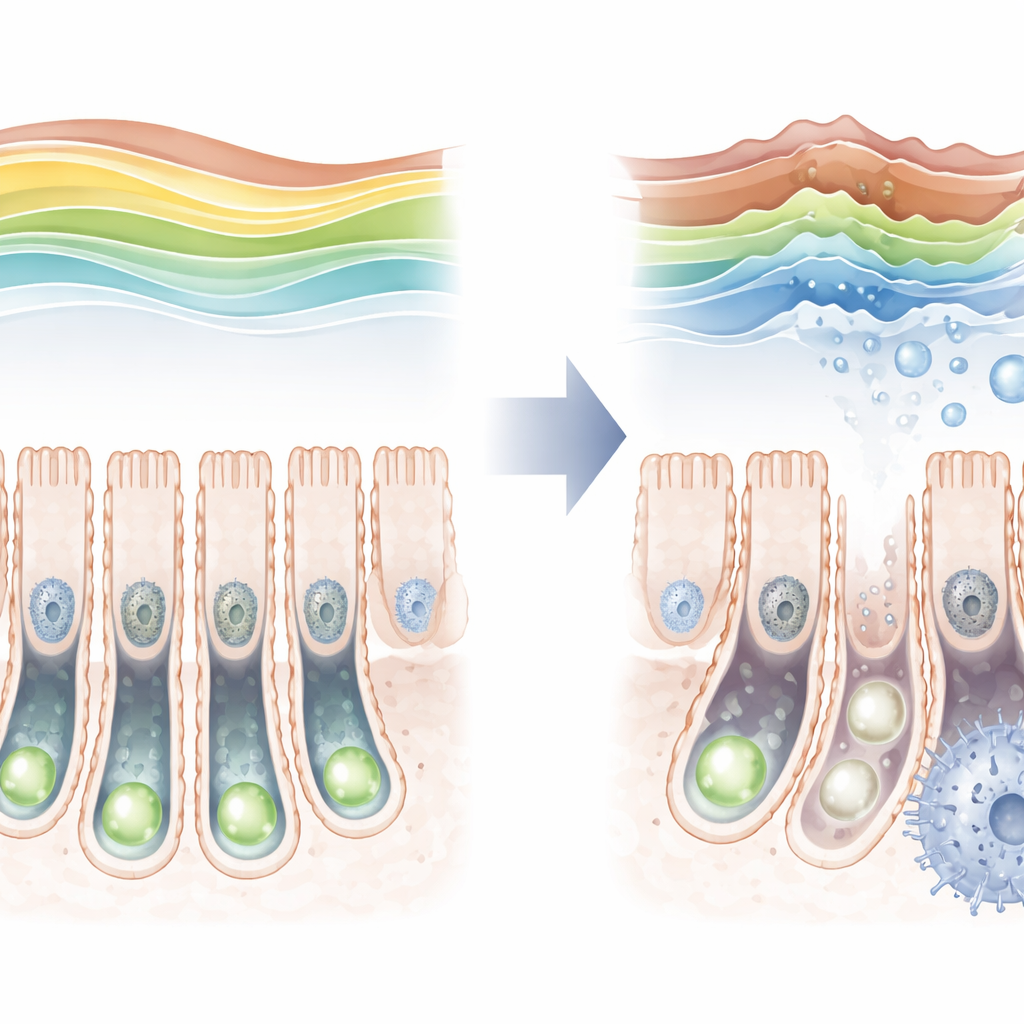
年齢とともに薄れる保護的な標識
研究者たちはマウスの腸を生涯にわたって調べ、H3K36三重メチル化が静的ではないことを見いだしました。出生直後は比較的低く、若年期にピークに達し、高齢になると再び低下します。この標識が高齢の個体で低下するにつれて、幹細胞内の老化マーカーが増加し、両者の関連を示唆しました。より直接的に検証するため、研究チームはSETD2を腸幹細胞に限って除去できるように遺伝子改変マウスを作成しました。この酵素を欠くと保護的な標識はほぼ消失し、幹細胞の分裂頻度は下がり、腸の専門化した細胞群を完全に生み出すのが困難になりました。
エピジェネティック変化が脂肪燃焼をどのように混乱させるか
この単一のヒストン標識の喪失は、幹細胞内で一連の変化を引き起こしました。遺伝子発現の測定では細胞周期やDNA複製に関わる多くの遺伝子が抑制され、ストレスや老化に関連する遺伝子は上方制御されていました。特に顕著だったのは脂質処理の乱れです。通常は脂肪酸酸化を支える遺伝子群が低下し、クレフト内に脂質が蓄積し始めました。代謝物プロファイリングは長鎖脂肪酸の蓄積を確認し、通常の脂質代謝経路が機能不全に陥っていることを示しました。同時に核内でのDNAの詰まり具合(クロマチンの構造)も変化し、多くの領域がより開放的またはより緊密になり、細胞が利用しやすい遺伝子群の構成が再編されました。
クロマチンリモデラーと老化への進行
これらのDNAパッキング変化がどのように生じるかを理解するため、著者らはゲノム全体の開いたクロマチン領域と複数のヒストン標識をマッピングしました。H3K36三重メチル化が失われると、大規模なDNA領域が“活性”の標識を獲得してアクセス可能になり、とくに代謝や老化に関連する遺伝子近傍で顕著でした。この変化の主要な立役者の一つがSWI/SNFクロマチンリモデリング複合体で、その中核サブユニットSMARCA4が駆動していました。SETD2欠損の幹細胞ではSMARCA4の量が増加し、この複合体が老化プログラムを駆動する領域をこじ開けるのに寄与しているように見えました。研究者らが遺伝学的手法や標的阻害剤でSMARCA4活性を低下させると、幹細胞は培養でのミニ腸形成能をいくぶん回復し、老化マーカーが低下しました――過剰なリモデリングがこれらの細胞を疲弊した老化状態へと押しやっていることを示唆します。
エネルギー経路の再活性化で幹細胞を救う
脂肪燃焼の混乱が中心的問題として浮かび上がったため、チームはこの経路を活性化して幹細胞の老化に対抗できるかを試しました。彼らは脂肪酸酸化のマスター調節因子であるPPARαを活性化する薬剤を用いました。SETD2欠損の幹細胞から作ったオルガノイドでは、この処置により成長が促進され、活力ある幹細胞に特徴的な芽状構造が回復し、脂肪蓄積が減少しました。生体マウスでも同様の処置は幹細胞プールを部分的に回復させ、老化マーカーを低下させ、腸クレフト内の脂質蓄積を正常化しました。これらの所見は、脂肪酸酸化がエピジェネティック制御と幹細胞の健康をつなぐ重要な環であることを示しています。
健康的な加齢に向けての示唆
まとめると、本研究はSETD2が付加する特定のヒストン標識が腸幹細胞のバランスの取れたエピジェネティック環境を維持するのに寄与することを示しています。この標識が薄れるとクロマチンが異常にリモデリングされ、脂肪燃焼経路が障害されて脂質が蓄積し、細胞は老化へと傾き腸の修復機能が弱まります。過剰なリモデリング機構を抑えるか、標的化された薬剤で脂質代謝を回復することで、晩年における幹細胞機能と腸の健康を維持できる可能性があります。これらの発見はマウス由来のものであるものの、人間の腸疾患で見られるパターンとも呼応しており、慎重に調整された代謝治療がいつか私たちの腸幹細胞の加齢に対抗する助けとなる見通しを示しています。
引用: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
キーワード: 腸幹細胞, エピジェネティクス, 脂肪酸酸化, 細胞性老化, SETD2