Clear Sky Science · ja
ADSC由来のLamp2a結合RNAがENO1–ラクトイル化–解糖のフィードバックと三重陰性乳がんにおける細胞の悪性挙動を抑制する
患者にとってなぜ重要か
三重陰性乳がんは最も攻撃的な乳がんの一つで、他のサブタイプで有効なホルモンや成長因子を標的にした治療法が使えないため治療が難しい。本研究は、これらの腫瘍が低酸素環境で生き残るためにどのようにエネルギー利用を書き換えているかを明らかにし、その配線を狙う斬新な方法を示している。がん代謝を理解することで、従来の化学療法とは大きく異なる新たな高選択的治療法が生まれる可能性があることを示す内容である。
これらの腫瘍はどうやってエネルギーを得ているか
多くのがんは、糖を乳酸という副産物に変える速いが効率の低いエネルギー産生法である解糖に強く依存している。患者試料、公開遺伝子データベース、複数の乳がん細胞株を解析した結果、三重陰性腫瘍は他の乳がんよりもさらに解糖に依存していることが示された。この経路の重要な酵素であるENO1はこれらの腫瘍で特に高発現し、生存率の低下と関連していた。実験室でENO1の量を減らすと、三重陰性細胞は解糖からミトコンドリアでのより正常なエネルギー産生へとシフトし、増殖は遅くなり、浸潤やコロニー形成能力が低下した。
がん細胞内の危険なフィードバックループ
さらに掘り下げると、乳酸自体がENO1を強化し、がん細胞を悪循環に閉じ込めることがわかった。乳酸はタンパク質に化学修飾を与える乳酸化(ラクトリレーション)を引き起こす。三重陰性細胞では、過剰な乳酸がENO1の乳酸化を増加させ、それが酵素の活性と安定性を高め、さらに解糖を促進してより多くの乳酸を産生するという悪循環を生んでいた。固形腫瘍に典型的な低酸素条件下でこのループは強化され、細胞死に対する抵抗性や増殖継続を助ける。小分子阻害剤でENO1活性を阻害するか、乳酸生成を減らすことでこのループは弱まり、解糖が抑制され、マウスの腫瘍増殖が遅延した。
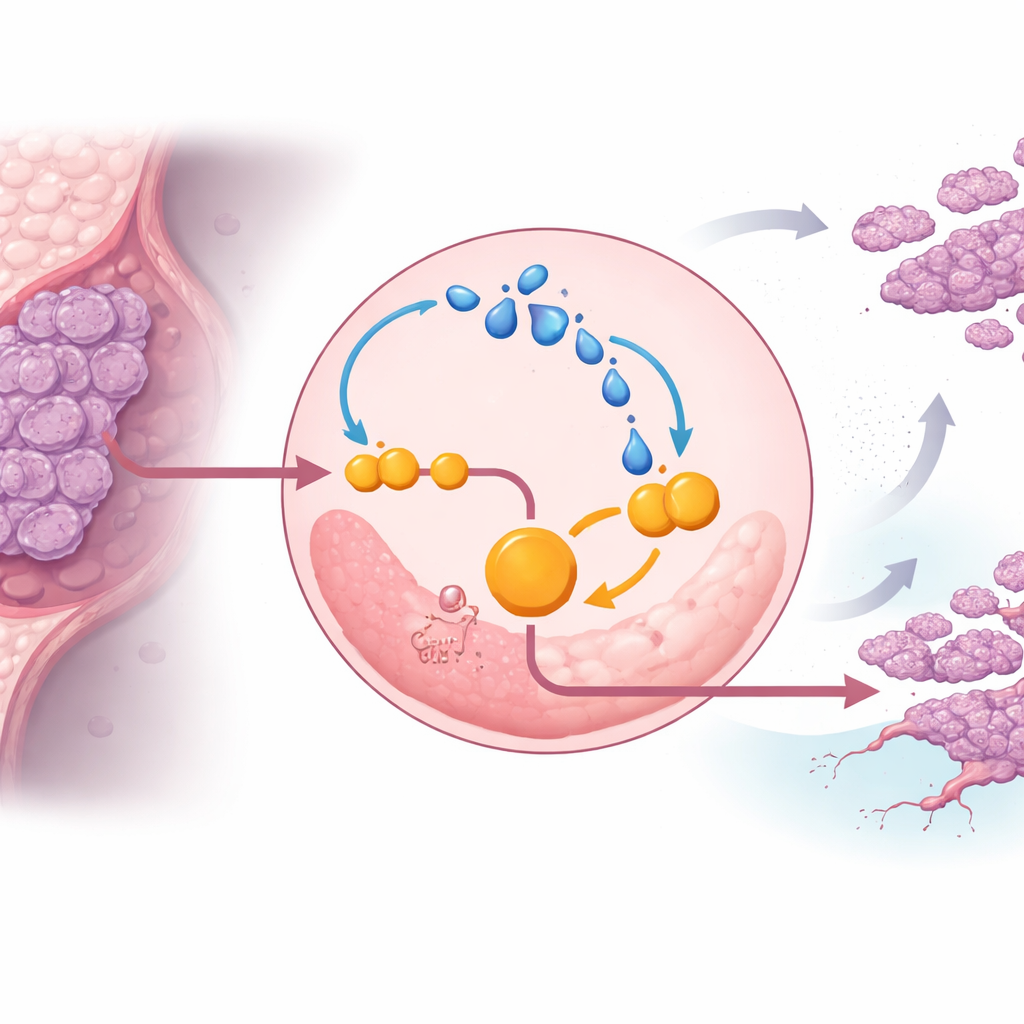
ENO1を保護する分子スイッチ
研究は、このループを可能にするENO1上の特定の制御点を同定した。EP300として知られるタンパク質がENO1のいくつかのリジン残基に乳酸由来のタグを付加し、そのうちK262と呼ばれる一つの部位が重要であることがわかった。この部位が乳酸化されなくなるよう変異させると、ENO1は迅速にリソソーム(細胞の分解装置)へ送られて分解された。この保護タグがないと、三重陰性細胞は解糖駆動力や動物モデルでの腫瘍形成・転移能力の多くを失った。つまりK262でのENO1乳酸化は、酵素を破壊から守り、がんの改変された代謝を維持する分子スイッチであることが示された。
ENO1を破壊する新たな方法
単にENO1を阻害するのではなく、著者らはがん細胞から選択的に除去する戦略を設計した。ENO1はRNA結合タンパク質としても作用し、特定の短いRNA配列を認識する。チームはENO1に強く結合する人工RNA断片を設計し、それを選択的タンパク質分解に関与するリソソーム膜タンパク質Lamp2aに結合させた。ヒト脂肪由来幹細胞を遺伝子改変してこのRNA–Lamp2a複合体を産生させ、小胞(エクソソーム)に封入して放出させるようにした。改変エクソソームを三重陰性細胞に与えると、RNA部分がENO1に結合し、Lamp2a部分が複合体全体をリソソームへ導き、たとえ安定化する乳酸化マークがあってもENO1は分解された。
動物での標的分解アプローチの検証
このアイデアを実用的な治療に近づけるため、研究者らは改変幹細胞を生分解性の足場上で増殖させ、この構築体を三重陰性腫瘍近傍の皮下に移植した。そこから幹細胞は継続的にENO1標的複合体を搭載したエクソソームを放出した。これらのマウスの腫瘍はENO1タンパク質量が著しく低下し、解糖の低下、分裂細胞の減少、細胞死の増加を示した。腫瘍はよりゆっくり成長し、悪性挙動が明らかに抑えられたことから、ENO1をリソソームに誘導することで腫瘍のお気に入りの燃料経路を効果的に枯渇させ得ることが示された。
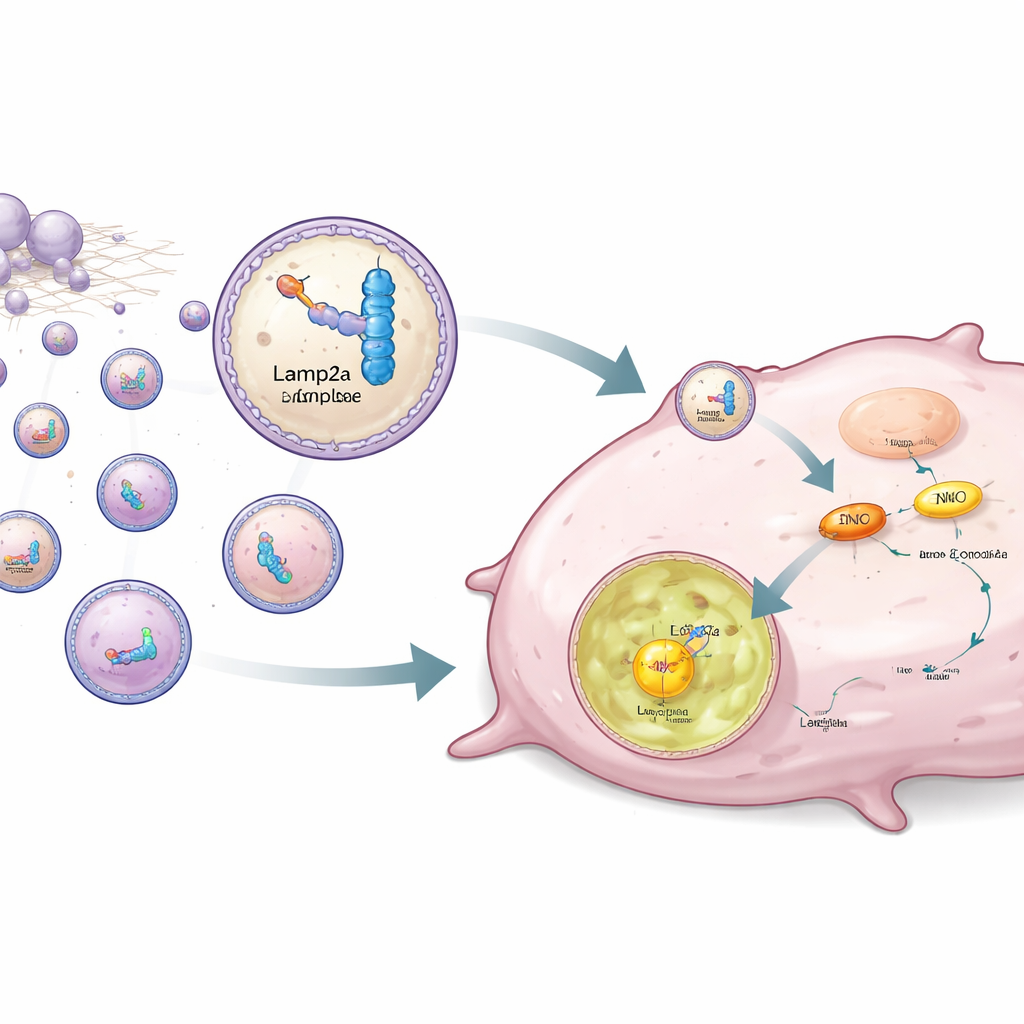
将来の治療にとって意味すること
専門外の読者に向けた要点は、この研究が三重陰性乳がんの弱点と新たな治療方針の両方を明らかにしたことだ。弱点は特に低酸素領域でENO1と乳酸を中心に作られる自己強化的なエネルギーループへの依存性である。治療の方針は、カスタムRNAと幹細胞由来エクソソームを用いてENO1を細胞の廃棄機構に引きずり込む標的タンパク質分解システムだ。臨床利用にはまだ遠いが、このアプローチは、がんの代謝的トリックを深く理解することで、悪性細胞を単に毒殺するのではなく無力化する精密な治療を生み出し得ることを示している。
引用: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
キーワード: 三重陰性乳がん, がん代謝, 乳酸シグナル伝達, 標的タンパク質分解, ENO1酵素