Clear Sky Science · ja
TP53変異卵巣がんにおける細胞周期阻害への適応的耐性を駆動するROR1‑PI3K/AKTシグナル伝達
なぜこの研究が女性の健康に重要なのか
卵巣がんは化学療法に対して腫瘍がしばしば耐性を獲得するため、女性にとって最も致命的ながんの一つです。本研究は重要な問いを立てます:強力な薬剤でがん細胞を致命的な分裂エラーに追い込むよう設計したとき、細胞はどのように生き延びる経路を見つけ出し、その脱出経路自体を弱点として利用できるか?研究者らは数週間〜数か月にわたる治療中の卵巣がん細胞を追跡することで、細胞が増殖を続けるか修復に回るかを決定する中心的な制御システムを明らかにし、標準治療に既に耐性を獲得した腫瘍を攻撃する新たな方略を示しています。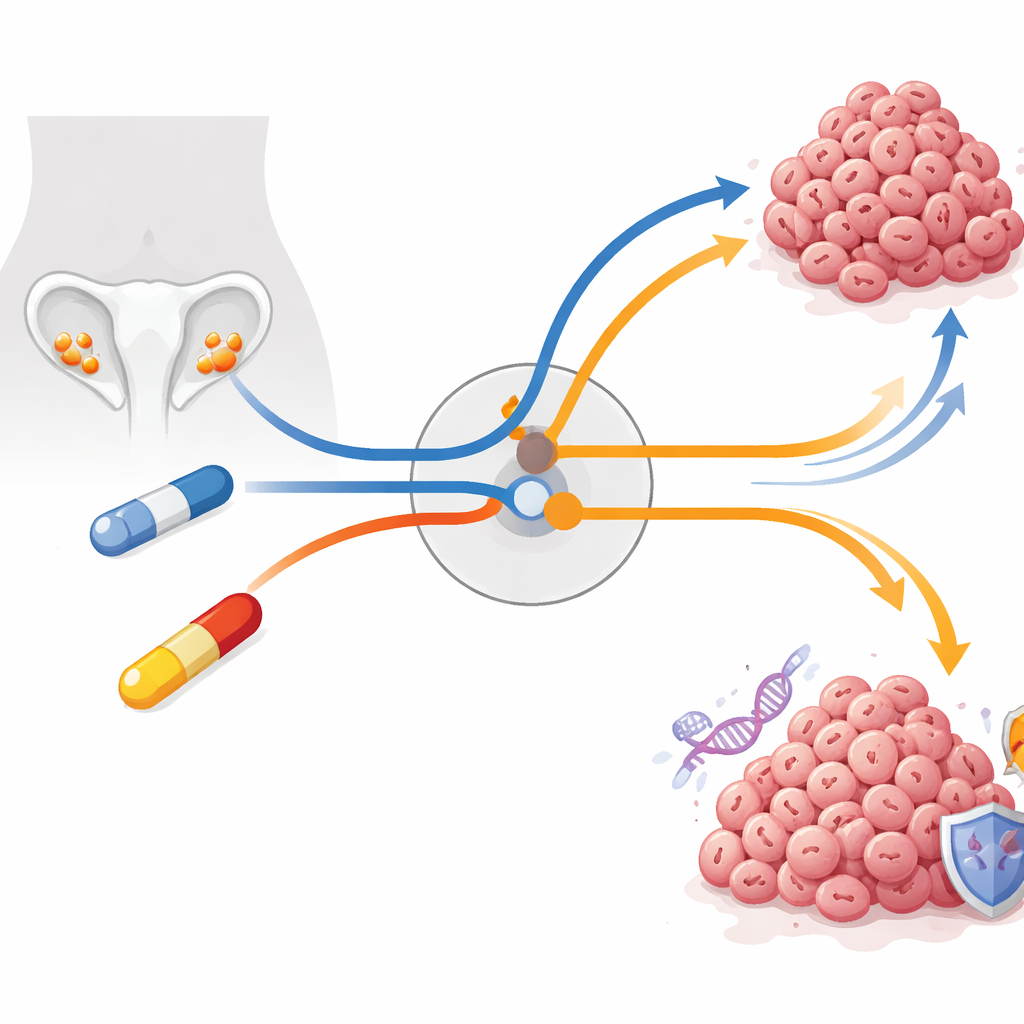
2つの一般的な薬剤、共通の脱出経路
研究チームは、高悪性度漿液性卵巣がんに着目しました。これは最も攻撃的で一般的なタイプであり、ほぼ常にゲノムの守護者であるTP53遺伝子に変異を抱えています。TP53が壊れているため、これらの腫瘍は細胞分裂サイクル後期のチェックポイントに異常に依存しています。この弱点を突く薬剤が二つあります:損傷細胞を早期に分裂へ押し込む実験的なWEE1阻害剤アダボセーティブ(adavosertib)と、染色体分離に必要な細胞内足場を固定する基幹化学療法パクリタキセル(paclitaxel)です。理論上、どちらもがん細胞を“有糸分裂カタストロフィー”——致命的な分裂失敗——へと導くはずですが、臨床や実験室ではしばしば腫瘍が適応します。研究者らは、患者で起こる現象を短期の高用量実験よりも忠実に模倣するため、数か月かけて薬剤用量を段階的に上げることで長期耐性モデルを作成しました。
がん細胞が生き残るためにどのように自らを再構築するか
高度なイメージングと「セルペインティング」——複数の細胞構造を同時に染める手法——を用いると、耐性細胞は単に元の姿のままではないことがわかりました。多核化、再編成された内部足場、より密に凝集したクラスターや小さく散在する3D球状体の形成など、多くの細胞に上皮–間葉転換を思わせる部分的な形態変化が見られました。これらの物理的変化は、細胞が移動、分裂、相互作用の仕方を配線し直したことを示唆します。同時に、詳細な単一細胞RNAシーケンシングにより、各薬剤と各細胞株が固有の遺伝子や染色体の変化パターンを発展させていることが明らかになりました。こうした遺伝的多様性にもかかわらず、一貫したテーマが浮かび上がりました:PI3KとAKTを中心とする増殖・生存経路の活性化が耐性モデル全体で上昇し、しばしばMAPKやNF-κBといった関連シグナル経路も伴っていたのです。
「高速バイパス」と「低速修復」を切り替える細胞内スイッチ
さらに掘り下げると、このPI3K/AKTシステムはがん細胞を二つの生存戦略の間で切り替えるスイッチとして働くことがわかりました。「高速バイパス」モードでは、PI3K/AKT活性が高くFOXO3という抑制タンパク質を無効化し、細胞周期チェックポイントを弱めるため、細胞は分裂を維持してアダボセーティブやパクリタキセルの致死効果を回避します。対照的に「低速修復」モードでは、PI3K/AKT活性は低く、核内でFOXO3が活性を保ち、複製速度を落としてDNA修復プログラムを起動し、薬剤をより効率的に排出します。驚くべきことに、短期の薬剤曝露はすべてのモデルでPI3K/AKT活性の急激な一時的上昇を引き起こし、長期的な耐性はがんの遺伝的背景や既存のシグナル状態に応じて高速バイパスまたは低速修復の状態に落ち着きました。これは同じ中心ハブが非常に異なる脱出経路を支えうることを示しています。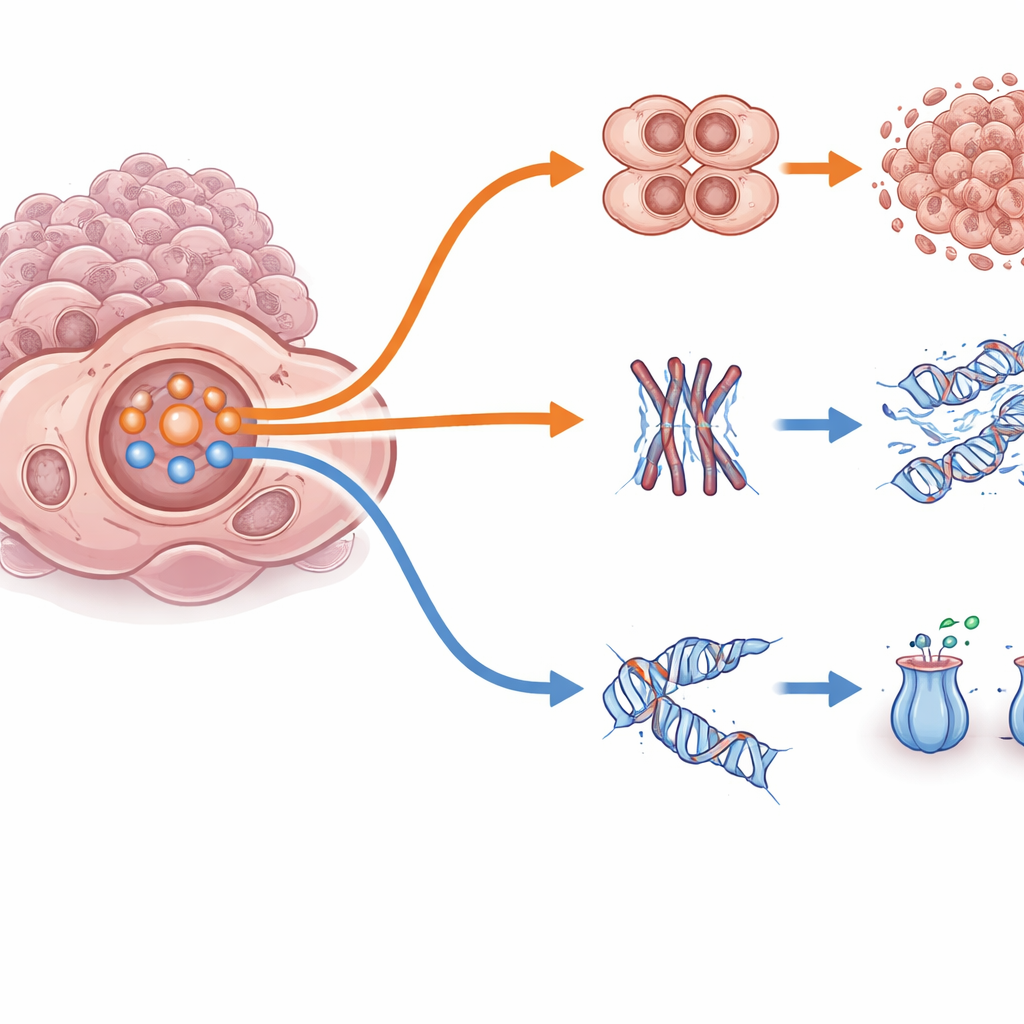
耐性シグナルを治療標的に変える
このハブの重要な上流プレーヤーの一つがROR1です。ROR1は正常な成人組織ではほとんど見られない受容体タンパク質ですが、いくつかのがんで上昇します。多くの耐性卵巣がんモデルで、ROR1レベルはPI3K/AKT活性とともに上昇しました。研究チームはROR1の発現を上下させることで、アダボセーティブやパクリタキセルに対する耐性獲得のしやすさが文脈依存で変化することを示しました。最も重要な点として、彼らはROR1を標的に有害ペイロードを運ぶ抗体薬物複合体ジロベルタマブ‑ベドチン(zilovertamab‑vedotin)を試験しました。細胞株と患者由来の3Dオルガノイドの両方で、ROR1高発現のアダボセーティブ耐性腫瘍はこの薬剤に特に脆弱であり、アダボセーティブとの併用はしばしば細胞死を増強しました。パクリタキセル耐性モデルの一部は反応が鈍く、これは薬剤排出能力が強化されていることが理由と考えられます。
今後の卵巣がん治療にとっての意義
本研究は、TP53変異卵巣がんにおける薬剤耐性を偶発的な出来事ではなく、中心的なシグナルスイッチによって統括される協調的な応答として再定義します。PI3K/AKT–FOXO3軸とROR1を重要ノードとして特定したことで、実践的な戦略が示唆されます:アダボセーティブやパクリタキセルのような有糸分裂標的薬を、耐性ハブを阻害する治療や耐性細胞上のROR1を利用する療法と組み合わせることです。ROR1は健康な組織にはほとんど存在しないため、こうした併用療法は再発・薬剤耐性を持つ腫瘍を選択的に攻撃し正常細胞を温存する可能性があります。これらの結果は実験室モデルおよび患者由来培養系に基づくもので、完了した臨床試験に基づくものではありませんが、高悪性度漿液性卵巣がんと向き合う女性に対してより賢明で持続性のある治療法を設計するための明確な道筋を示しています。
引用: Raivola, J., Rantanen, F., Dini, A. et al. ROR1-PI3K/AKT signaling drives adaptive resistance to cell cycle blockade in TP53 mutated ovarian cancer. Cell Death Dis 17, 276 (2026). https://doi.org/10.1038/s41419-026-08501-x
キーワード: 卵巣がん, 薬剤耐性, PI3K AKT経路, ROR1抗体療法, 細胞周期阻害薬