Clear Sky Science · ja
mTOR駆動のオートファジー抑制はCDK4/6阻害薬耐性HR+/HER2−乳がんにおける代謝的脆弱性を定義する
なぜこれが乳がん患者に重要なのか
進行乳がんの多くの女性は、腫瘍細胞の分裂を遅らせるCDK4/6阻害薬のおかげで長く生存できるようになりました。しかし残念ながら、多くの腫瘍は最終的にこれらの薬を回避する手段を獲得します。本研究は一つの希望に満ちた問いを投げかけます:乳がんがCDK4/6阻害薬に耐性を示すようになったとき、メトホルミンやジクロロ酢酸(DCA)のような既存で比較的単純な代謝薬で突くことができる新たな弱点を獲得しているのだろうか?
細胞周期薬が効かなくなったとき
臨床では、最も一般的な乳がんタイプであるホルモン受容体陽性・HER2陰性の病変には、ホルモン療法とともにパルボシクリブやリボシクリブといったCDK4/6阻害薬がよく用いられます。これらは細胞分裂を進めるタンパク質を標的にします。しかし時間とともに一部のがん細胞は適応し強い耐性を示すようになり、高用量の薬剤下でも増殖を続けます。研究者たちはこの問題を実験室で再現するため、乳がん細胞株(T47DおよびMCF7)に対して徐々に増量するCDK4/6阻害薬を投与しました。その結果、部分耐性を示す細胞と、治療にほとんど反応しなくなった少数の高耐性クローンという二種類の生存集団が得られました。
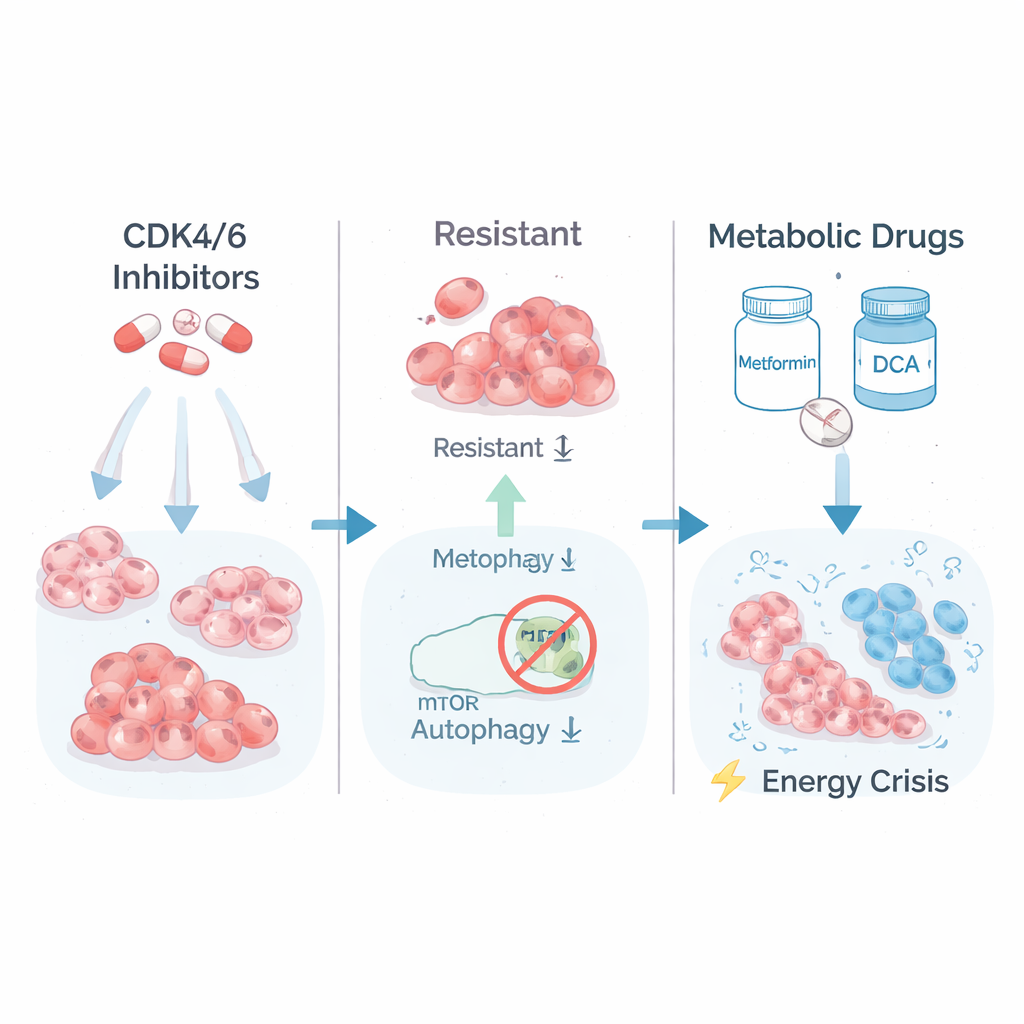
腫瘍のエネルギー利用に潜む弱点
高耐性細胞が何を変えたのかを理解するために、研究チームはオン・オフされている遺伝子を解析しました。最も耐性の高い細胞は、糖を燃やす経路(解糖)と、mTORC1と呼ばれるタンパク質複合体に制御される増殖シグナル経路を活性化していることがわかりました。言い換えれば、これらの細胞は高速モードで燃料を大量に消費して増殖していました。研究者らはこの“ハイギア”代謝を逆手に取れるかを試しました。彼らは代謝ストレスを与える一般的な糖尿病薬メトホルミンと、細胞により効率的な燃料処理を強いるDCAで耐性系と親株を処理しました。驚くべきことに、最も薬剤耐性の高いクローンが最も脆弱であることが示されました:長期の培養増殖は代謝治療で崩壊し、親株や部分耐性細胞はそれほど影響を受けませんでした。
自己清掃の遮断とエネルギー崩壊
なぜこれらの逃避したがん細胞がエネルギーのストレスに対してこれほど敏感なのか。その答えはもうひとつの基本的な生存プロセス、オートファジー(細胞の「リサイクルと掃除」システム)にありました。通常、エネルギーが不足すると細胞は自身の構成要素を分解して再利用し生き延びます。研究者たちは高耐性クローンではmTORC1が過剰活性化され、オートファジーの起動に重要なULK1に化学的なブレーキをかけていることを示しました。高感度のリポーターアッセイを用いて、これらの細胞は代謝薬で刺激しても適切にオートファジーをオンにしたり増強したりできなくなっていることを実証しました。その結果、メトホルミンとDCAは深刻なエネルギー危機を引き起こしました:低エネルギーのセンサーが活性化し、脂質合成は停止し、不可逆的な細胞死のマーカーが強い耐性細胞で特に出現しました。
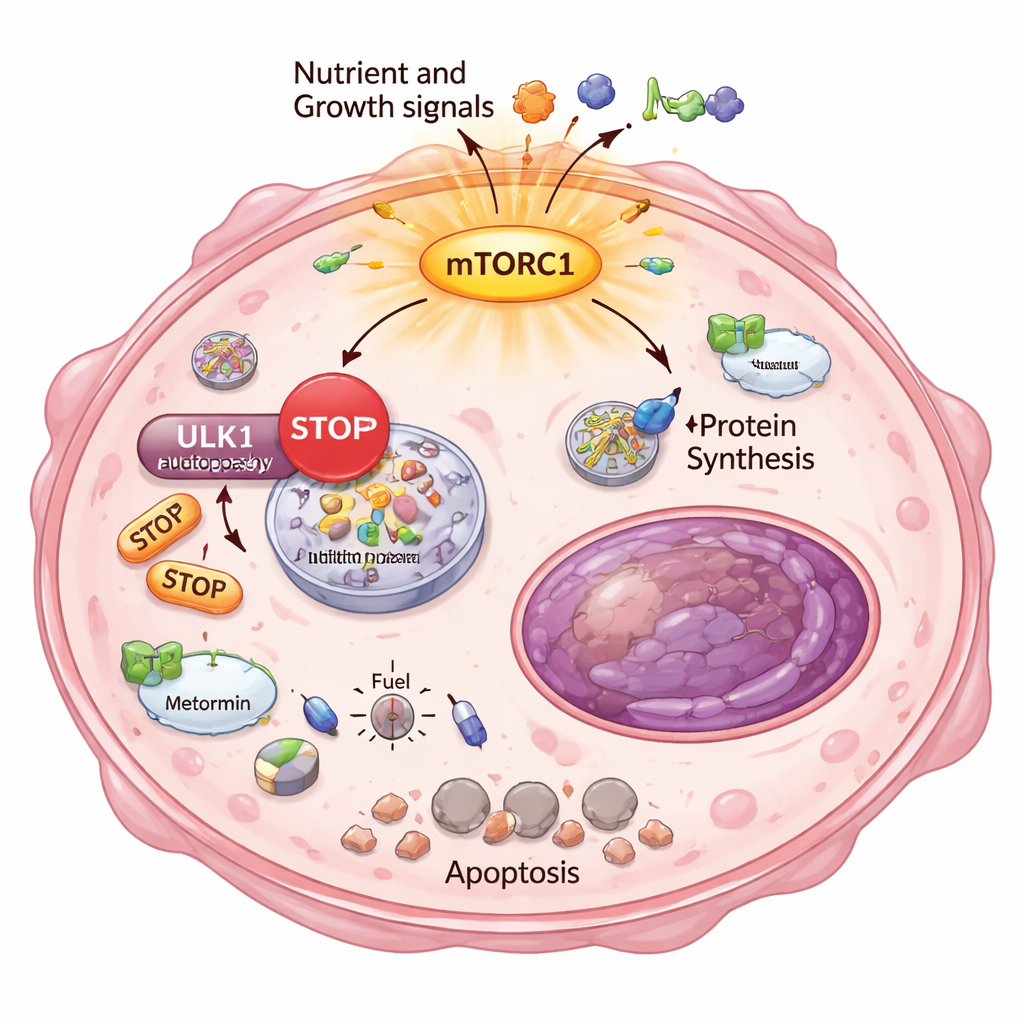
患者腫瘍からの証拠
実験モデルが必ずしも患者で起こることを反映するわけではないため、研究チームはヒトの乳がん検体に目を向けました。彼らは100を超えるがんに対してmTORC1活性の指標(リン酸化4E-BP1)と、オートファジーが阻害されると蓄積するタンパク質p62を免疫染色しました。mTORC1活性が高い腫瘍はp62が多い傾向があり、「過剰に駆動された成長シグナル+リサイクル不良」というパターンが細胞株だけでなく実際の乳がんにも存在することを裏付けました。これは、臨床の一部の患者が実験で見られたのと同じ代謝的弱点を持つ腫瘍を有する可能性を示唆します。
今後の治療にとって意味すること
一般向けの要点はこうです:乳がんが強力なCDK4/6薬から逃れるように進化するとき、同時に代謝的に行き詰まる可能性があるということです。増殖シグナルを恒常的にオンにし、細胞のリサイクルをオフにすることで、これらの腫瘍は一定のエネルギー供給に強く依存するようになります。本研究は、この状況がメトホルミンやDCAのような既知の代謝薬で悪用できることを示しています。重要なのは、mTORC1活性とオートファジーマーカーを調べる簡便な組織検査が、耐性腫瘍がこの種の代謝的攻撃に適しているかを同定するのに役立ちうると著者らが提案している点で、CDK4/6阻害薬が効かなくなった後のより個別化された救済治療への道を開く可能性があります。
引用: von Wichert, L., Stroh, A., Witt, M. et al. mTOR-driven autophagy suppression defines metabolic vulnerability in CDK4/6 inhibitor-resistant HR+/HER2− breast cancer. Cell Death Dis 17, 235 (2026). https://doi.org/10.1038/s41419-026-08496-5
キーワード: 乳がん, CDK4/6阻害薬耐性, mTOR, オートファジー, 代謝療法