Clear Sky Science · ja
発がん性BCS1Lアイソフォームのスプライス切替がミトコンドリア機能を破壊して卵巣がんの進行を抑制する
がん細胞内の発電所
私たちの体のすべての細胞はミトコンドリアと呼ばれる小さな発電所に依存しています。急速に増殖・転移するがん細胞は特にエネルギーを必要とします。本研究は、卵巣がんがどのように主要なミトコンドリア補助因子の一つを書き換えるかを解き明かし、この補助因子の分子的な“スイッチ”を穏やかに切り替えることで腫瘍を飢餓状態にし、正常組織には比較的影響を与えない可能性を示しています。
腫瘍がエンジンに頼る理由
卵巣がん細胞は多くのがんと同様に、柔軟に異なるエネルギー源を利用できます。研究者らは大規模な患者データベースと単一細胞プロファイルを精査することで、多くの卵巣腫瘍が酸化的リン酸化(OXPHOS)として知られる高駆動モードでミトコンドリアを稼働させていることを見いだしました。このような強化されたミトコンドリア活性を示す腫瘍はより攻撃的で、進行した病期で多く見られました。ミトコンドリアのエネルギー機構を構築する多くのタンパク質の中で、ひときわ注目されたのがBCS1Lです。BCS1Lは複合体IIIの組立を助けるシャペロンで、細胞のエネルギー回路の中心的ハブです。高OXPHOS腫瘍や特定の腫瘍細胞サブタイプではBCS1Lの活性が特に強く、がん細胞がこの補助因子に頼ってエンジンを稼働させていることを示唆していました。
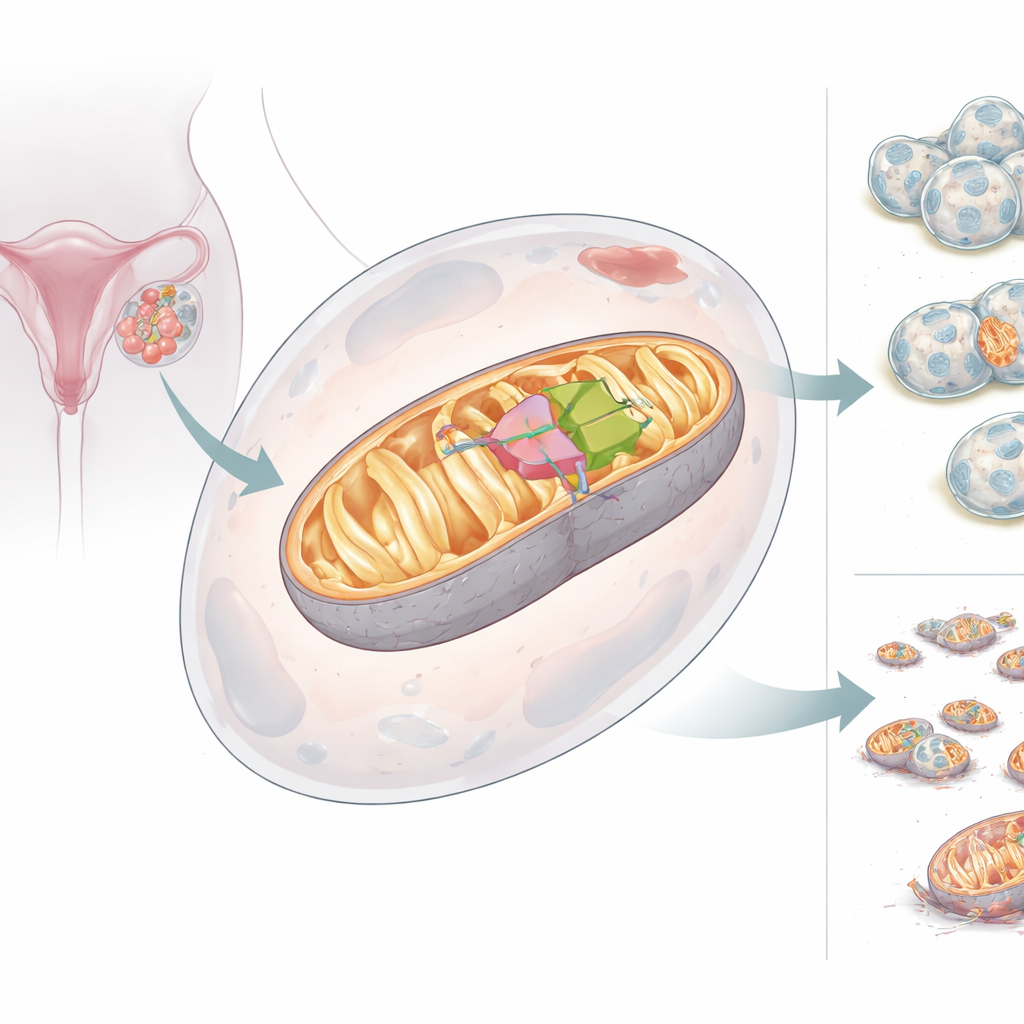
ミトコンドリア補助因子の二つの顔
研究チームはBCS1L遺伝子が二つのバージョン(アイソフォーム)を産生し得ることを発見しました。全長型のBCS1L-Lはミトコンドリアへ向かうアドレスタグを持ち、複合体IIIの適切な組立と強いエネルギー産生を支えます。短縮型のBCS1L-Sは重要な領域を欠いておりミトコンドリアに到達できず、細胞質や核に留まりエネルギー産生を支えません。健常組織では短い型が一般的ですが、卵巣がんではそのバランスが逆転し、ミトコンドリア結合型の長い型が優勢になります。細胞にBCS1L-Lを多く作らせると、ミトコンドリアのエネルギー産生は増加し、膜電位は維持され、ダメージを与える酸素由来副産物は減少し、細胞死に対する抵抗性が高まりました。逆にBCS1Lを減らすとミトコンドリアは断片化し、エネルギー産生が低下し、有害な酸素分子が増加し、がん細胞は死にやすくなりました。
がんはメッセージをどう書き換えるか
長い型か短い型かを産生するかは、スプライシングと呼ばれるRNAメッセージの編集の仕方に依存します。研究者らはBCS1L RNAに結合してこの選択に影響を与えるタンパク質を探索しました。その結果、USP39というスプライシング因子に着目しました。USP39は既にいくつかのがんと関連付けられている因子です。卵巣がん細胞ではUSP39はBCS1Lのエクソン2となるRNA領域の近傍に結合し、その包含を促進してミトコンドリアに向かう長い型を優勢にします。USP39をサイレンシングすると細胞はこの領域をより頻繁にスキップし、短いBCS1L-S型へのシフトが生じました。このシフトは複合体IIIを弱め、ミトコンドリア呼吸とATP産生を減少させ、酸化ストレスを増大させ、がん細胞死を誘導しました。これらの細胞にBCS1L-Lを再導入するとミトコンドリア機能と生存が大部分回復し、USP39が主にBCS1Lを介して重要なミトコンドリアのスイッチを駆動していることを示しました。
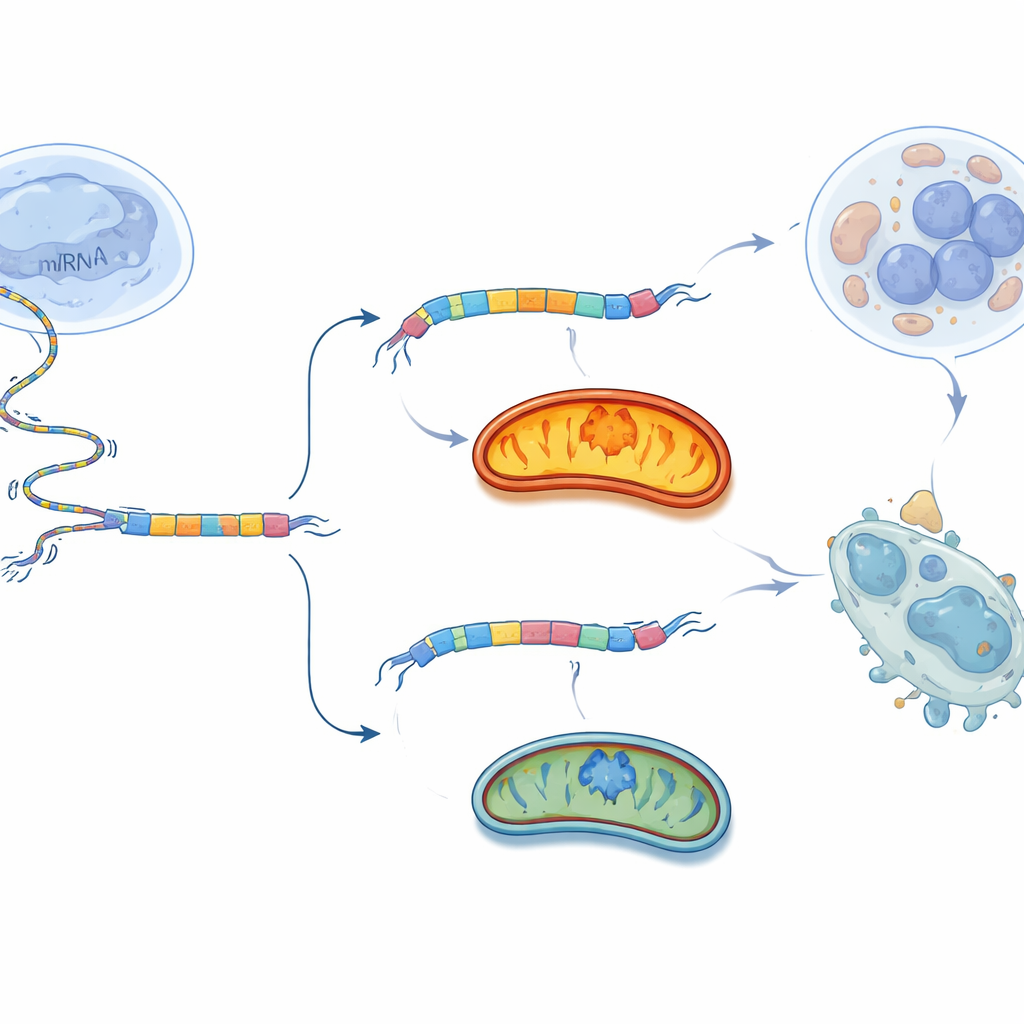
腫瘍に対してスイッチを切る
ミトコンドリアを広く阻害すると多くの組織が損なわれる可能性があるため、チームはより外科的な手法を試みました。BCS1L自身のスプライス選択をわずかに操作するのです。彼らはBCS1L RNAのエクソン2の周辺に結合する短い遺伝材料断片、いわゆるアンチセンスオリゴヌクレオチド(ASO)を設計しました。これらのASOは小さな洗濯ばさみのようにスプライシング機構の読み方を変え、細胞にエクソン2をスキップさせることを促します。培養皿内の卵巣がん細胞で、最も有効なASOは長いBCS1L-Lを強く減らし短いBCS1L-Sを増強しました。その結果、ミトコンドリア呼吸とATP産生は低下し、有害な酸素レベルは上昇し、多くの細胞がプログラム細胞死を起こしました。同じASOをマウスの卵巣がん腫瘍に注入すると、腫瘍増殖は遅くなり腫瘍重量は減少し、正常な線維芽細胞に対する影響よりもがん細胞への効果がはるかに強く現れました。
患者にとって何を意味するか
簡潔に言えば、本研究は多くの卵巣がんが成長のためにミトコンドリア補助タンパク質の“ターボ”版に依存していることを示しています。スプライシング因子USP39は細胞のRNA編集機構を傾け、このターボ版の産生を増やして腫瘍の発電所を最適化します。精密に設計したASOを用いてスプライシング選択を弱い型へ戻すことで、研究者らはがん細胞のミトコンドリアを選択的に機能不全にし、がん細胞死を引き起こしつつ大部分の正常細胞には比較的影響を与えないことが可能になります。こうしたASO薬を腫瘍へ届けることは依然大きな課題ですが、本研究はBCS1Lのスプライシングスイッチが卵巣がん治療のための有望で非常に特異的な新たな標的であることを示しています。
引用: Xu, M., Wang, Z., Yang, S. et al. Splice-switching of the oncogenic BCS1L isoform suppresses ovarian cancer progression by disrupting mitochondrial function. Cell Death Dis 17, 293 (2026). https://doi.org/10.1038/s41419-026-08495-6
キーワード: 卵巣がん, ミトコンドリア, RNAスプライシング, BCS1L, アンチセンスオリゴヌクレオチド