Clear Sky Science · ja
NSD2は酸化的リン酸化を介してPD-L1の発現を抑制し、肝細胞がんにおける免疫監視を制御する
なぜこの肝臓がんの話が重要なのか
肝細胞がんは肝臓がんの中で最も一般的な型で、診断が遅れることが多く多くの治療に耐性を示します。腫瘍細胞のPD-L1による「透明マント」を遮断する免疫療法薬は一部の患者に効果がありますが、多くには効きません。本研究は、肝がん細胞のエネルギー産生と免疫からの可視性をつなぐ予想外の因子、NSD2というタンパク質を明らかにしました。この結びつきを理解することで、既存療法の効果を高める手がかりや、どの患者が利益を得られるかを見極める手段が得られる可能性があります。
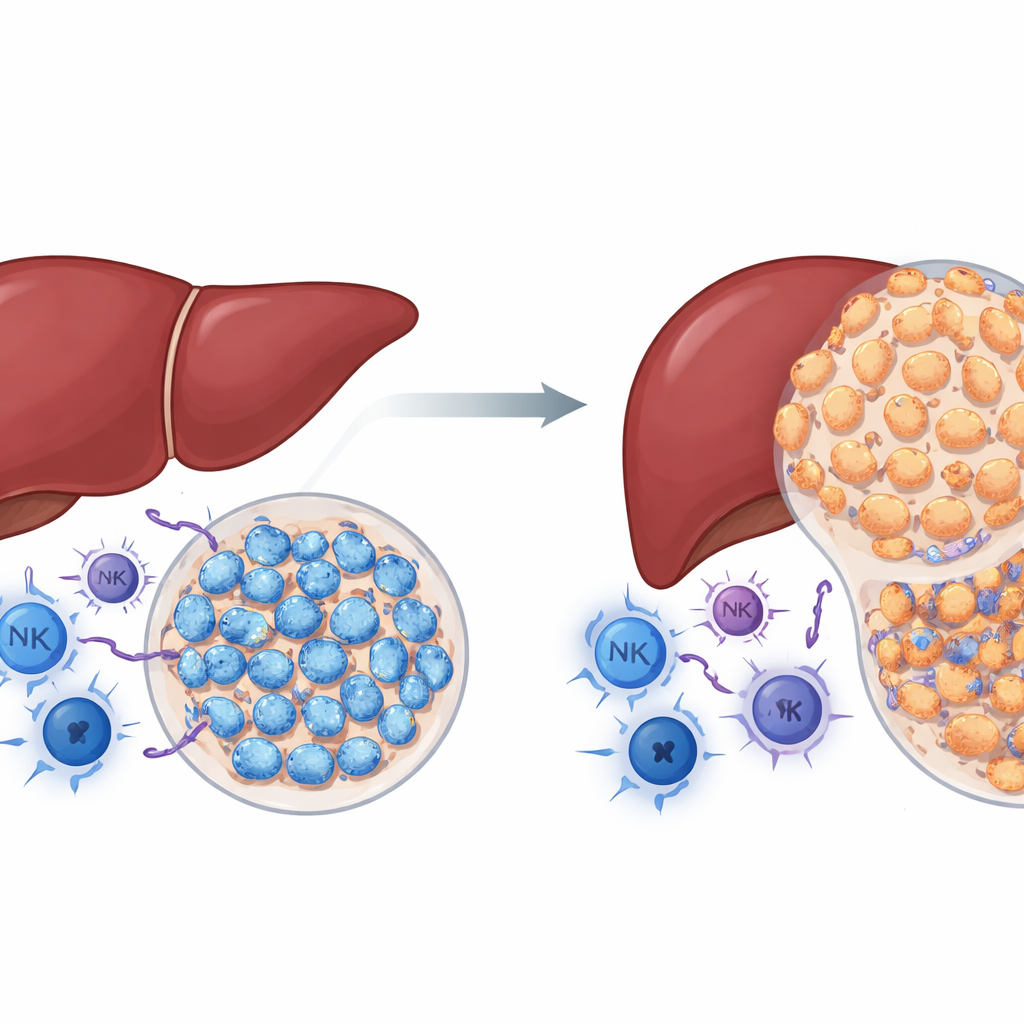
知られたが意外な役割を持つがんタンパク質
NSD2はヒストンを修飾する酵素で、DNAが巻き付くタンパク質を変化させます。多くのがんでNSD2は腫瘍増殖を促す因子と見なされてきました。著者らは肝がんでも同様かどうかを問いました。肝細胞で特異的にNSD2を活性化する遺伝子改変マウスを用い、肝腫瘍を確実に誘導する化学物質で処置すると、期待に反してNSD2を過剰発現するマウスは正常マウスよりもはるかに少数で小さな腫瘍を発生させ、肝障害、線維化、細胞増殖も少なかったのです。同時に、NSD2過剰発現肝由来の腫瘍には、ヘルパーT細胞やキラーT細胞、ナチュラルキラー細胞など抗がん作用を持つ免疫細胞がより多く浸潤していました。これらの発見は、免疫系が機能する環境ではNSD2が腫瘍を加速するというよりは抑制する働きを持つことを示唆します。
腫瘍細胞のエネルギー工場と燃料利用
NSD2がどのように腫瘍を抑えるかを調べるため、研究チームは肝組織の遺伝子発現プロファイルを解析しました。するとNSD2過剰発現は、ミトコンドリア—細胞の「発電所」—が酸素を使ってエネルギーを作る過程である酸化的リン酸化に関わる遺伝子群を強く抑えることが分かりました。マウスおよびヒトの肝がん細胞株での追試実験では、NSD2を高めると多くの酸化的リン酸化遺伝子の発現が低下し、酸素消費量とATP産生が減り、ミトコンドリア膜電位が低下してミトコンドリア活動が弱まる指標を示しました。同時に、これらの細胞はグルコース消費も減らしましたが、解糖系へ依存を切り替えるわけではなく、総じてエネルギー産生の低下を示しました。NSD2の欠失は逆にミトコンドリアの能力と燃料利用を強化しました。
NSD2がエネルギーと免疫可視性をどう書き換えるか
さらに踏み込み、研究者らはゲノム全体のクロマチンマッピングと遺伝子発現データを組み合わせて、NSD2が存在すると直接活性化される遺伝子群を同定しました。そのうちCamk2dとPrkceはミトコンドリア活性を抑えることが知られています。NSD2はこれらのプロモーター領域で特定のヒストン修飾(H3K36me2)を増加させ、それによって発現を高めました。NSD2欠失の肝がん細胞にこれらの遺伝子を再導入するとミトコンドリアの酸素利用とATP産生が低下し、これらがNSD2の下流で酸化的リン酸化を抑えるブレーキとして働くことが確認されました。重要なのは、以前の研究で活発なミトコンドリアが腫瘍細胞で高いPD-L1を支持することが示唆されていた点です。一致して、本研究でもNSD2過剰発現はPD-L1レベルを低下させ、NSD2欠失は肝がん細胞および腫瘍組織でPD-L1を上昇させました。
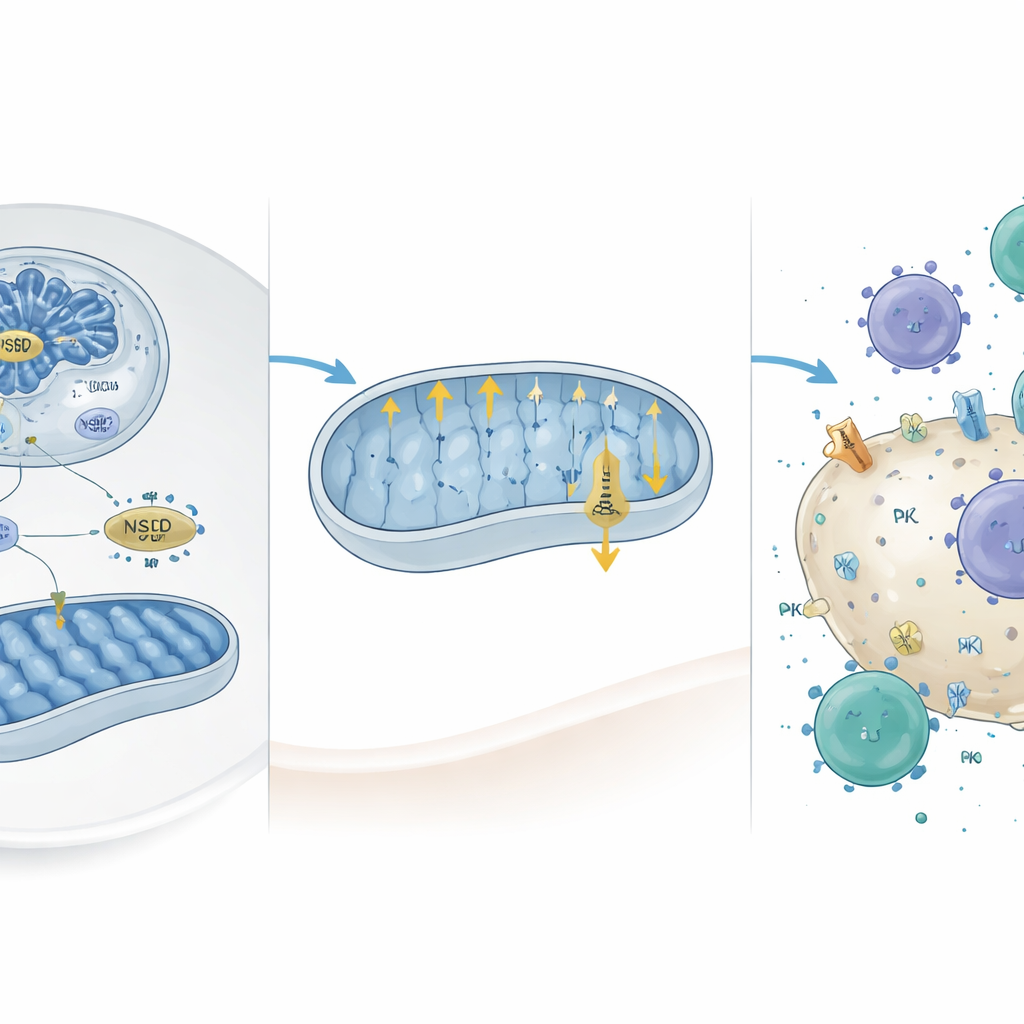
“盾”を弱めて免疫攻撃を呼び覚ます
これらの分子変化の機能的影響は、NSD2を獲得または喪失するように操作したがん細胞を肝臓に注入したマウスで試験されました。NSD2を欠く細胞は急速に大きな腫瘍を形成し、より多くのPD-L1を発現し、特に活性化したキラーT細胞を含むT細胞やナチュラルキラー細胞の浸潤が少なくなりました。研究者が酸化的リン酸化の主要成分であるミトコンドリア複合体Vを化学的に阻害すると、NSD2欠失細胞のPD-L1レベルは正常に近づき、免疫細胞は腫瘍細胞死をより引き起こしやすくなりました。同様に、NSD2欠失細胞にCamk2dやPrkceを過剰発現させるか、PD-L1を遮断する抗体で腫瘍を処置すると、腫瘍サイズが縮小し免疫細胞の浸潤が回復しました。患者データセットでは、NSD2発現が低いと生存率が悪い一方で、興味深いことにPD-L1標的療法への反応が良好である傾向があり、NSD2の状態がどの患者がこうした薬で恩恵を受けるかを予測する手がかりになり得ることを示唆しています。
将来の肝がん治療にとっての意味
一般読者への主要メッセージは、本研究が少なくとも機能する免疫系が存在する状況では、NSD2を肝がんにおける腫瘍抑制因子として再定義したことです。細胞の酸素を使ったエネルギー産生を抑えることで、NSD2は間接的に腫瘍細胞のPD-L1を低下させ、彼らの「透明マント」の一部を取り去り免疫細胞が認識して攻撃できるようにします。この新たに記述されたNSD2–エネルギー–PD-L1の連鎖は実用的な示唆を与えます。第一に、腫瘍にNSD2が欠如する患者はPD-L1遮断薬の適応が特に有望かもしれないこと、第二にミトコンドリアのエネルギー産生を阻害する薬と免疫療法を組み合わせることが、肝がんに対する強力な二段攻撃になり得るということです。
引用: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
キーワード: 肝細胞がん, NSD2, 酸化的リン酸化, PD-L1, 腫瘍免疫療法