Clear Sky Science · ja
ミトコンドリアホスファターゼPGAM5を標的にすることで、NRF2依存のFSP1発現を上方制御しフェロトーシスと急性膵炎を軽減する
なぜストレスを受けた細胞と痛む膵臓が重要なのか
細胞が過度の負荷を受けると、全身にダメージを与える死に方をすることがあります。その一つがフェロトーシスと呼ばれる細胞死で、鉄と進行する化学反応により細胞膜の脂質が酸化(いわば“さびる”)して起こります。この過程は、痛みを伴い時に致命的になりうる急性膵炎を含む臓器損傷と関連しています。本稿の基となった研究は、ミトコンドリア――細胞の発電所――内にあるフェロトーシスを調節する重要なスイッチを明らかにし、そのスイッチを遮断することでマウスモデルの膵臓を保護できることを示しています。
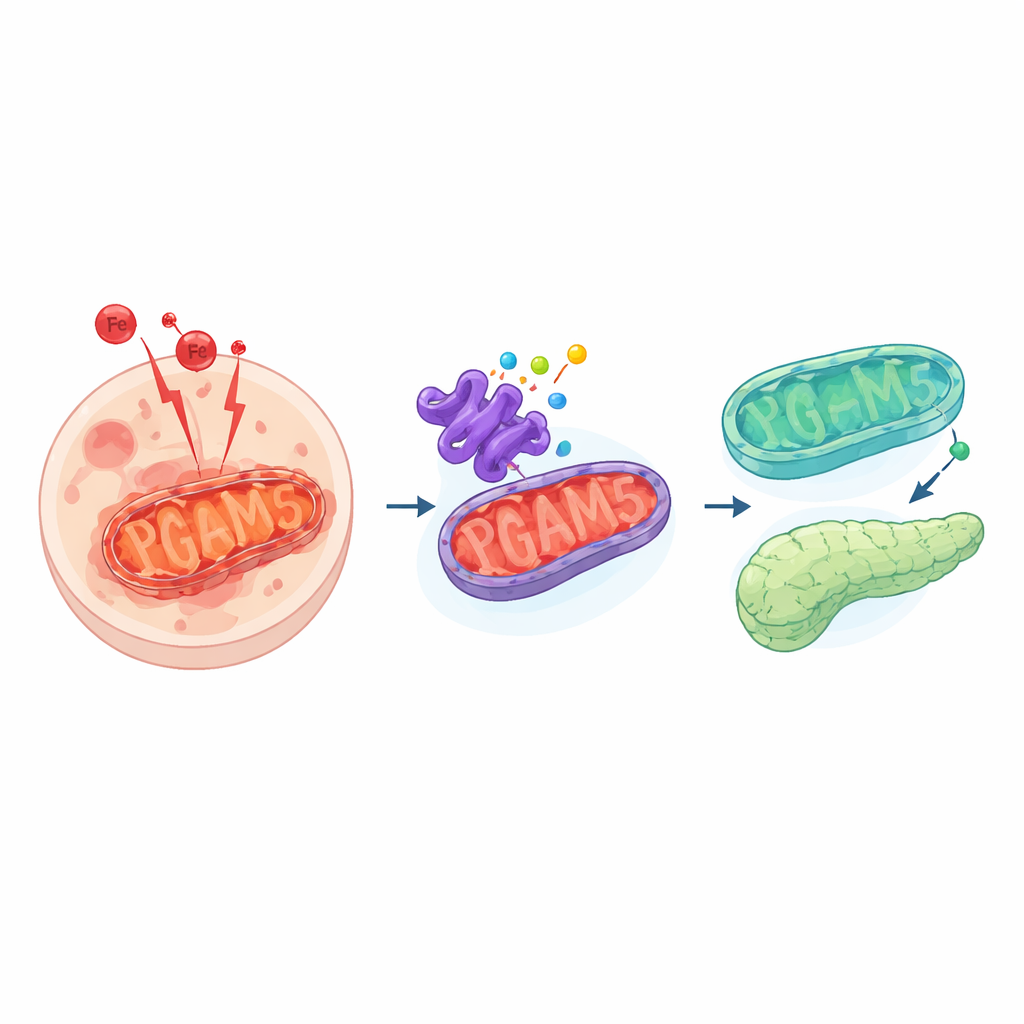
危険な細胞死の一形態
フェロトーシスはアポトーシスのようなよりよく知られた細胞死と異なります。整然とした自己破壊ではなく、フェロトーシスでは鉄を介した反応の嵐が細胞膜の繊細な脂質を酸化させます。これにより有毒な副生成物が生まれ、膜に穴が開いて最終的に細胞が死に至ります。通常、細胞はこれらの反応性分子を解毒する保護システムで均衡を保っていますが、これらのシステムが機能不全に陥るか圧倒されると、フェロトーシスは組織全体に損傷を広げ、がんから臓器不全までさまざまな疾患に寄与します。
標的にされるミトコンドリアのスイッチ
研究者たちはPGAM5と呼ばれるタンパク質に着目しました。PGAM5はミトコンドリアの内側面に局在し、シグナル伝達のハブとして働きます。PGAM5はミトコンドリアの形態を制御し、ストレスに応答し、酸化の処理に影響を与えます。驚くべきことに、チームがPGAM5を減らすか過剰発現させると、細胞はフェロトーシスによる死にくさを示しました。PGAM5の化学的阻害、遺伝学的ノックダウン、および過剰発現はいずれも有害な脂質副産物の蓄積を軽減し、フェロトーシス誘導薬による細胞死を抑えました。これにより、この系は精密に調節されており、PGAM5が少なすぎても多すぎても細胞がより保護された状態へ傾くことが明らかになりました。
内部シールドの作動
さらに詳しく調べると、PGAM5の影響はNRF2とFSP1という二つの別の因子を含む保護軸を通じていることがわかりました。NRF2は核内で活性化されると幅広い抗酸化防御を作動させるマスターレギュレーターです。FSP1はその下流の防御因子の一つで、脂溶性抗酸化物質を再生して細胞膜での脂質損傷を阻止します。PGAM5の量が変わると、細胞はNRF2のmRNAおよびタンパク質レベルを上げ、NRF2が細胞質から核へ移行しやすくなりました。そこでNRF2はFSP1の産生を増強します。FSP1またはNRF2を阻害すると保護効果は消え、フェロトーシスに対する感受性が回復しました。これはPGAM5–NRF2–FSP1の連鎖が観察された耐性に必須であることを示しています。
エネルギーのストレスが隠れたメッセンジャー
研究はまた、ミトコンドリアのストレスがどのようにしてこの保護応答に変換されるかを明らかにしました。PGAM5を乱すとミトコンドリアの均衡が崩れ、細胞のエネルギー通貨の比率が変化しました:低エネルギー分子(AMPとADP)に対する高エネルギーATPの比が低下し、エネルギー不足のシグナルが上昇します。これがエネルギー感知酵素AMPKを活性化しました。活性化されたAMPKはNRF2を直接変化させ、NRF2の核への移行を促進し、さらにFSP1の産生を高めます。AMPKを除くとNRF2はもはや核に蓄積せず、FSP1レベルは低下し、細胞は再びフェロトーシスに陥りました。したがって、PGAM5はミトコンドリアの状態をエネルギーおよび抗酸化応答につなげ、鉄による細胞死から保護する役割を果たします。
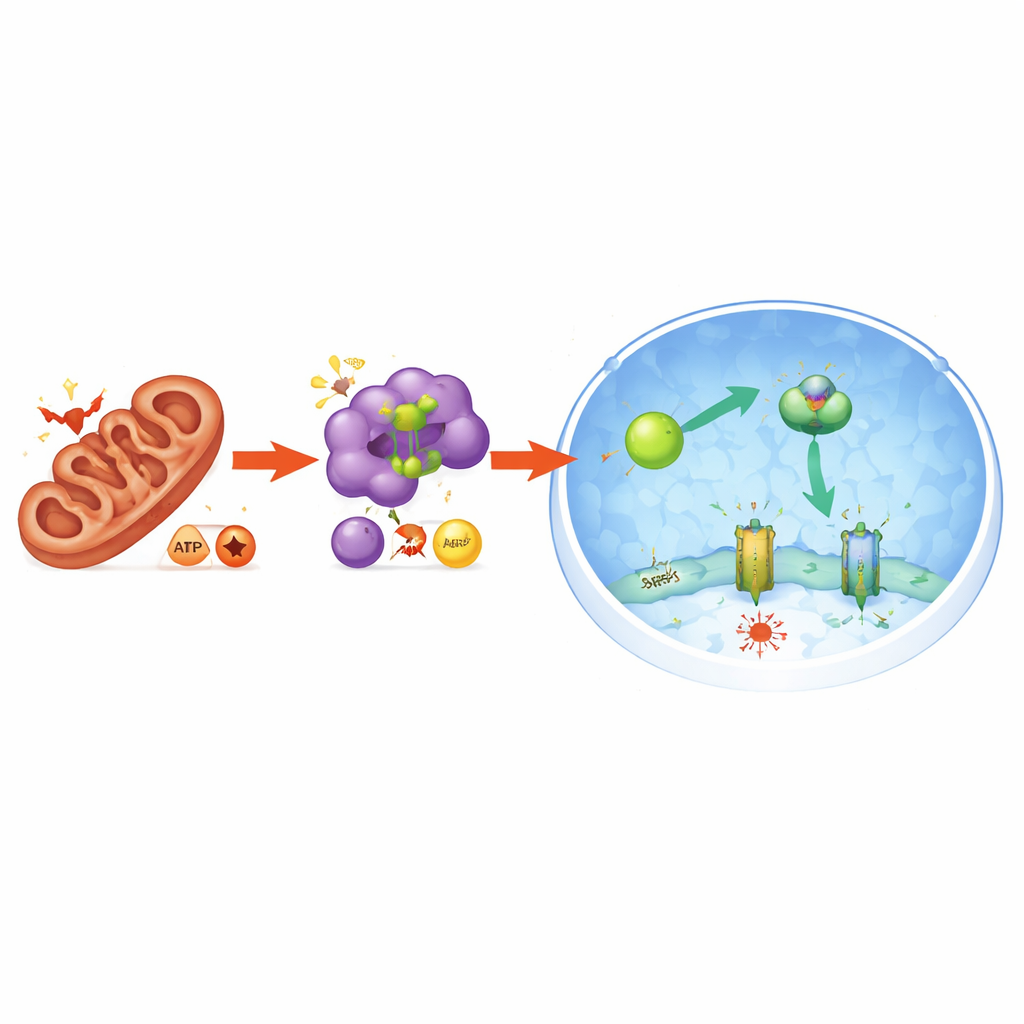
生体動物で膵臓を保護する
このメカニズムが臓器全体で重要かを確かめるため、研究者たちはアルギニン高投与で誘発される急性膵炎のマウスモデルを用いました。このモデルでは膵臓に広範な損傷が生じ、組織傷害を示す血中酵素が上昇し、炎症性分子が急増します。脂質過酸化のマーカー――フェロトーシスの指標――も膵臓で急激に上昇しました。PGAM5阻害化合物でマウスを治療すると、これらの症状は和らぎました:血中の損傷マーカーは低下し、顕微鏡で見た膵組織はより健康的に見え、炎症性シグナルは減少しました。同時にフェロトーシスマーカーは低下し、膵臓ではAMPK活性、NRF2、FSP1のレベルが上昇し、細胞培養で見られた保護経路と一致しました。
将来の治療への意味
総じて、この研究はPGAM5をミトコンドリアのストレス、細胞のエネルギー状態、およびフェロトーシスを阻止する強力な抗酸化プログラムを結びつける中心的制御点として特定しました。PGAM5の活性を低下させることで、細胞はAMPKとNRF2を作動させ、FSP1を増強し、鉄による脂質損傷に対して耐性を高めます。マウスではこの戦略が急性膵炎の膵臓損傷を軽減しました。一般向けに言えば、研究者たちは破壊的な細胞死の形を防ぐ新しい内部の“サーキットブレーカー”を見つけたということです。臨床利用にはまだ多くの課題がありますが、PGAM5やその下流パートナーを標的にすることで、フェロトーシスやミトコンドリア機能不全が有害な役割を果たす病態に対する新たな治療の道が開ける可能性があります。
引用: Ma, S., Qin, J., Luan, J. et al. Targeting mitochondrial phosphatase PGAM5 alleviates ferroptosis and acute pancreatitis by upregulating NRF2-mediated FSP1 expression. Cell Death Dis 17, 252 (2026). https://doi.org/10.1038/s41419-026-08484-9
キーワード: フェロトーシス, ミトコンドリア, 急性膵炎, 酸化ストレス, 細胞死