Clear Sky Science · ja
RIPK1はマウスの自己反応性β細胞モデルにおいて遺伝子発現とキナーゼシグナルを介してβ細胞の運命を制御する
インスリン産生細胞を守ることが重要な理由
1型糖尿病は、体の免疫系が膵臓のインスリン産生を担うβ細胞を破壊してしまうことで発症します。これらの細胞が失われると、生涯にわたるインスリン注射に頼らざるを得ません。本研究は、免疫攻撃を受けた際にβ細胞が生き残るか死ぬかの決定に関わる内部の“スイッチ”であるRIPK1に着目しています。このスイッチを理解し制御できれば、残存するβ細胞を保護し、1型糖尿病の経過を遅らせたり緩和したりする新たな方策が開ける可能性があります。
β細胞内のストレススイッチ
1型糖尿病が進行する際、β細胞は厳しい環境に置かれます。免疫細胞はTNFαやIFNγといった炎症性シグナルを放出し、β細胞をストレスや死へと追い込みます。RIPK1は多くの細胞で中心的な意思決定因子として働き、これらのシグナルを統合して細胞を生存へ導くか、異なるタイプのプログラム化された死へ導くかを制御します。本研究では、免疫攻撃を受けるβ細胞においてRIPK1が同様の役割を果たすか、そしてRIPK1の活性を下げることが細胞の生存に寄与するかを検証しました。
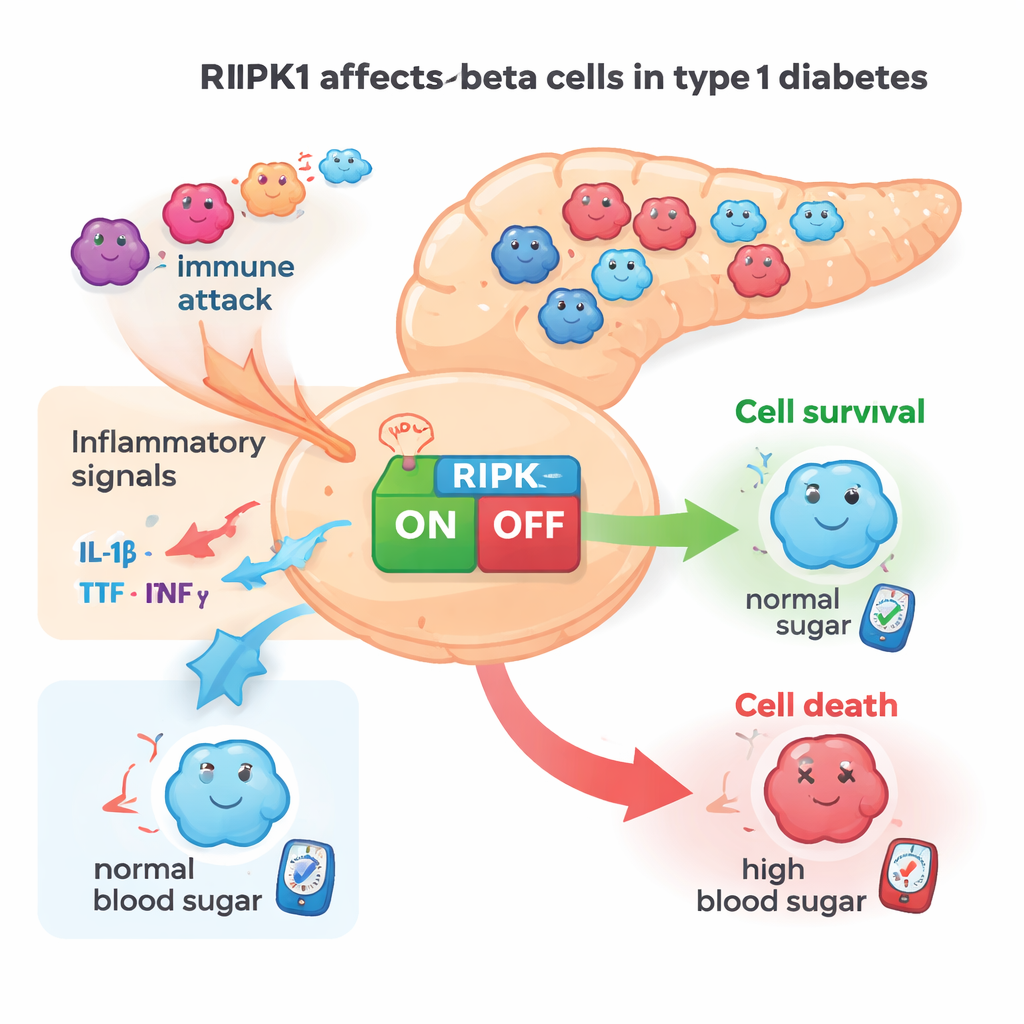
糖尿病感受性の細胞でRIPK1レベルが上昇する
まずチームは、RIPK1が1型糖尿病に関与している兆候を探しました。炎症性シグナルはマウスのβ細胞株や培養したヒトβ細胞でRIPK1の活性を高めることが示されました。マウスとヒトの膵組織では、RIPK1がインスリン産生細胞に明確に存在していました。重要なのは、糖尿病感受性のNODマウスのアイソレットでは、年齢とともに自己免疫が進むにつれてRipk1遺伝子活性が上昇していたことです。ヒトドナーの単一細胞遺伝子データでも同様の傾向が見られ、1型糖尿病の人由来のβ細胞は非糖尿病ドナー由来よりもRIPK1 RNAが多く検出されました。これらの観察は、RIPK1が自己免疫による圧力を受けているときにより活性化されるストレス関連タンパク質であることを示唆しています。
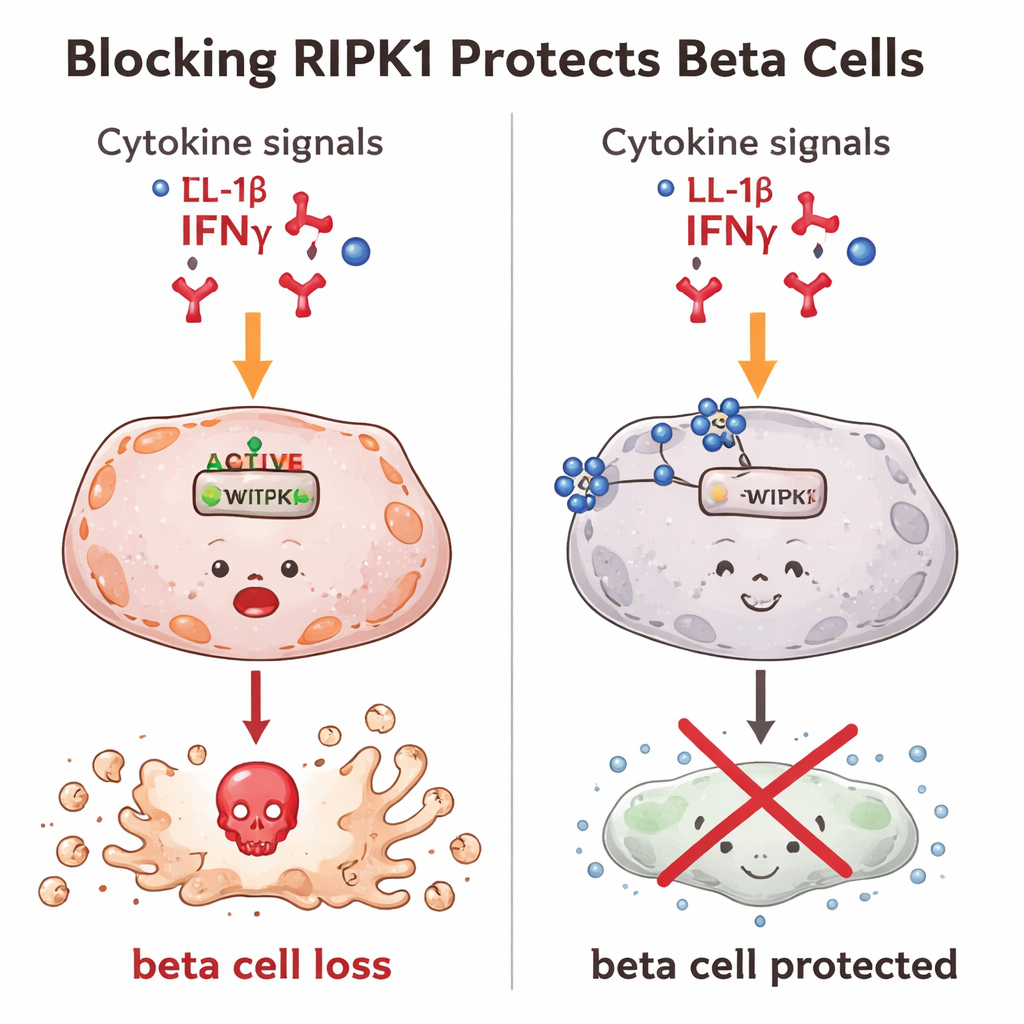
RIPK1を阻害するとβ細胞の生存が改善する
次に、RIPK1を遮断した場合に何が起きるかを検証しました。炎症性シグナルにさらされたマウスβ細胞では、通常RIPK1が活性化され細胞死が増加します。研究者らが小分子の阻害剤を用いてRIPK1の活性を抑えるか、細胞内量を減らすと、はるかに少ないβ細胞が死にました。さらに遺伝子編集ツールでRipk1遺伝子そのものを弱め、RIPK1量が著しく低いβ細胞を作製しました。これらの編集細胞は、従来型の“プログラム化”された細胞死と、より爆発的で炎症性の高い細胞死の双方に対して著しく耐性を示しました。つまり、RIPK1の働きを低下させることで、強い有害シグナル下でもより多くのβ細胞が生存したのです。
細胞プログラムとシグナル伝達の大規模な変化
β細胞の保護は単一の死経路を止めるだけではありませんでした。大規模なRNAシーケンス解析により、RIPK1を除去するとβ細胞内の多くの遺伝子プログラムが再編成されることが分かりました。炎症や自然免疫応答に関連する遺伝子は抑えられ、一方でβ細胞の恒常性やインスリン産生に関わるいくつかの遺伝子は増加しました。同時に、活性化された酵素の広範な解析では、MAPKやJAKなどのストレスや免疫信号を伝える複数のシグナル経路がRIPK1欠損によって配線変更されることが示されました。これらの変化は、RIPK1がβ細胞の死の有無だけでなく、自己免疫攻撃時の“炎症化”の程度、認識されやすさ、機能性にも影響を及ぼすことを示唆しています。
生体内での免疫攻撃への抵抗
これらの知見がより現実的な状況で意味を持つかを調べるため、研究者らはNODマウス由来の糖尿病を引き起こす免疫細胞を正常またはRIPK1欠損のβ細胞と混ぜ合わせました。どちらのタイプのβ細胞も免疫細胞を活性化することはできましたが、RIPK1欠損細胞は通常細胞に比べて殺される割合が約半分でした。マウスモデルでは、同じ動物に正常なβ細胞とRIPK1欠損β細胞の両方を移植し、その後自己免疫攻撃を誘導しました。時間の経過とともに、通常のβ細胞移植片はほとんど消失しましたが、RIPK1欠損移植片は生体発光イメージングで数十倍から百倍以上明るく保たれ、多くの細胞が免疫攻撃を生き延びたことを示しました。
1型糖尿病の患者にとっての意味
本研究は、RIPK1が自己免疫攻撃時にインスリンを作る細胞が生きるか死ぬかを決める中心的なストレススイッチとして作用することを示しています。RIPK1を低下させると、β細胞は死ににくくなり、炎症性シグナルを発しにくくなり、恒常性や機能を保ちやすくなります。RIPK1を安全に標的とする薬は他の疾患で既に検討されているため、同様の戦略をβ細胞保護に応用することで、特に病期の早期にまだ一部のβ細胞が残っている場合に、1型糖尿病の予防や進行抑制に新たな道を提供する可能性があります。
引用: Contreras, C.J., Mukherjee, N., Harris-Kawano, A. et al. RIPK1 regulates β-cell fate via actions on gene expression and kinase signaling in a mouse model of β-cell self-reactivity. Cell Death Dis 17, 220 (2026). https://doi.org/10.1038/s41419-026-08471-0
キーワード: 1型糖尿病, β細胞, RIPK1, 自己免疫, 細胞死