Clear Sky Science · ja
メラノーマ細胞の運命を書き換える:TRPM8変調薬がアポトーシスを誘導しNK細胞の細胞傷害性を高める
“冷感センサー”を皮膚がんに対して利用する意味
メラノーマは薬剤や免疫系を回避する能力を身につけやすい危険な皮膚がんです。本研究はメラノーマ細胞の意外な弱点、すなわち冷感やメンソールを感知することで知られるタンパク質TRPM8に注目します。研究者らは、TRPM8を阻害するように設計した薬剤が、メラノーマ細胞を自己破壊に追い込み、同時にナチュラルキラー(NK)細胞による攻撃を受けやすくすることを示しました。この二重の作用は、治療が難しい進行メラノーマに対する新たな治療戦略を示唆します。
メラノーマ細胞上の隠れたスイッチ
大規模ながんデータベースの解析と患者由来メラノーマ細胞の実験解析により、TRPM8は正常な皮膚(健康なメラノサイトや真皮線維芽細胞を含む)に比べて転移性メラノーマではるかに多く発現していることが明らかになりました。イメージングでは、TRPM8が細胞表面だけでなく内部の膜にも局在しており、細胞挙動に影響を与える戦略的な位置にあることが示されました。一連の新規TRPM8標的化分子を用いると、化合物4と9が一貫して際立ち、時間経過でメラノーマ細胞の生存を急速に低下させる一方、正常な皮膚細胞にはほとんど影響を与えませんでした。遺伝学的検証では、TRPM8を除去するとこれらの薬剤の殺傷効果が失われ、TRPM8を増加させるとメラノーマ細胞の感受性が高まることが確認され、この効果が特定のチャネル依存であることが証明されました。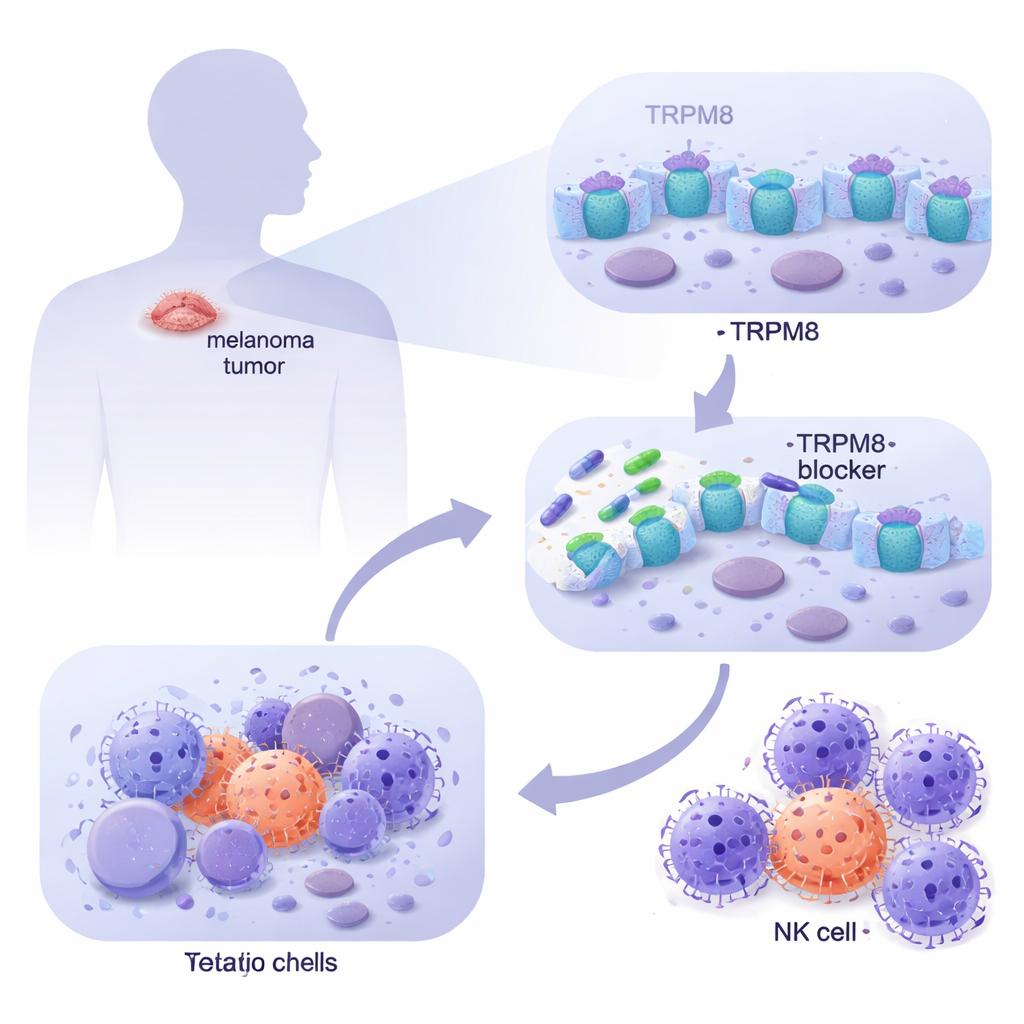
がん細胞をエネルギー危機に追い込む
メンソールのような古典的なTRPM8活性化剤とは異なり、これらの新しい阻害剤は細胞内へのカルシウム流入を引き起こしませんでした。代わりに、メラノーマ細胞内で酸化ストレスの波を引き起こしました。これらの化合物は特にミトコンドリア内で活性酸素種(ROS)を急速に増加させました。この酸化バーストによりミトコンドリアの電位が消失し、断片化し、シトクロムcが漏出するという、細胞の内在的“自殺”プログラムを起動する重要な段階が引き起こされました。これらの反応性分子を除去する抗酸化剤は細胞を大部分救済し、酸化還元バランスの崩壊が副次的な現象ではなく細胞死の駆動力であることを示しました。下流では、カスパーゼ-3の活性化やPARPの切断といった古典的な死のマーカーが認められ、細胞が無作為な損傷ではなくプログラムされたアポトーシスを経ていることが確認されました。
生存シグナルの無力化と守護者の覚醒
この酸化ストレスはより広範なストレス応答を引き起こしました。薬剤はDNA損傷のセンサーであるATMを活性化し、有名な腫瘍抑制タンパク質p53の蓄積と活性化を促しました。p53は損傷細胞が修復を試みるか死を選ぶかを決定します。同時に、これらの化合物はメラノーマの主要な生存経路の一つであるPI3K–AKT経路を弱体化させました。通常、TRPM8はPI3K構成要素と物理的に相互作用してAKTを成長促進型の活性状態に保つのに寄与しますが、処理後はこの結びつきが壊れAKT活性が低下し、細胞死への傾倒をさらに促しました。重要なのは、これらの変化が非がん性細胞では顕著でなかった点であり、腫瘍を強く攻撃しながら正常組織を温存する治療的ウィンドウの存在を示唆します。
腫瘍を免疫“ヒットスクワッド”に見つけやすくする
メラノーマの危険性は免疫監視から逃れる能力にもあります。研究者らは、低用量のTRPM8阻害剤を長期にわたり生き残った腫瘍細胞に何が起きるかを調べました。残存した細胞は表面マーカーULBP1の発現を増やし、これはNK細胞側のNKG2D受容体によって認識される救援の旗のように作用することが分かりました。他の関連するフラグは変化せず、選択的な効果であることが示されました。三次元メラノーマスフェロイド(実際の腫瘍をよりよく模倣するモデル)では、TRPM8阻害剤による前処理が構造を縮小させ細胞死を増加させるだけでなく、NK細胞攻撃に対して格段に脆弱にしました。ULBP1またはNKG2Dを抗体でブロックすると、この追加的な殺傷効果はほとんど消失し、免疫による除去の改善が腫瘍とNK細胞間の特定の握手(相互作用)を介していることが示されました。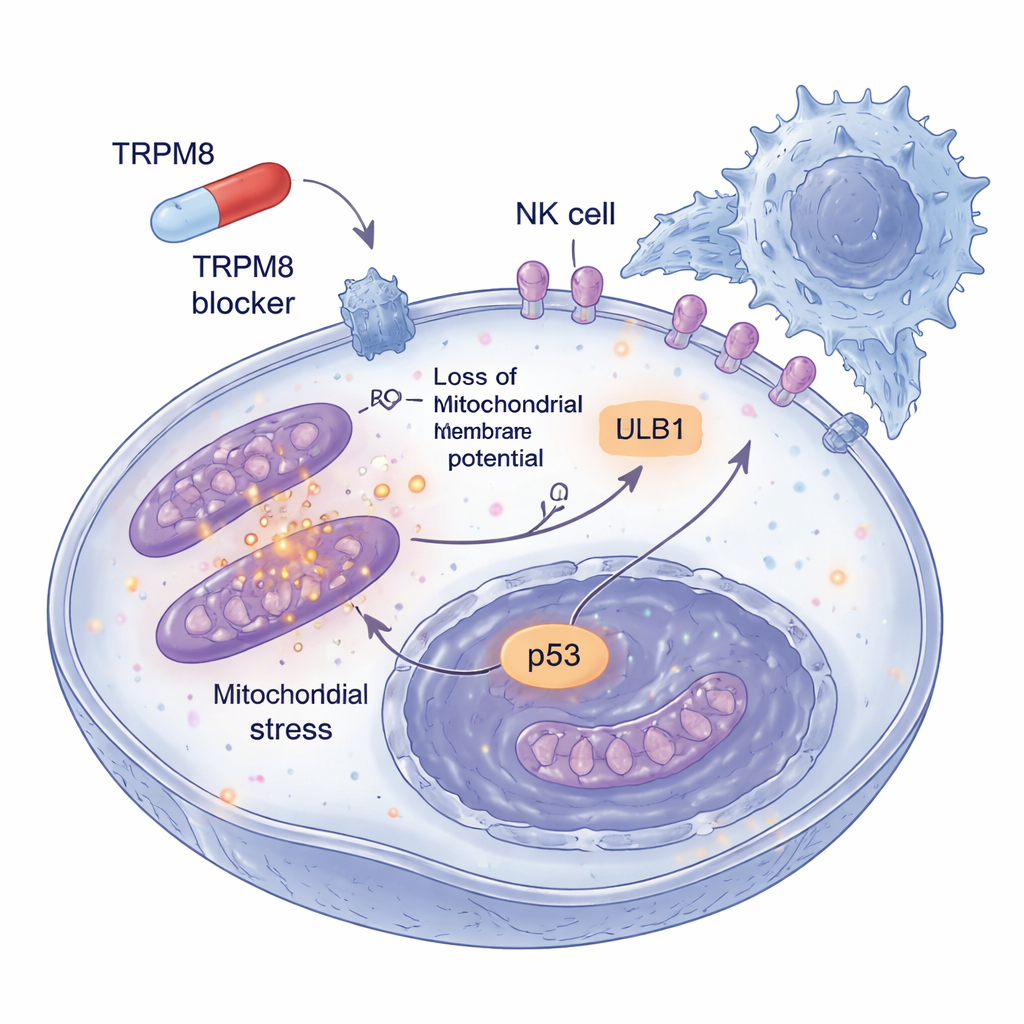
将来のメラノーマ治療に向けての意義
端的に言えば、TRPM8という“冷感センサー”を阻害することは治療的なレバーとして働きます:メラノーマ細胞を致命的なミトコンドリア・DNA危機に追い込み、同時にNK細胞による破壊のための旗を立てます。これらの薬剤は正常な皮膚細胞を温存しNK細胞自体を傷つけないため、新しい治療法の有望な基盤となります。著者らは、TRPM8阻害剤が既存の免疫療法と併用されることで、腫瘍細胞を直接殺すと同時に生き残った細胞を免疫系がより見つけやすくして除去する、二方面からの攻撃を可能にすると提案しています。
引用: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
キーワード: メラノーマ, TRPM8, ミトコンドリア, 酸化ストレス, ナチュラルキラー細胞