Clear Sky Science · ja
PDHA1のアセチル化シグナルがカプロプトーシスを抑制し、前立腺がんにおける抗アンドロゲン効果を弱める
この研究が重要な理由
前立腺がんは男性に多いがんの一つで、多くの進行例は男性ホルモンのシグナルを遮断する薬で治療される。主要薬剤であるエンザルタミドは当初有効でも、やがて腫瘍が耐性を獲得して効かなくなることが多い。本研究は、なぜ一部の前立腺がんがエンザルタミドの効果を回避するのかという意外な理由を明らかにし、単一の代謝経路を阻害することで腫瘍の再感受性化が可能になることを示し、より持続的な治療法への道を開く。
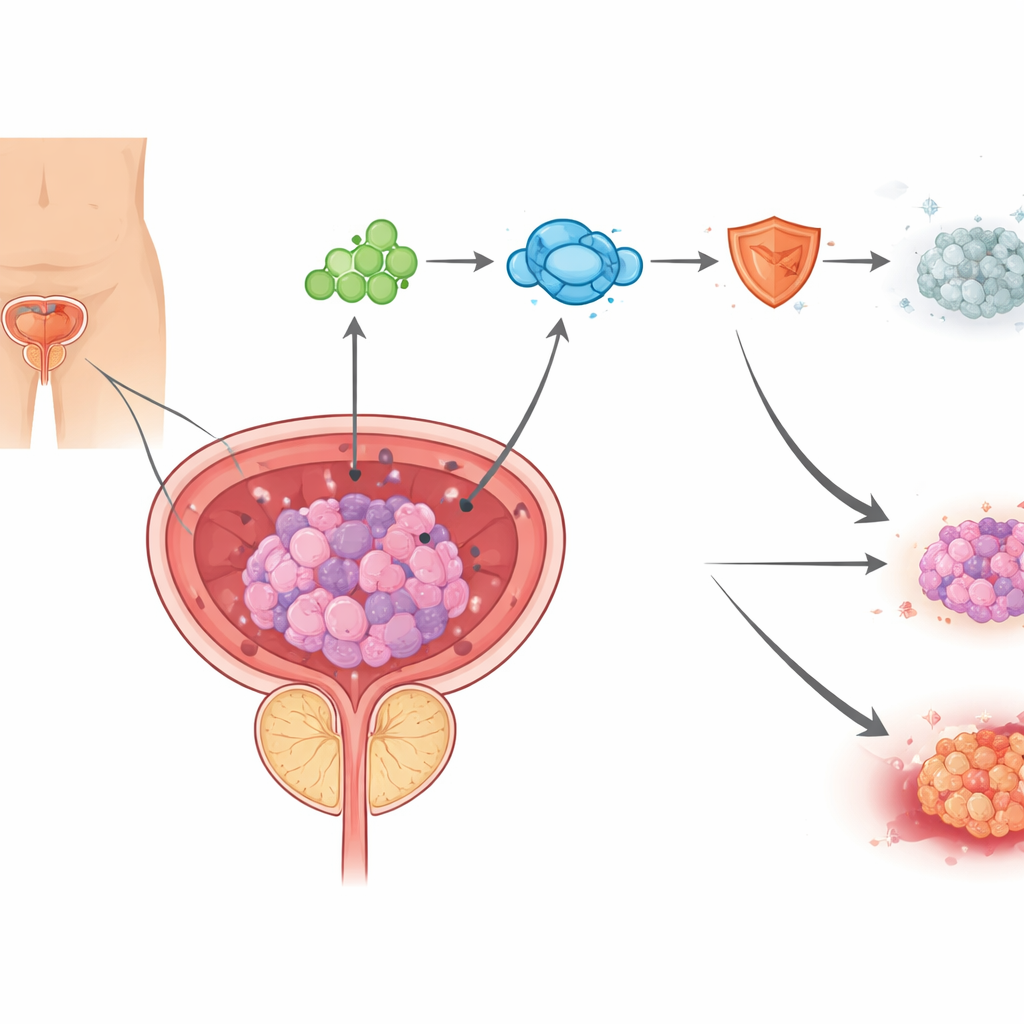
銅によって駆動される新しいタイプの細胞死
細胞はさまざまな経路で死にうるが、現代のがん研究ではこうした自然の死のプログラムを腫瘍細胞で再活性化しようとすることが増えている。著者たちはカプロプトーシスと呼ばれる新たに記述された細胞死の型に着目した。これは銅がミトコンドリア内に蓄積すると誘導されるものである。抗アンドロゲン薬で治療された患者の前立腺がん試料では、銅の蓄積とミトコンドリア損傷、さらにカプロプトーシスの印であるタンパク質変化の兆候が見られた。培養細胞ではエンザルタミドが銅レベルを上昇させミトコンドリアを損なわせ、銅結合化合物が細胞を大部分救済できたことから、エンザルタミドは一部その作用を銅駆動性の細胞死を促すことで示すことが分かった。
腫瘍はどのようにして銅の毒性を鈍らせるか
しかし、すべてのがん細胞が死ぬわけではない。著者らはエンザルタミド耐性前立腺腫瘍の複数のデータセットを解析し、カプロプトーシスに関連する遺伝子に注目していく中で、際立ったタンパク質を特定した。それがPDHA1であり、糖由来の燃料をアセチルCoAに変換する仕組みの中核を成す構成要素である。PDHA1は耐性腫瘍で高発現し、予後不良やより攻撃的な疾患と関連し、またエンザルタミド自体によって増加していた。実験室でPDHA1を抑えると、がん細胞はエンザルタミドや直接的なカプロプトーシス誘導薬に対してはるかに感受性が高まり、逆にPDHA1を増やすと細胞は死ににくくなった。マウスではPDHA1を減らした腫瘍がエンザルタミド治療でより大きく縮小し、この酵素が生体内で治療への抵抗を助けることを確認した。
治療に対する代謝的かつエピジェネティックなシールド
研究チームは次にPDHA1がどのようにしてこの防御を築くかを解明した。PDHA1はアセチルCoAの産生に関与するため、DNAのパッケージングや転写の読み取り方を変える可能性を検討した。PDHA1が高いとアセチルCoAのレベルとヒストンタンパク質の化学的な「アセチル」修飾が増加し、特に活性遺伝子に関連するマークが上昇した。主要な標的の一つはSLC7A11であり、これはシステインを細胞内へ取り込み、主要な抗酸化物質であるグルタチオンを生成するトランスポーターである。PDHA1が多いと細胞はより多くのグルタチオンを作り、PDHA1が少ないとシステインとグルタチオンが減少した。グルタチオンは銅と結合して中和し、カプロプトーシスを引き起こすストレスを低減する。グルタチオンやSLC7A11を回復させると、PDHA1阻害時に見られる増大した銅ストレスを元に戻せたことから、PDHA1–アセチルCoA–ヒストン–SLC7A11–グルタチオンという連鎖が、がん細胞が銅を掃き取り死を回避する仕組みであることが示された。
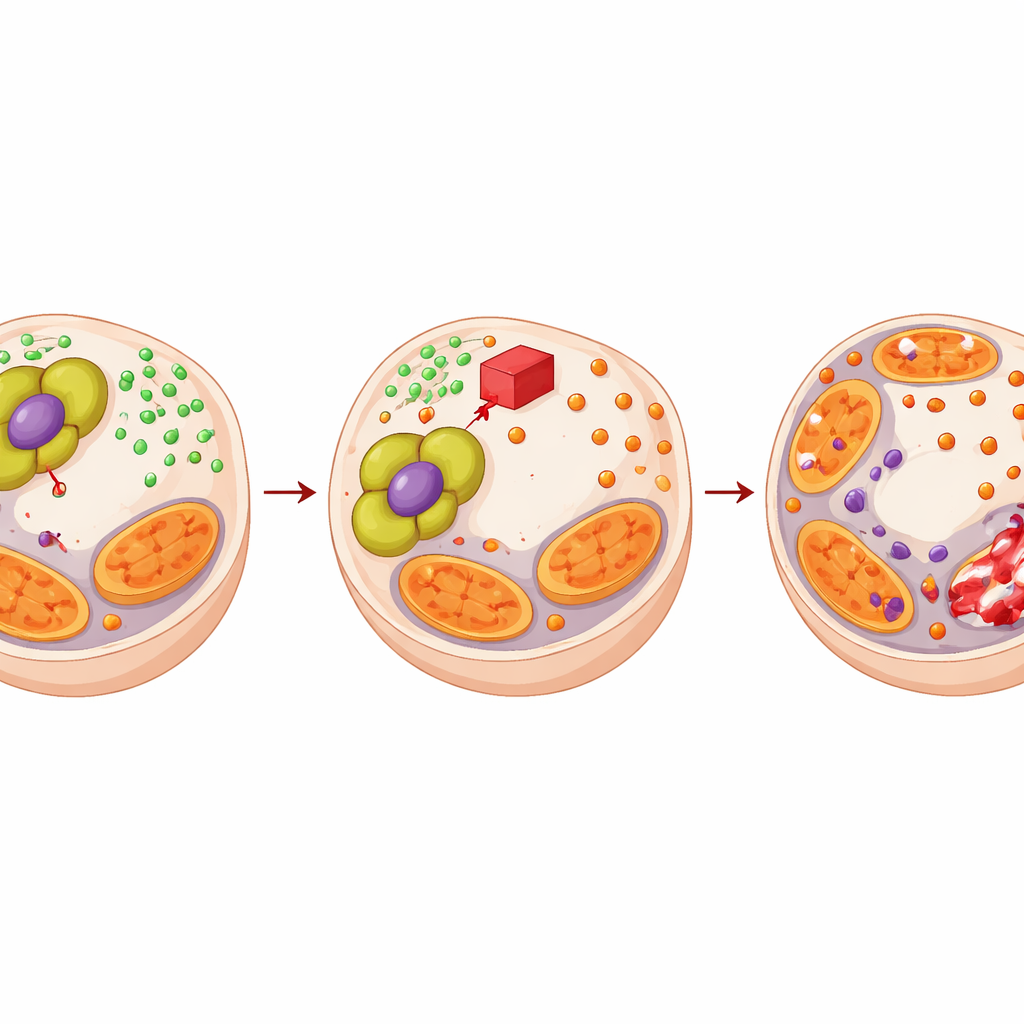
脆弱性を治療戦略に変える
PDHA1はこの銅緩衝システムを強化して腫瘍のエンザルタミド耐性を助けるため、著者らはPDHA1を標的とする薬剤がその状況を逆転できるかを検討した。彼らは同じ代謝複合体を撹乱する化合物CPI‑613を用いた。CPI‑613単独で前立腺がん細胞の銅ストレスを増加させミトコンドリアタンパク質を損傷させたが、正常な前立腺細胞は保護されたままだった。エンザルタミドと併用すると、CPI‑613はいずれか単独よりもはるかにがん細胞の増殖を抑え、数学的解析でも真の相乗効果が確認された。マウス腫瘍モデルや患者由来腫瘍移植でも、薬剤の組み合わせは腫瘍を小さくし、壊死組織を増やし、分裂中の細胞を減らし、銅駆動性の細胞死の特徴を強めた。
患者にとっての意義
総じて、本研究は一部の前立腺がんがエンザルタミドを回避するのは、代謝を書き換えてアセチルCoAを増やし、遺伝子発現を書き換えてグルタチオンを増やし、有毒な銅を吸収してカプロプトーシスを阻害するためであることを示す。PDHA1を阻害すればこの防御回路は解体され、銅駆動性細胞死が進行してホルモン遮断療法の効果が回復する可能性がある。臨床試験は必要だが、本研究は検証可能な具体的戦略を示している:エンザルタミドとCPI‑613のようなPDHA1標的薬を組み合わせて、進行した治療困難な前立腺がんにおける耐性を克服するという方策である。
引用: Zhuang, R., Zhou, Q., Cheng, B. et al. PDHA1–acetylation signaling suppresses cuproptosis to attenuate anti-androgen effect in prostate cancer. Cell Death Dis 17, 243 (2026). https://doi.org/10.1038/s41419-026-08462-1
キーワード: 前立腺がん, 薬剤耐性, 銅誘導性細胞死, がん代謝, エピジェネティック制御