Clear Sky Science · ja
可逆的なアルギニンのメチル化がミトコンドリアIDH2活性を制御する:CARM1とKDM3A/4Aによる協調的制御
細胞の発電所を微調整する
ミトコンドリアはしばしば細胞の発電所と呼ばれますが、単にエネルギーを作るだけではありません。体の要求に応じて燃料の使い方を絶えず調整しており、この制御が乱れると糖尿病、心不全、がんなどの疾患に寄与することがあります。本研究はミトコンドリア内に隠れた「ディマー(明るさ)スイッチ」を明らかにします。それは主要酵素IDH2の単一アミノ酸に付く小さな化学的タグで、ミトコンドリアが低出力でアイドリングするか、高出力で駆動するかを左右します。
小さなタグがもたらす大きな影響
細胞内のタンパク質は静的ではなく、小さな化学基で頻繁に修飾され、その振る舞いが変わります。細胞核や細胞質内で知られた修飾は多い一方で、ミトコンドリア内の修飾は十分に調べられていません。著者らはアルギニンのメチル化という特定の修飾に注目し、それがミトコンドリア酵素の働きを制御しているかを検討しました。彼らはTCA回路の働き手である酵素IDH2に着目し、蛋白質化学と質量分析を用いて、IDH2の一つの残基、アルギニン188に特異的なメチル基が付くこと、そしてこのマークが意外にもミトコンドリア内で働く酵素CARM1によって付与されることを突き止めました。
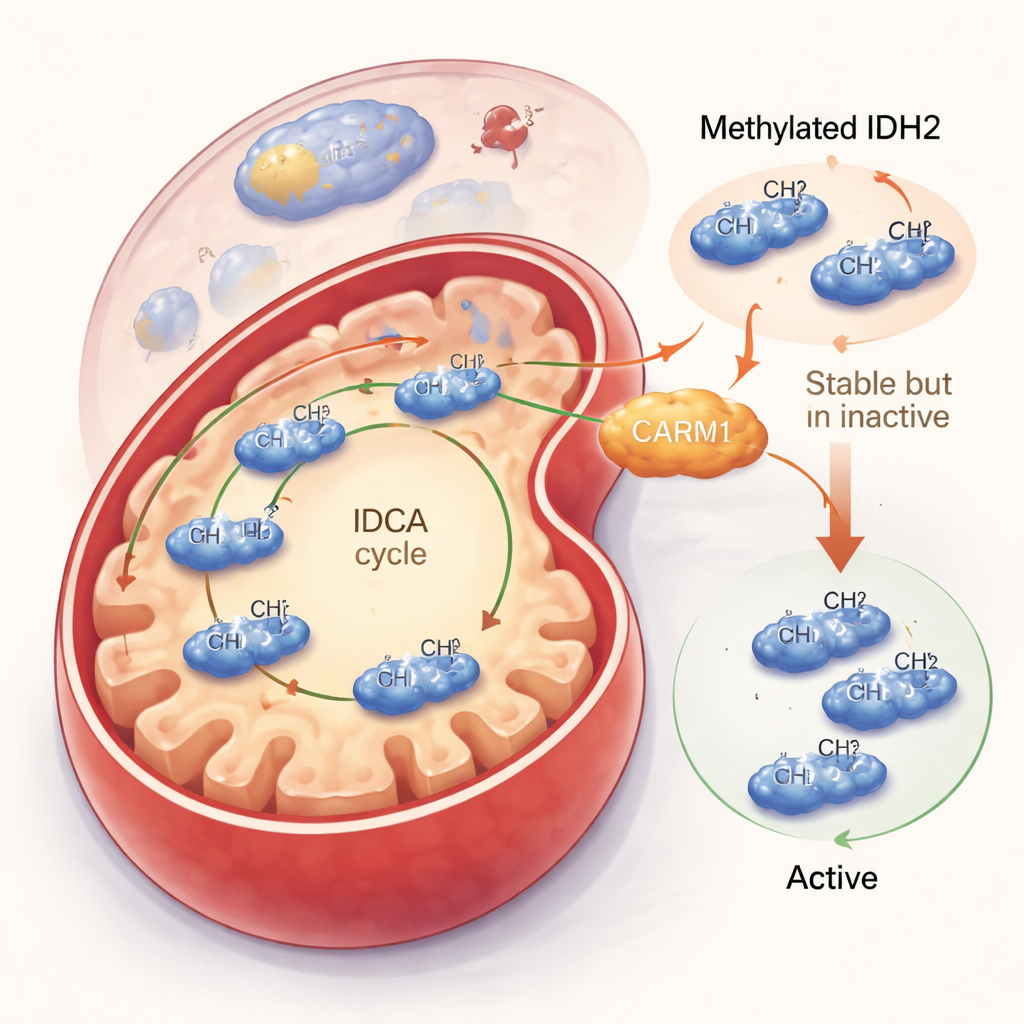
IDH2を抑えつつ寿命を延ばす
次にこのメチルタグが実際に何をするのかを調べました。CARM1が活性化してIDH2をメチル化すると、IDH2タンパク質はより安定になり細胞内で長く存在しました。しかしその見返りとして、メチル化されたIDH2は活性が低下しました。細胞実験や精製タンパク質試験で、メチル化IDH2は主要産物であるα-ケトグルタル酸を少なく生産し、保護的分子であるNADPHの産生も減少しました。一方、アルギニン188がメチル化されないIDH2のバージョンは、より活性な二量体形態を形成し、より速く働き、α-ケトグルタル酸とNADPHの両方を増加させました。全体量としては非メチル化IDH2は少なかったものの、個々の分子あたりの仕事量が大きく、ミトコンドリアの出力は純増しました。
二つの消去酵素による可逆的スイッチ
重要なのは、このメチルマークが恒久的ではないことです。研究者らは、通常は別種のタグを除去することで知られるリジン脱メチラーゼKDM3AおよびKDM4Aの二つが、IDH2のアルギニンメチルマークも除去できることを示しました。これらの脱メチラーゼが存在すると、位置188のメチル化アルギニンは付加基を失い、IDH2は安定性を下げる一方で活性は高まり、二量体形態が増加しました。KDM3AやKDM4Aが活性な細胞はミトコンドリア膜電位が高く酸素消費量も増え、酸化的代謝がより活発であることを示しました。これらの酵素が低下すると逆の現象が起き、IDH2活性とミトコンドリア機能が落ちるため、この制御は一方向の変化ではなく可逆的なシステムであることが強調されます。
代謝と疾患のつながり
IDH2はがんや他の疾患と関連づけられてきたため、著者らはこのメチル化スイッチが疾患においてどのような意味を持つかを調べました。様々な正常細胞株およびがん細胞株で、IDH2タンパク質量が多い場合にメチル化も増え、驚くべきことに酵素活性が低いことが多いと観察され、「タンパク質量が多い=機能が高い」とは限らないことを示しました。乳がんデータセットでは、IDH2タンパク質量が高い患者は生存率が低い傾向があり、IDH2遺伝子の発現自体は予後と一致しないことも示唆されました。これらの結果は、CARM1駆動のメチル化がTCA回路を遅らせ、細胞をがんが好む代謝経路へと傾ける一方で、KDM3AやKDM4Aのような脱メチラーゼはより効率的なエネルギー生産へ押し戻す可能性があるというモデルを支持します。
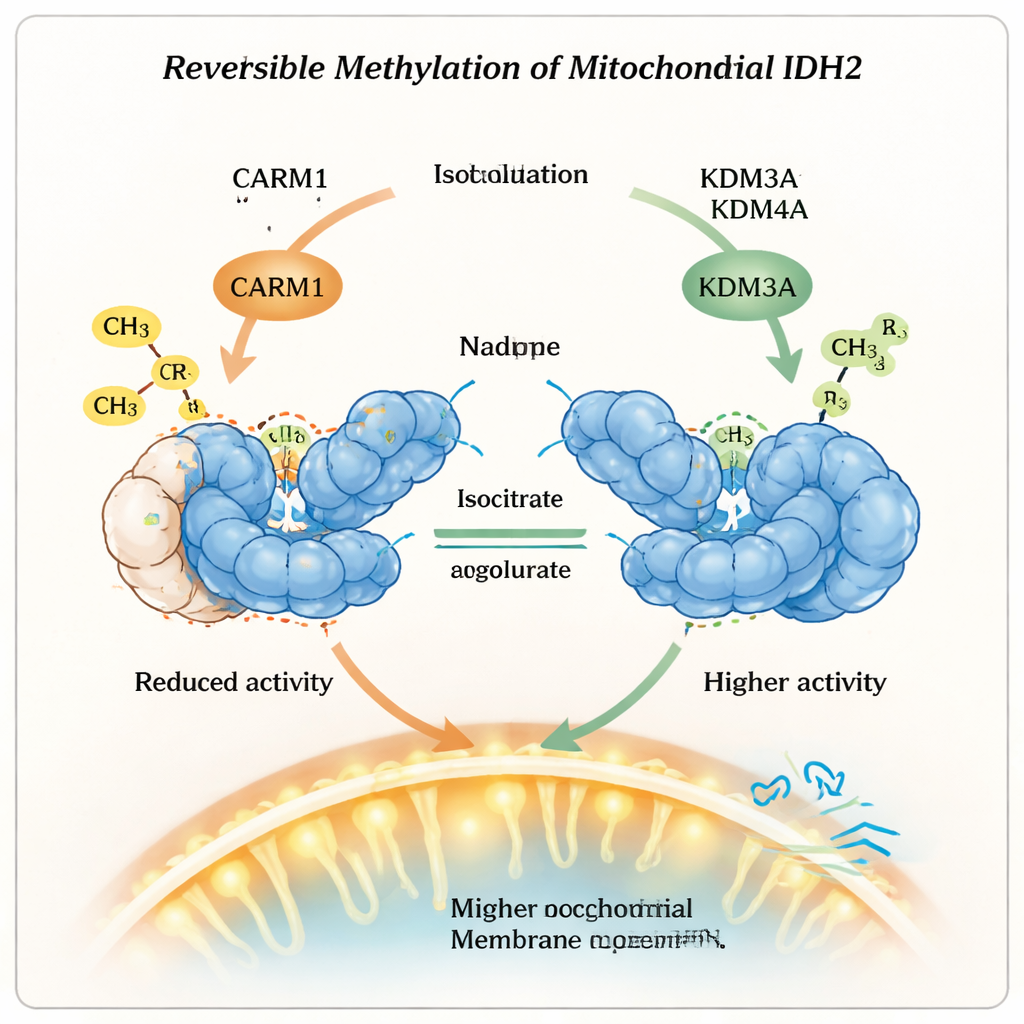
健康と治療への示唆
日常的な表現を借りれば、本研究はミトコンドリアが酵素を単純にオン・オフするのではなく、可逆的な化学タグを微調整用のダイヤルとして使っていることを示しています。CARM1がメチル基を付けることでIDH2は寿命を延ばすが活性は落ち、KDM3AおよびKDM4Aがそのタグを除去することで安定性を犠牲にして出力を高めます。このバランスは、細胞が速いが非効率的な糖の燃焼と、遅いが効率的なエネルギー生産のどちらを選ぶかに影響します。IDH2上のこのメチル化による“ディマー・スイッチ”の理解は、がんや代謝疾患のような状態で誤ったミトコンドリア代謝を修正することを目的とした治療法、すなわちこの小さいが強力な化学的マークを書き込む酵素や消去する酵素を標的にする新たな可能性を開きます。
引用: Cho, Y., Winarto, J., Song, DG. et al. Reversible arginine methylation regulates mitochondrial IDH2 activity: coordinated control by CARM1 and KDM3A/4A. Cell Death Dis 17, 195 (2026). https://doi.org/10.1038/s41419-026-08444-3
キーワード: ミトコンドリア, IDH2, アルギニンのメチル化, 細胞代謝, CARM1