Clear Sky Science · ja
ホノキオールはミトコンドリア標的の作用で腫瘍の発生と転移を阻止する
木の化合物をがん治療剤へ転用する
多くの抗がん薬は植物由来であり、科学者たちはこれら天然分子が細胞内でどのように働くかをいまだに解明しています。本研究は、伝統医療で長く用いられてきたモクレン(Magnolia)の樹皮に含まれる物質ホノキオールに焦点を当て、がん細胞内の小さな発電所を直接標的にして腫瘍増殖を抑え、転移を防ぎつつ、正常細胞には比較的影響を与えないことを示しています。
細胞の中の発電所
すべての細胞はミトコンドリア、いわゆる「発電所」に頼ってエネルギー分子ATPを生成します。がんではミトコンドリアは燃料を作る以上の役割を果たし、細胞が生き残るか死ぬかの判断にも関与します。大きな分子装置であるATP合成酵素はミトコンドリア内膜に位置しATPを合成します。がん細胞はしばしばIF1と呼ばれる補助タンパク質を過剰に産生し、これがATP合成酵素に結合して安全ロックのように働き、ミトコンドリア透過性移行(MPT)とそれに続く細胞死に対する耐性を高めます。
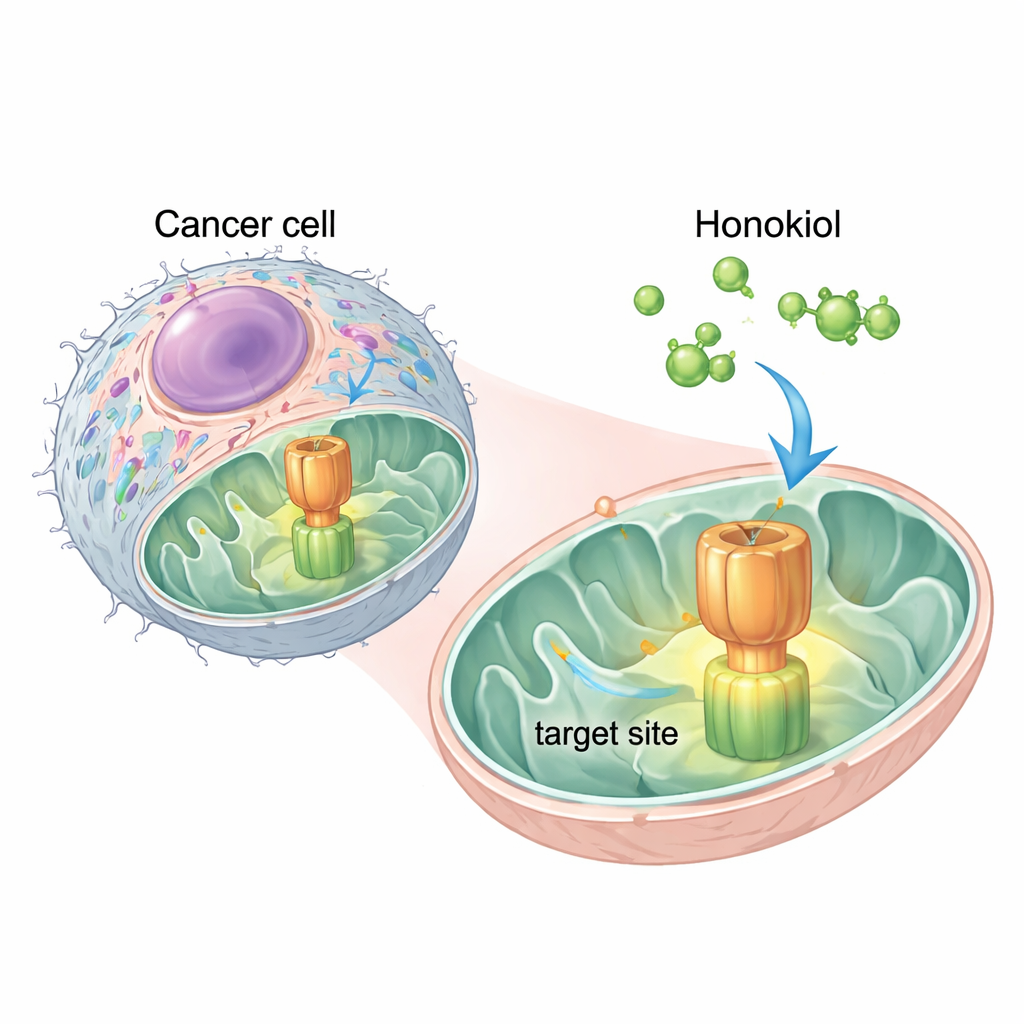
天然分子が見つけた決定的なスイッチ
研究者は計算機シミュレーションを用いてホノキオールがATP合成酵素のどこに結合するかを調べました。ATP合成酵素の構成要素の一つであるOSCPという領域に、有望な「ドッキング」部位が二つ見つかりました。最も強い部位はIF1がATP合成酵素に結合するパッチと重なっていました。これはホノキオールが分子のくさびのように作用し、OSCPに滑り込んでIF1を押しのける可能性を示唆します。ヒト子宮頸がん由来のHeLa細胞を使った実験はこの考えを支持しました。ホノキオールを添加するとIF1とOSCPの物理的接触が減少し、酵素の他の部分が乱されないことから、効果は特異的であることが示されました。
細胞から生体へ:より小さい腫瘍、減る転移
この分子的な作用が実際の影響を持つかを確かめるため、チームは発光するヒトがん細胞を小さなゼブラフィッシュ胚に移植しました。ゼブラフィッシュ胚は腫瘍成長と転移を追跡するための確立された全動物モデルです。IF1を多く持つ通常のHeLa細胞を注入した魚では、ホノキオール処理により腫瘍塊が著しく縮小し、遠隔部位へ広がるがん細胞の数が減少しました。そのパターンは保護タンパク質を欠くIF1ノックアウト細胞を注入した魚に似ていました。興味深いことに、IF1が欠損している場合でもホノキオールは転移細胞数を減らし、IF1に依存しない第2の転移抑制メカニズムが存在することが示唆されました。
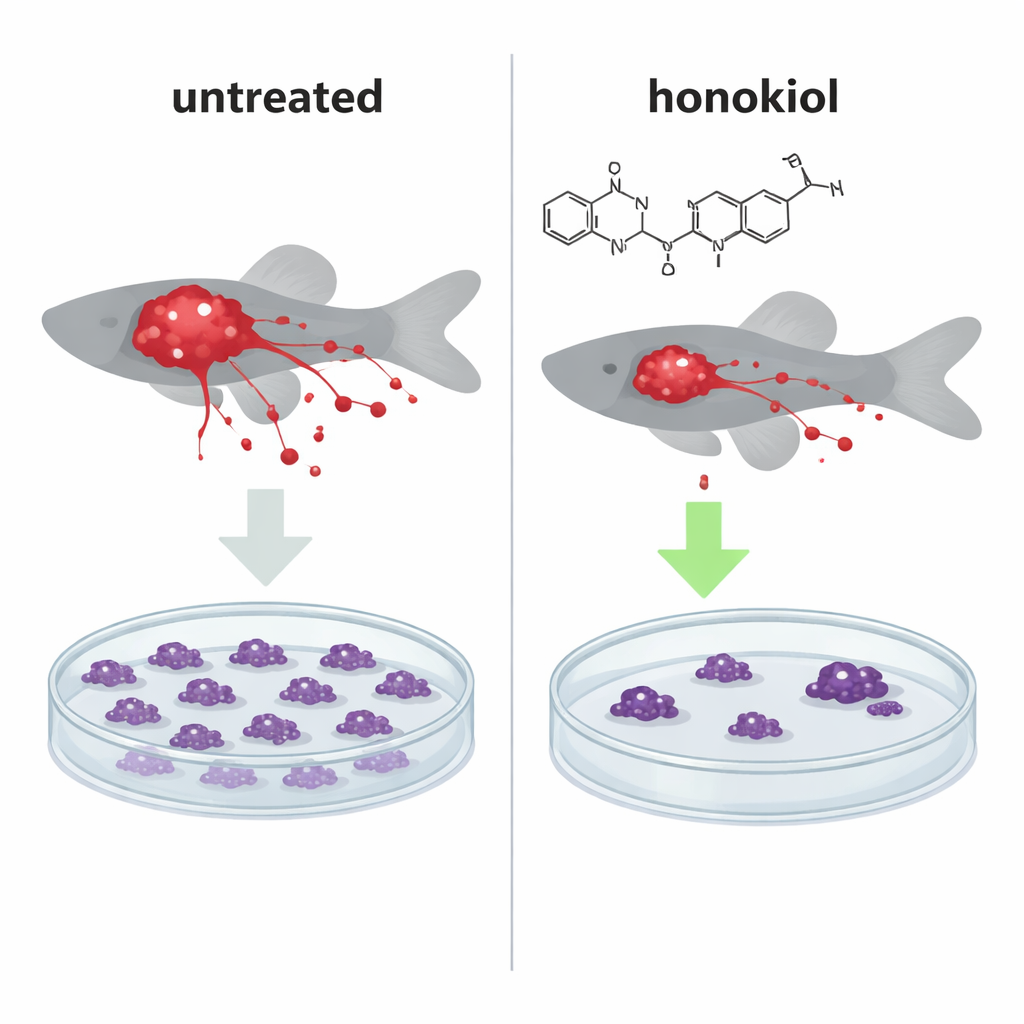
故障した発電所に自己破壊を促す
培養皿内の実験では、ホノキオールはがん細胞がソフトアガー中で大きなコロニーを形成する能力を低下させました。ソフトアガー試験は固形腫瘍内の低酸素で過酷な環境を模すものです。この効果は通常の細胞分裂や基礎的なミトコンドリア呼吸の大きな低下を伴わず、むしろミトコンドリアが生死を決める仕組みの変化を示しています。カルシウム取り扱いの測定により、ホノキオールはミトコンドリアがより低いカルシウム濃度で透過性移行ポアを開くようにし、これは膨張と死を促す因子の放出を引き起こす既知のトリガーであることがわかりました。適度な用量ではこの効果はIF1の解離に依存していましたが、高用量ではホノキオールはOSCPの第二の結合部位と反応性酸素種の増加を通じて作用し、IF1欠損細胞であってもプログラムされた細胞死に感受性を高めました。
がん細胞の移動を止める
がんが最も危険になるのは、細胞が剥がれて新たな臓器へ移動する場合です。創傷様の「スクラッチ」アッセイでは、ホノキオールはがん細胞シートの集団移動を強く遅らせ、腫瘍細胞に移動・浸潤能を与える上皮–間葉転換(EMT)のマーカーを低下させました。詳細な電子顕微鏡画像は、移動する細胞が通常、ミトコンドリアを拡大・再形成して内部のひだを増やし、先端部での高いエネルギー需要を満たすことを示しました。ホノキオール処理では、前面に位置するこれらのミトコンドリアがむしろ膨張し構造的に損傷し、透過性移行ポア開口の特徴を示しました。一方、非移動領域のミトコンドリアは影響が少ないか、IF1の状態に応じて数が増加することもありました。
将来のがん治療への示唆
簡潔に言えば、本研究はホノキオールがミトコンドリアのATP産生装置の小さな調節領域に的を絞り、がん細胞がしばしばロックしている内蔵の安全スイッチを切り替え得ることを示しています。IF1を押しのけポアの開口へ直接働きかけることで、ホノキオールは腫瘍細胞の自己破壊を促し、移動して転移の種をまく能力を低下させます。これらの効果は多くのがんが共有する特徴に基づいているため、ATP合成酵素のOSCP領域を標的にすることは、がん細胞の発電所の脆弱性を突きつつ正常組織への害を抑える新しい治療クラスの創出につながる可能性があります。
引用: Grandi, M., Boldrin, F., Risato, G. et al. Honokiol blocks tumor development and metastasis through mitochondrion-targeted effects. Cell Death Dis 17, 186 (2026). https://doi.org/10.1038/s41419-026-08441-6
キーワード: ホノキオール, ミトコンドリア, ATP合成酵素, アポトーシス, 転移