Clear Sky Science · ja
ミトコンドリアDNAがNLRP3に結合してミクログリアのNLRP3–IL-1β経路を活性化し、パーキンソン病モデルで神経変性を引き起こす
なぜパーキンソン病で重要なのか
パーキンソン病は振戦や運動の遅れで知られますが、これらの症状の背後では脳内で複雑な闘いが進行しています。本研究は、損傷を受けたミトコンドリア由来の小さな遺伝物質片が脳内の免疫細胞であるミクログリアに炎症を引き起こし、徐々に滑らかな運動に必要なドーパミン産生ニューロンを死に至らしめる仕組みを明らかにします。この連鎖反応を理解することで、パーキンソン様の損傷を遅らせたり防いだりする可能性のある、非常に特異的な薬剤標的が示されます。
ストレス下の脳の免疫細胞とエネルギー発電所
脳にはニューロンだけでなく常在免疫細胞であるミクログリアも存在します。パーキンソン病では、これらのミクログリアが過剰に活性化し、近傍のニューロンを傷つける有害な分子や炎症性シグナルを放出することがしばしば起こります。著者らは細胞の“発電所”であるミトコンドリアに注目しました。ミトコンドリアは独自のDNAを持ちますが、毒素や加齢、その他のストレスによって損傷を受けると、そのDNAは酸化され、活性酸素種による化学的な損傷を被ります。ミトコンドリアDNAは細菌DNAに類似しているため、こうした損傷片は脳内で警報信号のように働き、免疫系を刺激して慢性的な炎症を引き起こす可能性があります。
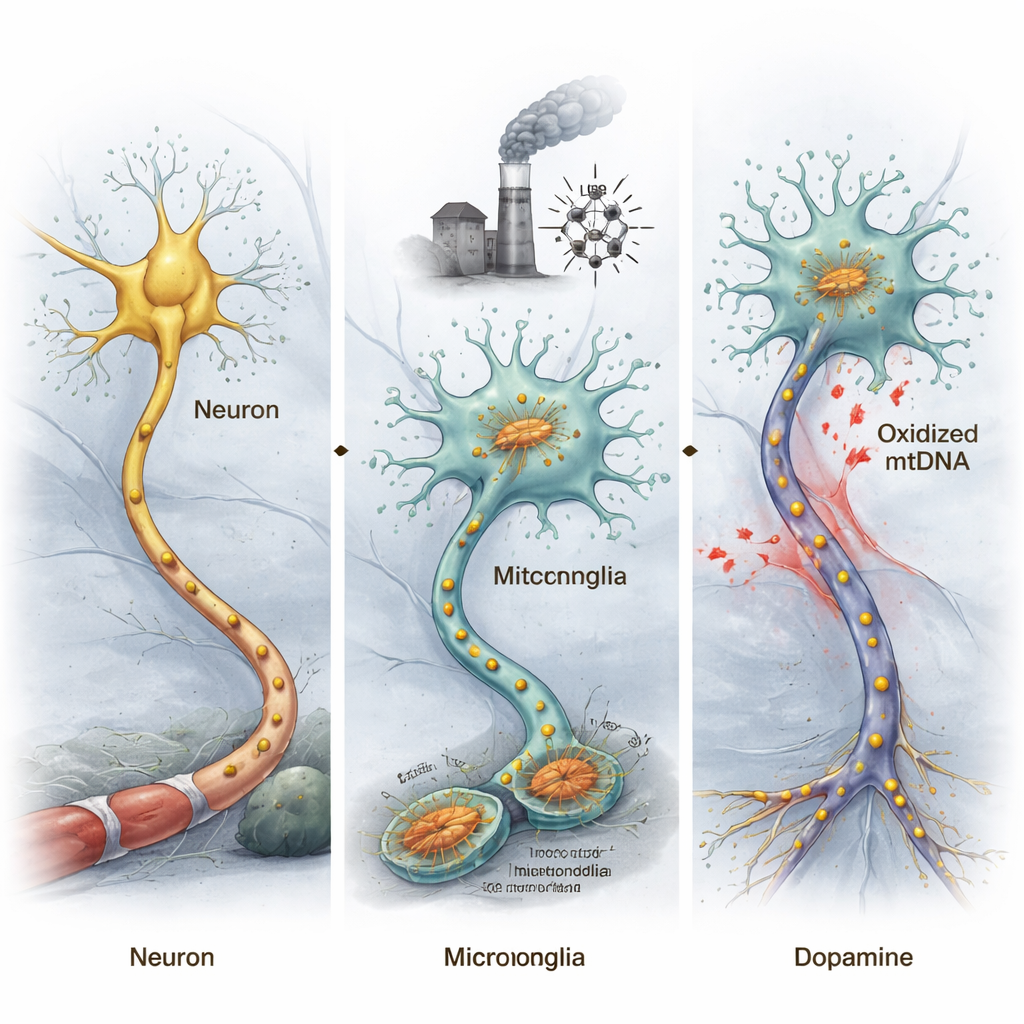
損傷したミトコンドリアDNAはマウスをパーキンソン様に傾ける
酸化ミトコンドリアDNA(ox-mtDNA)が実際にパーキンソン様の変化を誘導するかを確かめるために、研究者らはストレスを受けたミクログリアからox-mtDNAを抽出し、運動に重要なドーパミン産生ニューロンが存在する脳領域に直接注入しました。このox-mtDNAにさらされたマウスは行動試験で運動量が減少し、これらのドーパミンニューロンが失われ、パーキンソン病の中核的特徴が再現されました。中脳からニューロンとミクログリアを分離して遺伝子発現を解析すると、ニューロン側ではパーキンソン病に関連する遺伝子がより異常を示し、ミクログリア側では炎症関連遺伝子が強く活性化していることがわかりました。
ミクログリア内部の分子アラームスイッチ
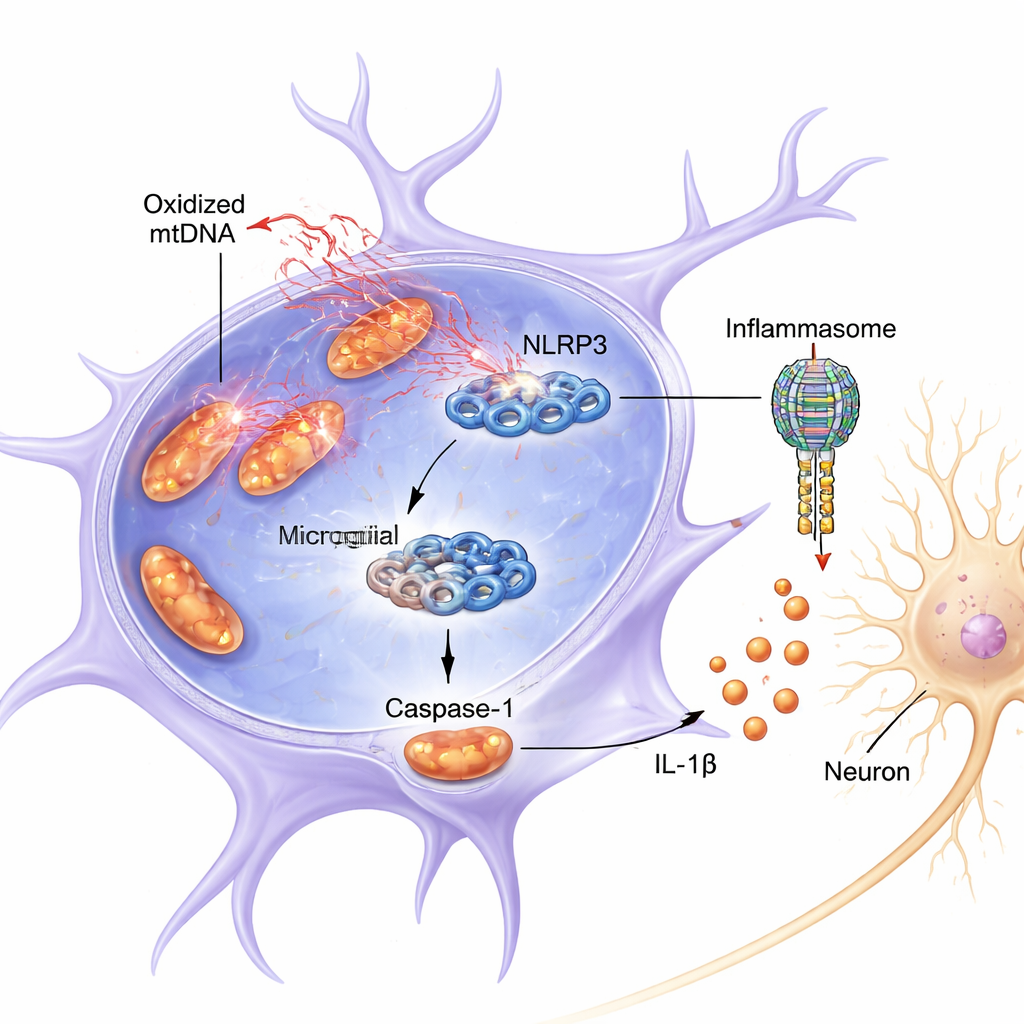
本研究はミクログリア内のタンパク質複合体であるNLRP3に着目しました。これはインフラマソームと呼ばれるより大きな装置の一部です。NLRP3が作動するとカスパーゼ-1が活性化され、炎症性分子IL-1βを切断して活性型の有害な形にします。マウスおよび培養細胞の両方で、炎症の一次刺激(LPS、細菌成分)と農薬様毒物ロテノンの組み合わせは、ミクログリアのミトコンドリアから酸化されたmtDNAを細胞質へ放出させました。この放出はNLRP3の強い活性化、より多くの切断(活性化)されたカスパーゼ-1、そして高いIL-1βレベルと一致しました。これらの過剰活性化したミクログリアから採取した培養上清は、試験管内で育てたドーパミン様ニューロンに直接毒性を示し、生存率と主要マーカーであるチロシンヒドロキシラーゼの量を低下させました。
直接結合:酸化DNAがNLRP3スイッチを切り替える仕組み
単なる相関を超えて、著者らはox-mtDNAが炎症時に存在するだけでなく、物理的にNLRP3に結合してそれを作動させていることを示しました。ミトコンドリアDNAの放出を薬で阻害すると、カスパーゼ-1とIL-1βの活性化は低下しました。逆に酸化されたmtDNAを直接ミクログリアに導入すると、非酸化のmtDNAよりも強くNLRP3シグナルが増強されました。生化学的なプルダウン実験では、酸化損傷マーカーを多く含むmtDNAがNLRP3に付着しているのが検出されました。計算モデルとタンパク質化学の解析は、ox-mtDNAがNLRP3の正に帯電した柔軟な領域(アミノ酸180–187にまたがる「本質的に無秩序な領域」)に結合することを示しました。この重要な配列をNLRP3から除去すると、ox-mtDNAの結合能とカスパーゼ-1活性化能は大幅に低下しました。
インフラマソームを止めればニューロンは救われる
研究者らは次に、NLRP3を妨げればニューロンを保護できるかを検証しました。培養ミクログリアでNLRP3を遺伝学的に低下させると、LPSとロテノン処理後のカスパーゼ-1およびIL-1βの活性化は著しく低下し、これらの細胞由来の条件培地はドーパミン様ニューロンに対する毒性が大幅に減少しました。マウスでは選択的NLRP3阻害剤(MCC950)がミクログリアの活性化を抑え、ドーパミンニューロンを保持し、LPS+ロテノンや注入されたmtDNAで駆動されるモデルにおけるインフラマソーム関連タンパク質を低下させました。これらの実験は、ox-mtDNA–NLRP3–IL-1β連鎖が単なる関連にとどまらず、観察されたニューロン喪失の多くに必要であることを示しています。
将来のパーキンソン治療への示唆
専門外の読者向けに言えば、要点は次のとおりです。脳の免疫細胞から漏れ出した損傷したミトコンドリアDNAが内部の「アラームスイッチ」(NLRP3)に直接取り付き、炎症の波を引き起こしてドーパミンニューロンを損傷し、モデルにおいてパーキンソン様の病態を推進するということです。この相互作用はNLRP3タンパク質の短く特定された領域とミトコンドリアDNAの酸化された性質に依存するため、極めて具体的な新たな薬剤標的を提供します。ミトコンドリアDNAの損傷や放出を防ぐ、NLRP3への結合を阻害する、あるいはNLRP3自体を抑える療法は、この炎症カスケードを鎮め、パーキンソン病の進行を遅らせる可能性があります。
引用: Gan, Q., Fu, X., Zhou, T. et al. Mitochondrial DNA drives NLRP3-IL-1β axis activation in microglia by binding to NLRP3, leading to neurodegeneration in Parkinson’s disease models. Cell Death Dis 17, 213 (2026). https://doi.org/10.1038/s41419-026-08424-7
キーワード: パーキンソン病, ミクログリア, ミトコンドリアDNA, NLRP3インフラマソーム, 神経炎症