Clear Sky Science · ja
酸性腫瘍微小環境におけるSLC26A3のラクトイル化が結腸直腸癌の悪性進行を促進する
なぜ腫瘍の酸性度が重要なのか
結腸直腸癌は依然として世界で最も致命的ながんの一つであり、その理由の一端は腫瘍が再発、転移、あるいは薬剤に反応しなくなることが多い点にあります。本研究は、そうした挙動の背後にあるあまり注目されてこなかった原因――腫瘍内部の酸性で乳酸に富む環境――を掘り下げます。著者らは、この過酷な環境が保護的な膜タンパク質SLC26A3を不安定化させる仕組みを明らかにし、がん細胞が幹細胞様の性質を獲得し、浸潤性や薬剤耐性を高める新たな連鎖反応を示しています。これにより治療の新しい着眼点が提示されます。
がん細胞を取り巻く過酷な環境
急速に増殖する腫瘍は大量の糖と酸素を消費し、乳酸と水素イオンを放出して周囲を酸性にします。大規模な患者データと組織標本を用いて、研究者らはCA9と呼ばれるマーカータンパク質で追跡されるこの酸性状態が攻撃的な結腸直腸腫瘍と相関していることを示します。進行したがんではCA9の発現が高く、一方でSLC26A3の発現は一貫して低くなっています。SLC26A3は通常、結腸細胞の表面に局在して塩類と重炭酸イオンのバランスを保ち、それによって酸性度を調節します。腫瘍組織、がん細胞株、単一細胞解析において、酸性度が上がるとSLC26A3のレベルが低下すること、特に悪性で幹細胞様のがん細胞で顕著であることが確認されました。 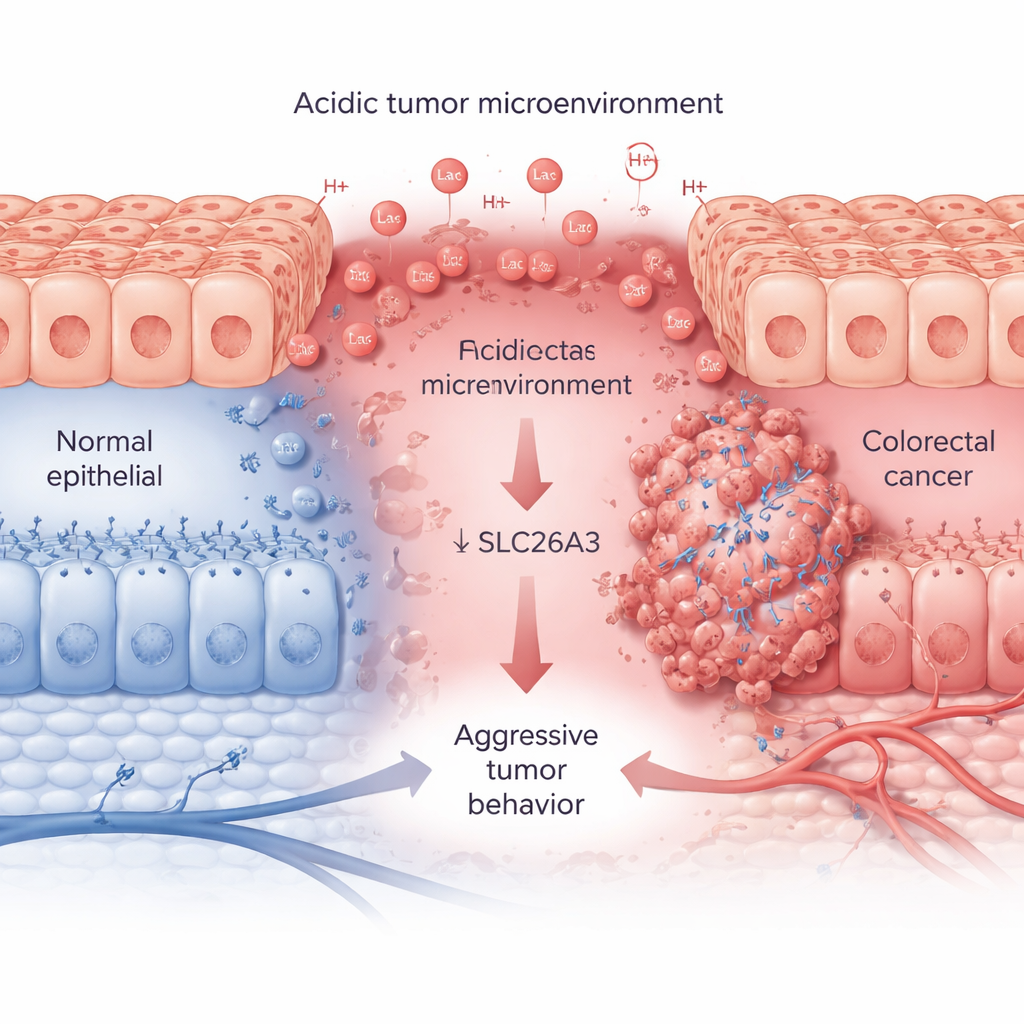
乳酸が破壊対象に印を付ける仕組み
著者らは次に、なぜ酸性腫瘍でSLC26A3が減少するのかを探ります。注目したのはラクトイル化です。これは乳酸由来の新しく注目された化学的修飾で、タンパク質に付加され得ます。結腸直腸がん細胞を乳酸にさらすか酸性条件で培養すると、SLC26A3は強くラクトイル化されます。詳細なタンパク質解析により、K536という一つのアミノ酸残基がこの修飾の主要部位であることが特定されました。K536のラクトイル化はSLC26A3の安定性を低下させ、ユビキチンという「処分」の標識が付きやすくなり、細胞の分解機構へ送られます。ラクトイル化を付加するのを助ける酵素p300を阻害すると、SLC26A3の分解が部分的に保護されます。結果として、酸性と乳酸は悪循環を生み出します――乳酸が増えるとラクトイル化が進みSLC26A3が減少し、pHの恒常性がさらに乱れてより酸性の微小環境を助長します。
がんの幹性と浸潤にかかるブレーキを外す
SLC26A3が枯渇すると、がん細胞はより攻撃的なふるまいを示します。培養系では、結腸直腸がんの幹様細胞は非幹様細胞に比べて自然にSLC26A3の発現が低いことが観察されます。研究者らがSLC26A3を意図的に低下させると、腫瘍細胞は球状コロニー(幹性の指標)をより多く形成し、自己再生能が高まり、人工膜を介してより侵襲的になり、スクラッチアッセイでは移動速度が増します。さらにオキサリプラチンや5‑フルオロウラシルといった一般的な化学療法薬への感受性も低下します。逆にSLC26A3を増やすと幹性マーカーが減り、浸潤や移動は抑えられますが、追加の乳酸を加えるとこの有益な効果は弱まり、酸性環境が保護効果を打ち消し得ることを示しています。
遺伝子制御への隠れた連結
SLC26A3は酸性度の調節に寄与する以外に、HuRとCUGBP1という二つのRNA結合タンパク質を結び付ける足場としても働きます。これらのタンパク質は多くのがん関連タンパク質をコードするメッセンジャーRNA(mRNA)の寿命を制御します。SLC26A3が十分に存在すると、それは一部のHuRやCUGBP1を拘束し、特定のがん関連メッセージの安定化や不安定化を抑制します。SLC26A3がラクトイル化され分解されると、HuRやCUGBP1はより自由に発がん性mRNAに結合できるようになり、幹性、上皮間葉転換(EMT)、浸潤、生存を促進します。実験ではHuRが幹性マーカーや細胞接着タンパク質のmRNAを安定化する一方、CUGBP1は一部の標的でHuRと拮抗し、接着の一体性を低下させEMTを促すことで腫瘍の拡散に寄与することが示されました。
環境の再均衡でがんに対抗する
これらの知見を治療戦略に結びつけられるか検証するために、研究者らは結腸直腸がんのマウスモデルを用いました。腫瘍の酸性度を重炭酸ナトリウムで中和する、MCT1阻害剤で乳酸輸送を阻害する、またはSLC26A3を過剰発現させるいずれも腫瘍成長を遅延させました。SLC26A3の回復と化学療法を組み合わせると腫瘍はさらに縮小しました。患者データではSLC26A3の高発現が生存率の向上、再発の低下、転移の減少、化学療法への良好な反応と相関しており、このタンパク質がバイオマーカーかつ治療標的になり得ることを示唆しています。 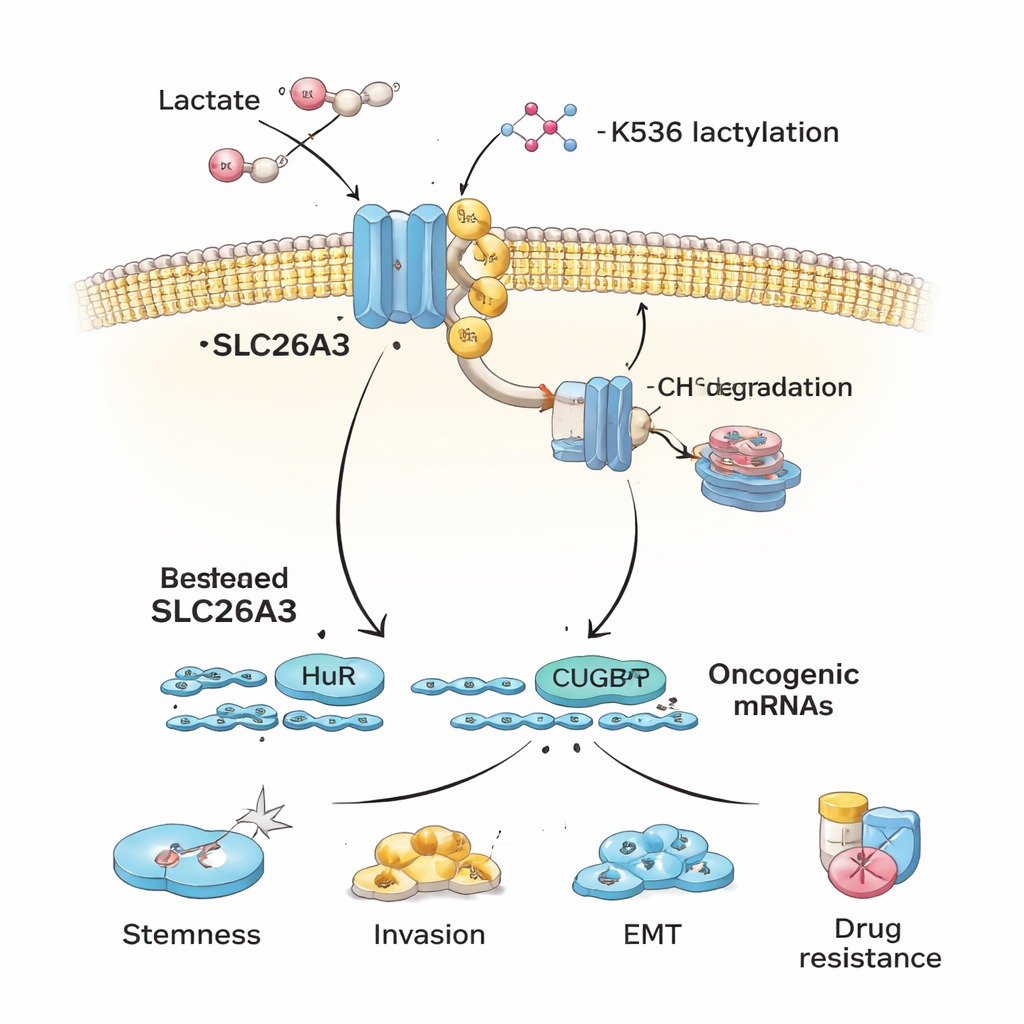
患者にとっての意味
平たく言えば、本研究は結腸直腸腫瘍が酸っぱい乳酸に富む環境で繁栄し、そこが保護的な門番であるSLC26A3に化学的な「印」を付けて破壊することを示しています。門番が失われると、がん細胞は幹細胞様の性質を取りやすくなり、拡散や治療抵抗性が高まり、細胞内の強力なRNA調節因子がそれを助長します。腫瘍の酸性を緩和する、乳酸の取り扱いを阻害する、あるいはSLC26A3を回復させることで、その悪性のフィードバックループを弱め、標準治療の効果を高められる可能性があります。こうしたアプローチはまだ厳密な臨床試験を要しますが、腫瘍の化学的な環境を管理することで結腸直腸癌を制御する新たな有望な観点を開きます。
引用: Chen, C., Cai, D., Liu, X. et al. Lactylation of SLC26A3 in the acidic tumor microenvironment promotes malignant progression of colorectal carcinoma. Cell Death Dis 17, 164 (2026). https://doi.org/10.1038/s41419-026-08422-9
キーワード: 結腸直腸癌, 腫瘍微小環境, ラクトイル化, がん幹細胞, 化学療法耐性