Clear Sky Science · ja
GNG4を標的とすることで自動消化(オートファジー)を抑制し、前立腺がんの腫瘍進展を抑えエンザルタミド感受性を回復させる
この研究が重要な理由
進行した前立腺がんの多くの男性では、エンザルタミドのような強力なホルモン阻害薬が当初はよく効くものの、時間とともに効果が弱まります。本研究は腫瘍細胞が用いる生存戦略を明らかにし、GNG4と呼ばれる特定のタンパク質ががんの増殖を助け、治療に抵抗する仕組みを示しています。このメカニズムの理解は、既存薬の効果をより長く、より強く保てる併用療法の開発につながる可能性があります。
目に見える場所に潜むタンパク質のスイッチ
前立腺がん細胞は男性ホルモンに強く依存しているため、進行がんの標準治療はこれらの信号を遮断します。それでも多くの腫瘍は最終的に「去勢抵抗性」となり再び増殖を始めます。著者らは、同一患者の腫瘍組織と周辺の正常前立腺組織を比較し、腫瘍で著しく活性化されている遺伝子を探索しました。その候補の中でGNG4が際立っており、前立腺がん細胞でその発現を下げると腫瘍細胞の増殖が著しく低下しました。数百例の患者サンプルの解析でも、GNG4は正常組織より原発性前立腺がんで高く、特により悪性度の高い腫瘍で上昇していることが確認されました。
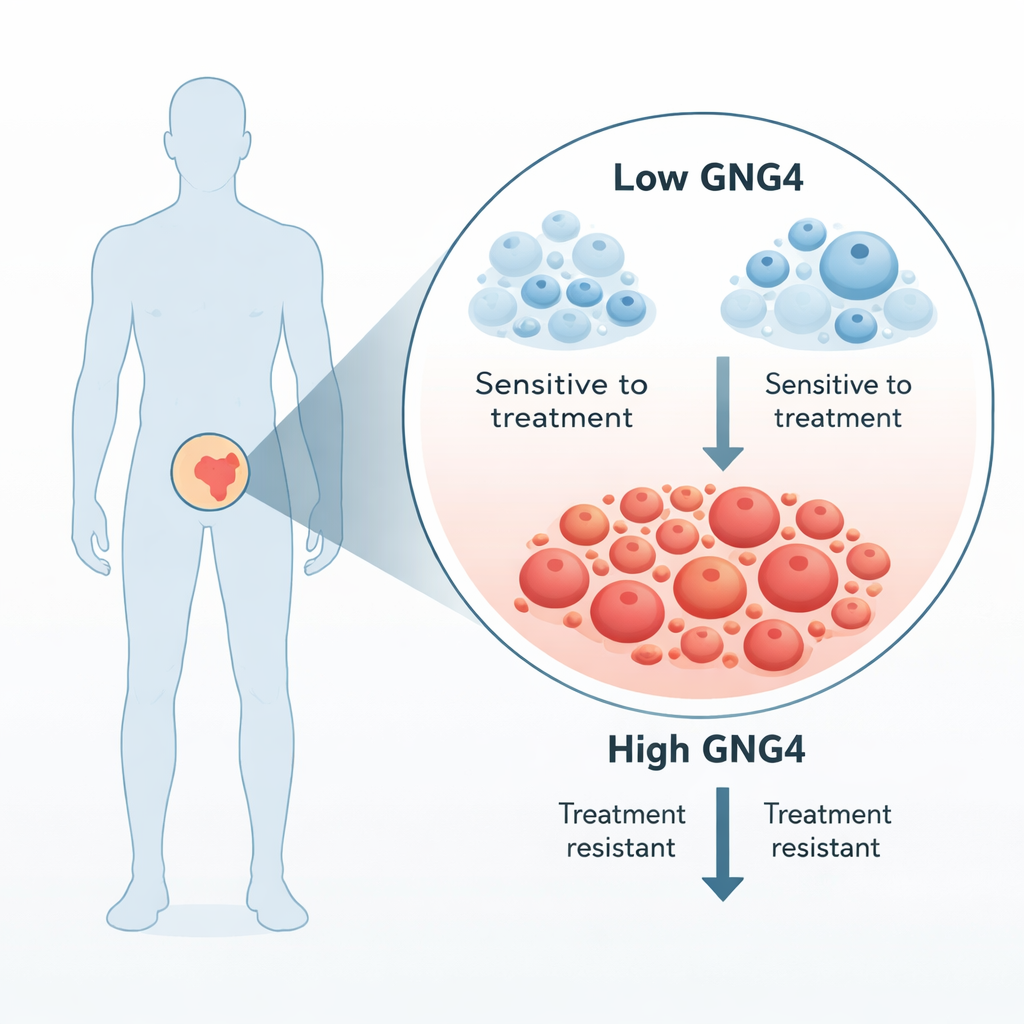
GNG4が腫瘍を生かす仕組み
GNG4はGタンパク質として知られる大きなシグナル伝達ファミリーの一部で、細胞膜に位置して外部からの信号を細胞内部に伝えます。研究チームは前立腺がん細胞株でGNG4を抑えると細胞分裂が遅くなり、細胞周期のチェックポイントで停止し、プログラム細胞死が増加することを示しました。これらの変化はまた、がん細胞の移動能や創傷閉鎖能を実験室で低下させ、GNG4欠損細胞から形成された腫瘍はマウスでも成長が遅れました。これらの結果は、GNG4が前立腺がんの増殖と転移に対するアクセルの役割を果たしていることを示唆します。
オートファジー:がん細胞の非常用備蓄庫
研究者らは次にオートファジーと呼ばれる過程に注目しました。これは細胞が飢餓や薬剤治療などのストレスに対処するために自らの構成要素を分解・再利用する仕組みです。多くの進行がんではオートファジーが非常用の備蓄庫として働き、厳しい環境に対処するのを助けます。本研究ではGNG4活性が高い前立腺がん細胞はオートファジーの活性化の指標を多く示し、GNG4をノックダウンした細胞ではリサイクリング構造が減少し、主要なオートファジーマーカーのレベルも低下していました。GNG4を過剰発現させると細胞はエンザルタミドに対して耐性を示し、細胞死が減りました。化学的阻害剤でオートファジーを遮断するとこの保護効果の多くが消え、GNG4が主にオートファジーを増強することで治療耐性を助けていることが示唆されます。
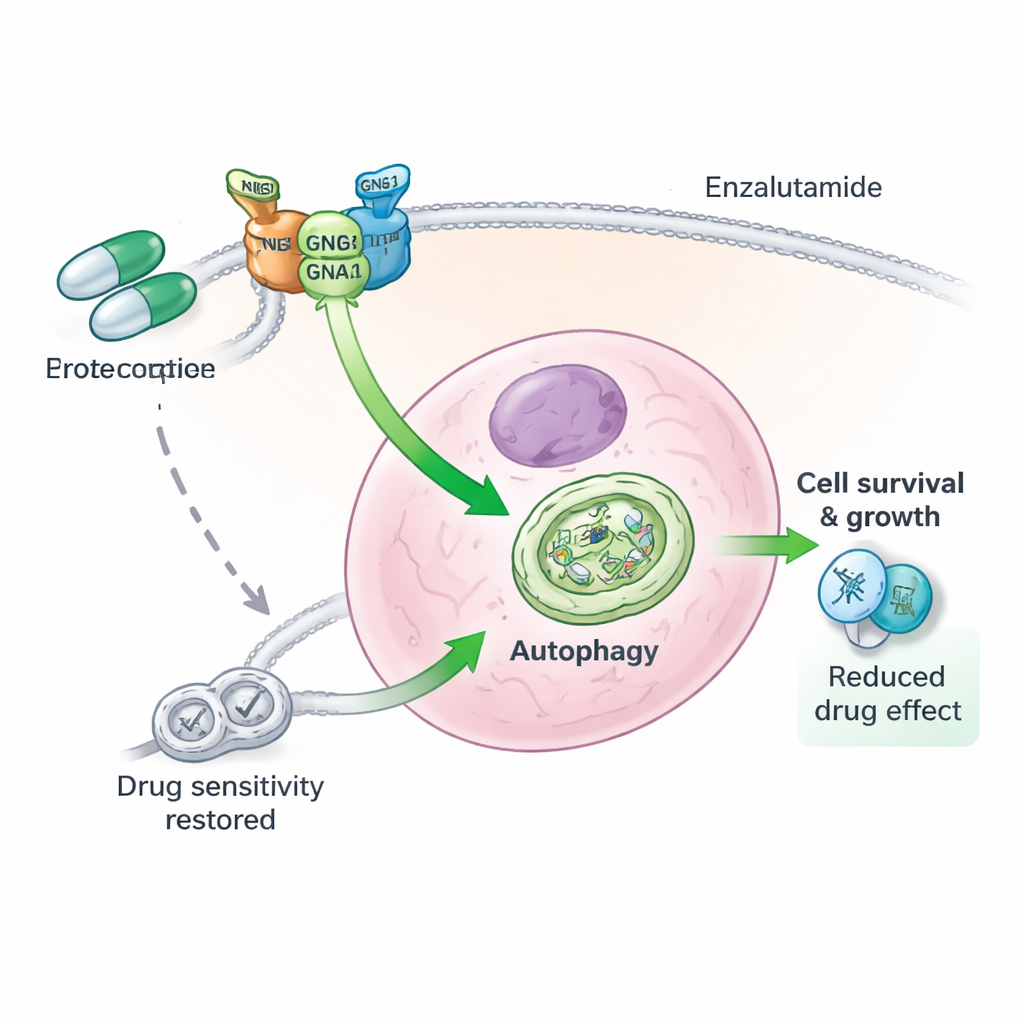
薬剤耐性の背後にある三者タンパク質チーム
さらに掘り下げると、GNG4は単独で働いているわけではありませんでした。GNG4は別のGタンパク質サブユニットであるGNB1と物理的に結合し、三つ目のタンパク質GNAI3を安定化させます。これら三つのサブユニットは協働して、前立腺がん細胞内のオートファジーを促進する機能的な複合体を形成します。GNG4を減らすと、GNAI3タンパク質はより速やかに標的化され分解装置によって分解され、オートファジーシグナルが遮断されました。GNAI3自体を除去すると、過剰なGNG4がもたらす増殖や生存の優位性は細胞培養でもマウス腫瘍でも打ち消されました。言い換えれば、GNG4は主にこのGNG4–GNB1–GNAI3軸を介して悪性化とストレス耐性を駆動しているのです。
既存薬の効果を高める
最後に、研究チームはGNG4の標的化をエンザルタミドと組み合わせた場合を検討しました。培養系ではGNG4のノックダウンはがん細胞をエンザルタミドに対して著しく感受性にし、治療後のコロニー形成能を低下させました。マウスではGNG4が低下した腫瘍はエンザルタミド投与で正常なGNG4レベルの腫瘍よりもより縮小し、明らかな増悪な毒性は観察されませんでした。オートファジーを直接阻害しても類似の改善が得られました。これらの結果は、GNG4が駆動するオートファジーを妨げることで腫瘍細胞の重要な生存手段を奪い、既存のホルモン阻害療法がより強力で持続的な効果を発揮できるようになることを示唆しています。
患者への意義
専門外の方への要点は、いくつかの前立腺がんが内部のリサイクルシステムを作動させることで治療を生き延びる、ということです。このシステムはバックアップ発電機のように働きます。本研究はGNG4をそのシステムをオンにする主要なスイッチとして同定し、パートナータンパク質と協働してエンザルタミドからがん細胞を守ることを明らかにしました。このスイッチをオフにする――直接GNG4を標的にするか、または安全にオートファジーを抑えることで――将来の治療は腫瘍の増殖を遅らせ、治療が効きにくくなった患者の薬剤感受性を回復させる可能性があります。
引用: Chen, L., Zhang, J., Hu, Y. et al. Targeting GNG4 inhibits tumor progression and restores enzalutamide sensitivity in prostate cancer by suppressing autophagy. Cell Death Dis 17, 160 (2026). https://doi.org/10.1038/s41419-026-08421-w
キーワード: 前立腺がん, 薬剤耐性, オートファジー, Gタンパク質, エンザルタミド