Clear Sky Science · ja
ENO1を標的にすることでマクロファージの極性が再プログラムされ抗腫瘍免疫が誘導され放射線療法の治療効果が改善される
腫瘍の盾を標的に変える
がんは単に急速に増殖するだけでなく、静かに身体の防御を無力化して生き延びることが多い。本研究はENO1という、腫瘍が免疫を回避し放射線治療に抵抗するのに関与する隠れた分子を探る。ENO1を標的とする新規抗体薬を開発することで、研究者たちは腫瘍の保護化学物質を減らし、免疫細胞を覚醒させ、結腸直腸がんやトリプルネガティブ乳がんのモデルで放射線の効果を高めることが可能であることを示した。 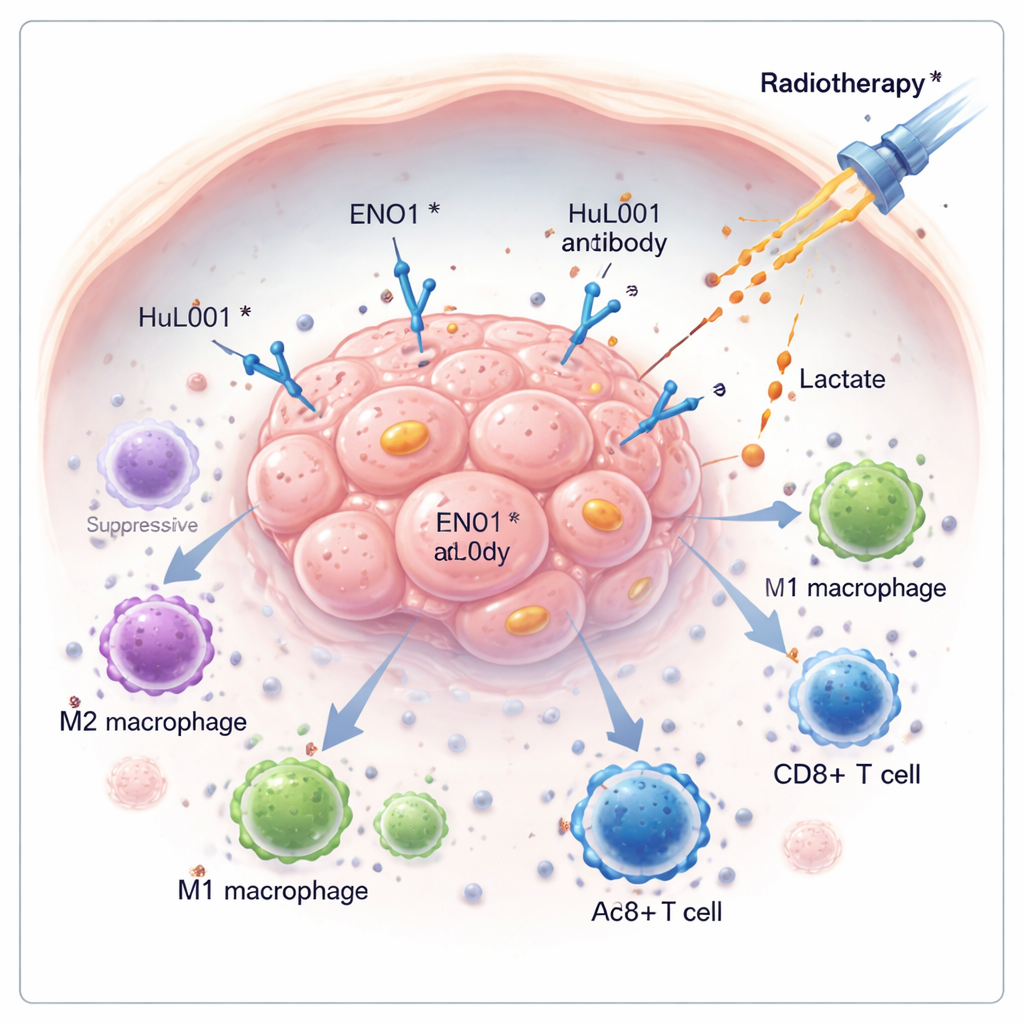
免疫を沈黙させる代謝のトリック
多くの腫瘍はエネルギー利用を書き換え、酸素がある場合でも大量の乳酸を生成する糖分解の経路を採る。この乳酸はがん細胞から外に排出され、腫瘍周囲に蓄積して厳しい酸性のニッチを作り、免疫攻撃を弱める。本研究では、糖分解に関与する酵素でありながらがん細胞表面にも現れることがあるENO1に着目した。細胞表面に存在すると、ENO1はMCT4というトランスポーターと連携して乳酸の輸出を助け、腫瘍成長を促し免疫細胞を抑制する環境を形成する。
放射が思わぬ裏目に出る仕組み
放射線療法は腫瘍のDNAを損傷し免疫応答を誘導するよう設計されているが、腫瘍微小環境内で副作用も生じる。研究チームは、放射線によって増強されるTGFβ1という分子に駆動されるシグナルが、ENO1を化学修飾しそれをがん細胞表面へ移動させる酵素(PRMT5)を活性化することを見出した。表面に移ったENO1はMCT4と物理的に相互作用してMCT4を安定化し、乳酸の排出を促進する。進行した結腸直腸がんやトリプルネガティブ乳がんの患者では表面ENO1濃度が高く、転移の増加や生存率の低下と関連しており、放射線が意図せず乳酸駆動の免疫抑制的シールドを強化し得ることを示唆している。
味方と敵の免疫細胞を再プログラムする
腫瘍の周囲に形成される酸性ハローの中で、マクロファージと呼ばれる免疫細胞は「治癒型」(一般にM2と呼ばれる)状態に追い込まれ、炎症を抑え修復を助けることでむしろ腫瘍を助長し攻撃を行わなくなる。研究者らはヒト化抗体HuL001を作製し、マウスとヒトのがん細胞表面に出たENO1の両方を認識させた。細胞培養およびマウスモデルでHuL001はENO1がMCT4を支える作用を阻害し、乳酸放出を減らし、マクロファージを腫瘍促進性のM2からより攻撃的でがん細胞の貪食に優れたM1状態へと変換させた。重要なのは、HuL001が単にマクロファージを殺すのではなく、それらを再教育しつつがん細胞死を直接増加させた点である。
放射線の効果を高める
結腸直腸がんおよびトリプルネガティブ乳がんのマウスモデルでHuL001を放射線療法と併用すると、腫瘍はより縮小し再発は遅れ、多くの動物で腫瘍が完全に消失した。 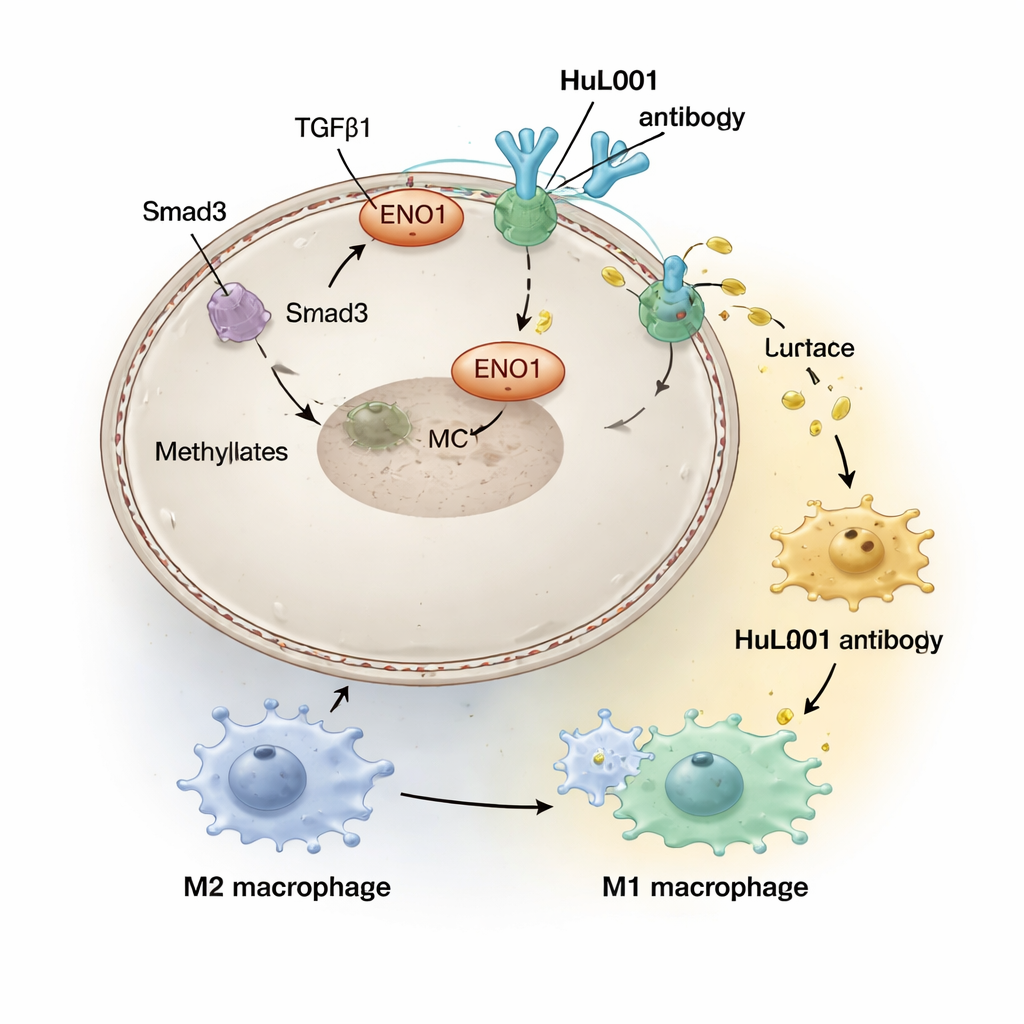
複雑な経路から実践的な可能性へ
専門外の読者に向けた本研究のメッセージは、腫瘍の化学環境とその周囲の免疫細胞群が深く結びついているということだ。ENO1は交差点に位置し、腫瘍が糖を燃やし乳酸を排出し、間違った種類の免疫支援を呼び寄せるのを助ける。表面ENO1を標的抗体で遮断することで、有害な乳酸の蓄積を減らし、マクロファージを腫瘍の助け手から敵へと反転させ、手ごわい治療モデルにおいて放射線の効果を高めることができた。HuL001はまだ臨床薬ではないが、ENO1のような代謝の門番を標的にすることは、腫瘍自身の防御を逆手に取り放射線療法など既存治療を強化する有力な方法になり得ることを示唆している。
引用: Lin, YS., Chang, HY., Hong, WZ. et al. Targeting ENO1 reprograms macrophage polarization to trigger antitumor immunity and improves the therapeutic effect of radiotherapy. Cell Death Dis 17, 194 (2026). https://doi.org/10.1038/s41419-026-08416-7
キーワード: 腫瘍代謝, マクロファージの極性, 放射線療法, 免疫療法, 乳酸